Najnoviji trendovi u terapijskoj primjeni konstruiranih materijala za pročišćavanje krvi za bubrežne bolesti
Jul 10, 2023
Abstract
Pročišćavanje krvi je uobičajena metoda za uklanjanje viška metaboličkog otpada u krvi u terapiji zamjene bubrega. Dovoljno uklanjanje ovih toksina iz krvi može smanjiti komplikacije i poboljšati životni vijek pacijenata na dijalizi. Međutim, trenutni biološki materijali za pročišćavanje krvi u kliničkoj praksi nisu idealni, gdje postoji nezadovoljena potreba za proizvodnjom novih materijala koji imaju bolju biokompatibilnost, smanjenu toksičnost i, posebno, efikasnije stope uklanjanja toksina i niže troškove proizvodnje. S obzirom na to, ovaj pregled je pažljivo sumirao novorazvijene različite strukturne biomedicinske materijale za pročišćavanje krvi u smislu tipova i strukturnih karakteristika materijala za pročišćavanje krvi, procesa proizvodnje, kao i međufaznih hemijskih adsorpcionih svojstava ili mehanizama. Ova studija može pružiti vrijednu referencu za izradu uređaja za pročišćavanje prilagođenog korisniku koji je pogodniji za kliničke primjene pročišćavanja krvi kod pacijenata na dijalizi.
Ključne riječi
Pročišćavanje krvi, Nadomjesna terapija bubrega, Projektirani biomaterijali, Adsorbens, Polimerna kompozitna membrana.

Kliknite ovdje da saznate šta je Cistanche
Uvod
Uremični toksini se često akumuliraju kod pacijenata sa kompromitovanom funkcijom bubrega, uključujući i one sa završnom stadijumom bubrežne bolesti (ESKD). To dovodi do ozbiljne bolesti, pri čemu su terapije zamjene bubrega jedino rješenje za preživljavanje. Mnoge studije su otkrile smanjenu smrtnost i izvještaje o boljem kvalitetu života među primaocima bubrega; međutim, potražnja nadmašuje dostupnost, gdje samo 25 posto pacijenata sa ESKD dobije bubreg [1]. U svijetu se procjenjuje da se oko 280 pacijenata na milion podvrgava redovnoj hemodijalizi ili peritonealnoj dijalizi, dok je petogodišnje preživljavanje ovih ljudi između 13 i 60 posto niže od osoba u općoj populaciji slične dobi [1–3] . Zbog starenja stanovništva, kao i povećane prevalencije dijabetesa i hipertenzije, očekuje se da će incidencija ESKD rasti u narednim decenijama [4]. Štaviše, akumulacija uremijske retencione otopine u visokim koncentracijama povezana je sa štetnim ishodima kod pacijenata na dijalizi, uključujući visok mortalitet i nisku ukupnu kvalitetu života u vezi sa zdravljem [5–8].

Kreatinin je glavni uremijski toksin, a njegovo skupljanje u krvi uzrokuje niz toksičnih simptoma koji mogu smanjiti funkciju bubrega i posljedično ubrzati opadanje bubrega [9]. Uremijski toksini vezani za proteine (PBUT) su male molekule koje se primarno vezuju za transportni protein, humani serumski albumin u krvi [10], i uključeni su u stvaranje reaktivnih vrsta kisika (ROS) [11]. Iako je posebno poznato da su PBUT-ovi povezani sa štetnim/toksičnim efektima, uključujući kardiovaskularne bolesti [12-14], progresiju zatajenja bubrega [15] i smrtnost [5], njihovi mehanizmi bubrežnog klirensa i uloge u uremskoj patofiziologiji ostaju nejasni [16 ]. Često, p-krezil sulfat (PCS), indoksil sulfat (IS), 3- karboksi-4-metil-5-propil-2-furanpropionska kiselina (CMPF) i indol{{14 }}octena kiselina (IAA) su najodlučniji biomarkeri uremije i smatraju se prototipom uremičnih toksina vezanih za proteine koji mogu vezati više od 90 posto proteina plazme. Sva četiri ova PBUT-a imaju aromatični prsten i ionsku funkcionalnu grupu i mogu formirati nekovalentne veze, kao što su Van der Waalsove sile i vodonične veze, kao i elektrostatičke i hidrofobne interakcije [16]. Kod PBUT-a postoji ravnoteža između oblika vezanih za proteine i nevezanih oblika u njihovom izlučivanju i cirkulaciji, a inherentni klirens nevezanih toksina u velikoj mjeri ovisi o bubrežnoj tubularnoj sekreciji putem specifičnih bazolateralnih transportera organskih aniona (OAT). Put proizvodnje i klirensa proteinskih PBUT-ova prikazan je na slici 1 [16]. Uremička toksičnost je povezana s disfunkcijom endotela i imunološkom disfunkcijom, što uzrokuje upalu i aktivaciju urođenih imunoloških efektora kroz indukciju proinflamatornog stanja koje uključuje Toll-like receptore i inflamatorne citokine [14]. Dakle, dovoljno uklanjanje ovih toksina iz krvi povećava efikasnost dijalize, što zauzvrat povećava stopu preživljavanja kod pacijenata sa ESKD. Osnovni mehanizam hemodijalize prikazan je na slici 2. Međutim, eliminacija viška metabolita upotrebom konvencionalnih ekstrakorporalnih terapija zamjene bubrega putem polupropusnih poroznih polimernih membrana trenutno nije efikasna u kliničkoj upotrebi. Posebno je teško ukloniti PBUT hemodijalizom jer svaki od ovih molekula posjeduje aromatični dio i ionsku funkcionalnu grupu koja omogućava vezivanje za nekoliko adsorpcionih mjesta na albuminu u ljudskom serumu [17–20]. Prijavljeno je da se manje od 35 posto redukcije PCS i IS eliminiše tokom hemodijalize visokog protoka [11].

S obzirom na hemodijalizu kao ekstrakorporalni tretman za održavanje života za zatajenje bubrega, gdje je velikom broju pacijenata sa ESKD potrebna dugotrajna dijaliza, potrebno je pripremiti materijale jednostavnim i jeftinim metodama proizvodnje. Iako su se efikasnost i selektivnost dijaliznih membrana poboljšala posljednjih decenija, tradicionalni tretman dijalizom ostaje nezgodan, dugotrajan i skup proces [21-23]. Nedavno je razvijeno nekoliko biomedicinskih materijala za pročišćavanje krvi kako bi se povećala brzina uklanjanja toksina, od kojih neki također posjeduju karakteristike poput manje toksičnosti i niske cijene proizvodnje. U ovom članku sumiramo ove rezultate po kategorijama kako bismo ponudili informacije za daljnja istraživanja o materijalima za dijalizu s poboljšanim svojstvima.

Cistanche tubulosa
Biomedicinski materijali za uklanjanje toksina-Adsorbenti
Aktivni ugljen (AC) i zeolit su dva uobičajena adsorbenta koji se koriste u prečišćavanju za povećanje ultrafiltracijskih svojstava. AC ima dugu evidenciju u sistemima za detoksikaciju kao adsorpciona čestica jer može adsorbovati širok spektar rastvorenih materija [24-26]. Posjeduje veliku veličinu pora, ali nije selektivan na veličinu. AC pokazuje visok kapacitet adsorpcije za uremičke toksine, ali istovremeno uklanja i druge korisne molekule. Smanjenje promjera čestice je izvediv način da se poveća vanjska površina i time poveća dostupna aktivna mjesta i brzo vezivanje. Međutim, primjena suspenzija s aktivnim ugljenom u prahu zahtijeva membranski filter kako bi sorbente držao suspendiranim i spriječio svaki kontakt čestica s krvlju, što obično ograničava količinu volumena sorbenta i neizbježno rezultira nižim koncentracijama sorbenata [27]. U poređenju sa AC, ugljenične nanocevi (CNT) poseduju veću površinu, veći odnos širine i visine i bolje performanse adsorpcije za uremične toksine, te se stoga smatraju prikladnijim materijalom za dizajn visoko efikasne membrane za pročišćavanje krvi [28–30] . Liu et al. proizvedene kuglice poroznog ugljičnog adsorbenta (NPCA) koje sadrže dušik, koje su imale dodatne prednosti u smislu sigurnog i efikasnog uklanjanja PBUT-a, i imale su zadovoljavajuću in vitro hemokompatibilnost. NPCA je pripremljen pirolizacijom umreženih poroznih zrna akrilonitrila/divinilbenzena kopolimera (slika 3a) [31]. NPCA perle su pokazale veće stope adsorpcije PBUT-a (IS, PCS i IAA; 45 posto, 44 posto i 95 posto) i ekvivalentne performanse adsorpcije prema toksinima srednje molekularne težine (PTH i IL-6) u ljudskoj plazmi u poređenju sa HA- 130/MG-150 (komercijalni adsorbent koji se koristi u klinici). Mehanizam uklanjanja PBUT-a iz NPCA pripisuje se konkurenciji između azotnih funkcionalnih grupa na NPCA i proteina za vezivanje PBUT-a putem elektrostatičkih interakcija, i nema jaku vezu sa strukturom pora (slika 3b) [31].

Za razliku od amorfnog AC, kristalni adsorbenti mogu omogućiti direktnu strukturnu karakterizaciju koja može pomoći u razumijevanju interakcija između adsorbenta i toksina, što je kritično za dizajn superiornih adsorbentskih materijala. Zeolit je jedan od najboljih alum inosilikata koji se primjenjuje za brojna molekularna sita i posjeduje visoku otpornost u kemijskim i termičkim procesima [32]. Zeoliti su netoksični, stabilni u vodenom rastvoru i ne razgrađuju se u fiziološkim uslovima. Štaviše, različite vrste mikroporoznog zeolita imaju sisteme kanala različitih veličina koji mogu selektivno adsorbirati neke uremične toksine [33–36], a mogu se naći prirodno ili proizvedeni sintetički. Ove karakteristike čine zeolite potencijalnim materijalom za primjenu umjetnih bubrega. Veličina i oblik čestica zeolita su važni za sposobnost uzimanja kreatinina kada su ugrađene unutar membrane [37, 38]. Na primjer, mikročestice imaju bolje performanse u adsorpciji kreatinina od nanočestica. U međuvremenu, u poređenju sa nanočesticama štapića, sferične nanočestice su bolji izbor za ugradnju u elektrospinirajuća polimerna vlakna za poboljšanje brzine klirensa kreatinina [37].

Cistanche dodatak
Wernet et al. istraživao eliminaciju uremičnih toksina pomoću zeolita različitih strukturnih tipova [33]. Zaključili su da svojstva adsorpcije zeolita ne zavise samo od veličine kanala, već i od interakcije između adsorbata i rešetki zeolita. Preciznije, zeolit silikalit (MFI) pokazuje snažnu adsorpciju p-krezola (oko 60 posto p-krezola u rastvoru sa koncentracijama bliskim onima koje se nalaze kod pacijenata sa uremijom), što se pripisuje efektu otvaranja kanala/veličine i interakcijama vodonične veze. Mehanizmi adsorpcije prikazani su na slici 4 (npr. adsorpcija p-krezola na silikalit zeolit) [39]. MFI ima kraće vrijeme ekvilibracije i viši nivo adsorpcije p-krezola od membrana na bazi celuloze i sintetičkih membrana [39]. Osim toga, moguće je selektivno eliminirati 75 posto kreatinina u otopini pomoću kiselog mordenita (MOR), što je u osnovi posljedica elektrostatičkih interakcija između Ofunkcionalne grupe i Brønstedtovih mjesta prisutnih u MOR porama [33]. Visoka adsorpcija mokraćne kiseline na stilbitima koji se izmjenjuju jonom (STI), kao što su Ca-STI, K-STI i Na-STI, može se pripisati elektrostatičkoj interakciji između kationa i negativnog atoma polarne molekularne veze. Međutim, postoji potencijalni način da se povećaju svojstva adsorpcije STI kroz formiranje jakih kovalentnih interakcija korištenjem kationa sa afinitetom za uremične toksine [33]. Bergé-Lefranc i dr. dalje je pokazao da čisti silicijum MFI ima bolji kapacitet za uklanjanje p-krezola od aluminosilikatnih MFI (Si/Al=30, kompenzujući naboje sa H plus , Na plus , K plus i Mg2 plus ) [34]. Otkrili su da su u poređenju sa rastvorom, afiniteti p-krezola prema zeolitima generalno smanjeni u ljudskom serumu (dobijenom od pacijenata na dijalizi) jer proteini opstruiraju sistem pora. Dakle, zeoliti se mogu koristiti samo u ultrafiltratu bez direktnog kontakta sa serumskim albuminom [35].

Metal-organski okvir (MOF) je jedna vrsta novog hibridnog materijala, koji ima visoku termičku i hemijsku stabilnost i koji se pokazao efikasnijim od AC ili mezoporoznih silicijumskih materijala, zbog svoje ultravisoke poroznosti i aktivnih mesta [40–42] . A BET površina i unutrašnji prečnik MOF kaveza su prethodno pretpostavljeni kao ključni parametri u adsorpcionom kapacitetu MOF [43]. MOF je napravljen od metalnih jona i organskih linkera preko koordinatnih granica kako bi se formirala 1D, 2D ili 3D struktura [40, 44]. MOF-ovi su brzo stekli popularnost u aplikacijama za, ali nisu ograničeni na, odvajanje bioaktivnih spojeva [45], prečišćavanje vode [46, 47], isporuku lijekova [48] i odvajanje plina [49]. Ipak, upotreba MOF-a u primjenama umjetnih bubrega je još uvijek u ranoj fazi. Nadalje, MOF-ovi posjeduju izuzetnu izdržljivost i, za razliku od drugih klasa kristalnih materijala, mogu se sistematski proučavati i uključiti u mnoštvo funkcionalnosti [50].

Ekstrakt Cistacnhe
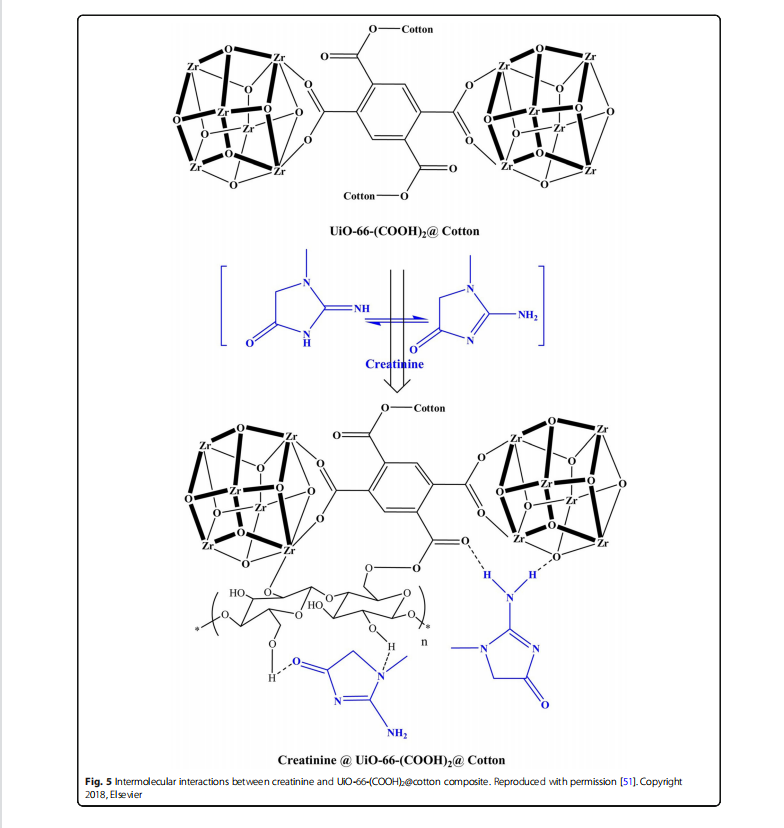
Abdelhameed et al. izvještava o jednoj vrsti MOF-a na bazi Zr-a koji je uzgojen u kompozitu pamučne tkanine, koji se može regenerirati ultrazvukom korištenjem metanola, dok se njegova efikasnost u uklanjanju kreatinina smanjuje samo za 16 posto (98 posto naspram 82 posto) nakon tri ciklusa proizvodnje [ 51]. Ovaj in situ kompozit je direktno formatiran bez proizvodnje UiO-66-(COOH)2 i umjesto toga je korišten 1,2,4,5- benzen tetrakarboksilni dianhidrid, cirkonij tetrahlorid i pamučna tkanina [51]. Kompozit UiO-66- (COOH)2@pamučne tkanine adsorbuje kreatinin kroz slabe interakcije između mesta vezivanja MOF-a i funkcionalnih grupa kreatinina. Mehanizam reakcije je prikazan na slici 5. Osim toga, objavljeno je da je funkcionalizacija UiO-66 sa izovalentnim supstituentima kao što su -NH2, -OH i SO2H značajno poboljšala kapacitet adsorpcije promjenom elektronskih svojstava MOF-a [52 , 53]. Klaudia i dr. sintetizirao niz UiO-66 materijala koji variraju sa konačnim sadržajem amino grupa promjenom H2BDC/H2BDC-NH2 omjera i dodavanjem hlorovodonične kiseline (HCl) tokom modulirane sinteze [52]. Oni su potvrdili da UiO-66-NH2(75 posto ) (sa 75 mol posto -amino grupa) i UiO-66-NH2 (75 posto )12,5 posto HCl imaju bolji kapacitet adsorpcije hipurinske kiseline i {{39} }indoloctene kiseline, otkrivajući analogni kapacitet adsorpcije za NU-1000, dok pripremljeni UiO-66-NH2 još nije pokazao nikakav citotoksični efekat.
Kato et al. uočio ponašanje adsorpcije krezil sulfata u seriji MOF-ova baziranih na Zr6- sa različitom topologijom, konektivnošću i strukturom linkera, uključujući UiO-66, UiO-67, UiO-NDC, PCN{ {4}}OH, NU-901, NU-1000, NU-1010, NU-1200 i MOF-808 [50]. Ovi MOF-ovi na bazi cirkonija posjeduju uporedive površine i veličine pora. Među njima, NU-1000 pokazuje najveću efikasnost uklanjanja toksina, gdje više od 70 posto p-krezil sulfata, 98 posto indoksil sulfata i hipurinske kiseline u otopini, kao i oko 93 posto p-krezil sulfata , može se ukloniti iz humanog serumskog albumina. Ovo se može pripisati visoko hidrofobnim adsorpcijskim mjestima koja su u sendviču sa dva piren linkera, kao i vodikovom vezom između hidroksilnih grupa na Zr6 čvorovima i ionskih funkcionalnih grupa adsorbata [50]. Dvije lokacije p-krezil sulfata na NU-1000 su prikazane na slici 6. Ove dvije lokacije imaju približno istu popunjenost, gdje elektrostatičke interakcije sa hidroksilnim grupama na Zr6 čvorovima i π-π interakcije sa linkerima na bazi pirena su važni faktori u sposobnosti adsorpcije. Međutim, Cuchiaro et al. istakao je da je primjena NU-1000 ograničena jer je komercijalno nedostupan, a željezo je poželjna alternativa cirkonijumu [43]. Cuchiaro et al. sintetizirani MIL-100(Fe) i MOF-808, oba imaju isti organski linker sa MOF-808, ali je MIL-100 (Fe) manje toksičan zbog svog željeza metalni čvorovi na bazi [43]. Otkrili su da je unos p-krezil sulfata za MIL-100(Fe) bio tri puta veći od onog za MOF-808, što je manje povezano sa BET površinom, veličinom prozora pora, prečnikom kaveza i brojem aromatični ugljici u organskom linkeru, što ukazuje da se interakcije metal-gvožđe mogu dešavati povoljnije u MIL-100(Fe) nego MOF-808.

Inspirisani sposobnošću samopročišćavanja bubrega, Chen i sar. predložio je novi adsorbens nazvan molekularno utisnute polimerne inverzne opal čestice (MIPIOPs) [54]. Ovdje se fluidno okruženje koristi za rješavanje dileme nedovoljnog kontakta između adsorbirajućih materijala i ciljnih molekula. MIPIOP-i su ugrađeni u mikrofluidni čip sa mešačem riblje kosti i vaga se može lako pojačati kako bi se prihvatio veliki broj MIPIOP-a za pročišćavanje. Štaviše, kanali riblje kosti mogu generisati haotičnu advekciju tečnosti, i stoga poboljšati efikasnost mešanja i adsorpcije između ciljnih biomolekula i MIPIOP. MIPIOP-i se proizvode kombinovanim procesom otiskivanja (slika 7). Koloidne kristalne kuglice silicijum dioksida (SCCB) su prvo bile proizvedene, a zatim su nanočestice silicijum dioksida na površini SCCB adsorbovale lizozim putem elektrostatičke interakcije. Sljedeći korak popunio je praznine između nanočestica silicijum dioksida SCCB funkcionaliziranih lizozimom koristeći prequel mješavinu metakrilatnog želatina (GelMA), polietilen glikol diakrilata (PEGDA), uree i kreatinina. Zatim su SCCB i molekuli otiska, uključujući lizozim, ureu i kreatinin, uklonjeni iz pre-gel polimera. Rezultirajući MIPIOP posjeduju višestruka molekularna vezna mjesta za lizozim na površini, dok se urea i kreatinin nalaze u unutrašnjosti. MIPIOP-i imaju jedinstvene karakteristike i pokazuju dobru kompatibilnost s krvlju, a pokazano je da se njihov kapacitet adsorpcije održava stabilno nakon petostruke ponovne upotrebe [54]. Štaviše, zbog visoko uređenih 3D poroznih struktura, daju im se svojstva fotonskog pojasa koji omogućavaju praćenje i samoizvještavanje o stanju adsorpcije.

Ciklodekstrini (CD) su ciklički oligosaharidi toroidnog oblika sastavljeni od 6-8 D-glukoznih jedinica ( , , ), sa hidrofilnom spoljašnjošću i relativno hidrofobnom unutrašnjom šupljinom, koja može inkapsulirati različite lipofilne goste niske molekularne težine ili makroelekule [555 , 56]. -CD u obliku čaše se sastoji od 7 jedinica glukoze i najčešće se primjenjuje zbog svog osjetljivog prepoznavanja različitih hidrofobnih molekula formiranjem kompleksa CD-gost. Li et al. je po prvi put predložio dodavanje umreženih poli- -ciklodekstrina (PCD) u dijalizat vanjskog dijalizatora za poboljšanje efikasnosti prijenosa mase indoksil sulfata (IS) (slika 8a) [56]. PCD je sintetiziran unakrsnom vezom između -CD i epiklorohidrina (ECH). -CD je prvo rastvoren u rastvoru NaOH, a zatim je u smešu dodat ECH, koja je zatim mešana na 30 stepeni 2 h. Prema originalnoj studiji, maksimalni kapacitet vezivanja PCD-a za IS je oko 45 mg g-1 i povećanje brzine uklanjanja od 21 posto je postignuto u eksperimentu simulacije dijalize sa uvođenjem PCD-a. Mehanizam vezivanja IS za PCD može biti da se indolni prsten IS smjesti u šupljinu -CD kroz hidrofobnu interakciju i vodoničnu vezu [56]. Ova nova strategija nema negativan utjecaj na membranu za dijalizu i sigurna je za kliničku primjenu jer je dokazano da je PCD niska stopa hemolize i ne može proći kroz membranu do kontakta s krvlju (hidrodinamički promjer polimera je 9 nm). Li et al. dalje je uporedio kapacitet adsorpcije poli- -ciklodekstrina, poli- - ciklodekstrina i poli- -ciklodekstrina i poli{27}} ciklodekstrina koji je bio najbolji sa maksimalnim kapacitetom vezivanja krezol sulfata (PCS) (263 mg g-1) [57]. Otkrili su da je čišćenje PCS u plazmi kroz jednokratni način rada (slika 8b) efikasnije od recikliranog načina (96 posto naspram 43 posto), što se pripisuje razlici u koncentraciji PCS između plazme i dijalizata koja se povećava s uklanjanjem PCS. A PCS (96 posto), hipurinska kiselina (98 posto) i kinolinska kiselina (97 posto) u plazmi su uklonjeni u PCD dodatkom dijalizatnom sistemu, dodatno razjašnjavajući svojstva uklanjanja PBUT širokog spektra PCD-a [57].

MXeni su porodica dvodimenzionalnih karbida i nitrida prelaznih metala sa opštom strukturom Mn plus 1XnTx (M je rani prelazni metal, kao što su Ti, V, Nb, itd.; n plus 1=1-3; X je C i/ili N; Tx predstavlja površinske završetke, kao što su O, OH, F i/ili Cl) [58, 59]. MXeni imaju jedinstvenu kombinaciju svojstava, uključujući hidrofilne zbog funkcionaliziranih površina i stabilnih koloidnih otopina u vodi zbog visokog negativnog zeta potencijala, i opsežno su istraženi u biomedicinskom polju posljednjih godina [58]. Ti3C2Tx je prvi prijavljeni i najviše proučavani član MXenes-a i poznato je da efikasno adsorbuje ureu. I za Ti3C2Tx je snažno pokazano da ima relativno visoku biokompatibilnost i nisku biotoksičnost u prethodnim in vivo studijama [60]. U radu Zhao et al., Ti3C2Tx (Ti3C2- F, Ti3C2-O, Ti3C2-OH, proizveden od prekursora Ti3AlC2 korištenjem 10 tež% fluorovodične kiseline) je korišten kao adsorbens u vodenom rastvoru, a vršio je brzu brzinu adsorpcije i veći kapacitet adsorpcije prema kreatininu i mokraćnoj kiselini u poređenju sa konvencionalnim aktivnim ugljem [59]. Visok afinitet između Ti3C2Tx i kreatinina u procesu adsorpcije pripisuje se hidrofilnim površinskim završecima Ti3C2Tx i intračestičnoj difuziji kreatinina između sloja Ti3C2Tx. U procesu adsorpcije mokraćne kiseline, međutim, visoki afinitet može proizaći iz vodonične veze (TiOH…N) i van der Waalsovih interakcija. Štaviše, s obzirom da Ti3C2Tx efikasno adsorbuje ureu, kreatin i mokraćnu kiselinu, kao i katjoni elektrolita (K plus, Ca2 plus, Mg2 plus, itd.) takođe mogu zauzeti aktivna mesta Ti3C2Tx, Zhao et al. je predložio da Ti3C2Tx ima potencijal da se koristi kao efikasan sorbent za regeneraciju dijalizata. U novije vrijeme, Wang et al. pripremio Ti3C2Tx nanolist razdvajanjem ugravljenog Ti3C2Tx u deaeriranoj vodi ultrazvukom i po prvi put otkrio da je ultravisoka sposobnost uklanjanja Ti3C2Tx prema IL-6, što je pokazalo 13,4 puta od tradicionalnog aktivnog ugljena i mnogo bržu brzinu uklanjanja [ 61]. Glavni mehanizam za adsorpciju je formiranje vodonične veze između MXene i IL-6 (TI-X … HNC=O), kao i imobilizacija IL-6 na površini MXene nanosheets.

Cistanche kapsule
Zaključak
U zaključku, saželi smo novi biomaterijal za pročišćavanje krvi koji je objavljen posljednjih godina. Ovi biomaterijali su grubo podijeljeni u 3 kategorije, uključujući adsorbente, polimerne kompozitne membrane i nanomaterijale. Adsorbenti, kao što su zeoliti, aktivni ugljen i CTN, obično su ugrađeni u polimerne materijale kako bi se poboljšao kapacitet ultrafiltracije. Kada su adsorpcijske čestice dispergirane po polimernoj matrici, efikasnost uklanjanja uremičnih toksina može se značajno poboljšati kombinacijom adsorpcije i difuzije uremičnih retencijskih otopljenih tvari, što je potvrđeno u studijama vezanim za MMM i f-CNT/PES kompozitne membrane. Zbog velike površine i poroznosti, i nanomaterijali i MOF-i pokazuju povoljne sposobnosti adsorpcije. Osim toga, proizvodnja polimernih nanovlakna je isplativa, a MOF-ovi na bazi Zr imaju dobru mogućnost ponovne upotrebe.
Permeacija je vitalno svojstvo membrane koja se koristi za hemodijafiltraciju, jer niska brzina uklanjanja toksina uzrokuje da pacijenti pate kroz duge periode dijalize s većim troškovima. Kada se koncentracija slobodnog toksina na strani dijalizata održava na niskim razinama, postoji kontinuirana pokretačka sila difuzije po cijeloj dužini hemodijalizatora, posebno za PBUT [130, 131]. Kao što je spomenuto u ovom radu, materijali velike površine i poroznosti su obećavajući kandidati za proizvodnju membrana za hemodijalizu. Ugrađivanje adsorptivnih čestica u matricu polimerne membrane je također efikasna metoda za postizanje efikasnije stope klirensa uremičnih toksina, što je posljedica održavanja razlike u koncentraciji. Postoji i nekoliko adsorbenata čija je sposobnost adsorpcije manje povezana sa strukturom pora, kao što su NPCA perle. Stoga je ključno analizirati odgovarajuću molekularnu strukturu adsorbentskih i uremičkih toksina, kao i interakciju unutar njih.
Dijaliza je dugotrajan tretman koji održava život za pacijente s ESKD, a potrebno je skoro 500 L vode iz slavine za dobivanje čiste vode za dijalizu za jednu sesiju hemodijalize, koja je visoka i po cijeni i po potrošnji energije [132]. Stoga je jednostavan i jeftin način proizvodnje materijala za dijalizu od velikog značaja za njegovu kliničku primjenu. Osim toga, mikrobiološki biofilm uzrokovan stagnacijom vode i dalje će se formirati kada je sustav cijevi neadekvatan ili postoji nepravilno održavanje mašine [133, 134]. Rast i liza bakterija u sistemu za pročišćavanje vode, a time i pirogeni mogu se prenijeti u krv pacijenata, što uzrokuje mikroinflamatorni status, što dovodi do kardiovaskularnih nuspojava ili akutnih nuspojava, poput groznice i mišićnih grčeva [133–139] . Prijavljeno je nekoliko sistema sorbenta za uklanjanje endotoksina (npr. lipopolisaharida), kao što su funkcionalizirane nanočestice [140], aktivni ugljen [26, 141], dodatak PS-poli (etilen glikol) kopolimera (PS-PEG) i izbjeljivač sterilizacija [133]. Dodatno, MMM nudi superiorno uklanjanje endotoksina i djeluje kao sigurnosna barijera koja izbjegava upalne odgovore bez smanjenja uklanjanja uremičnih toksina [71]. Općenito, biomaterijali s dugotrajnom i visokom ultrafiltracijom, povoljnom biokompatibilnošću i isplativim metodama proizvodnje idealni su kandidati za pročišćavanje krvi. Čak i ako su novi biomaterijali spomenuti u ovom pregledu poboljšali kapacitet adsorpcije i biokompatibilnost, još uvijek ima puno posla koji treba obaviti koji se fokusira na modifikaciju materijala kako bi bili pogodni za kliničku primjenu.
Reference
1. Webster AC, Nagler EV, Morton RL, Masson P. Hronična bolest bubrega. Lancet. 2017;389(10075):1238–52.
2. Tonelli M, Wiebe N, Knoll G, Bello A, Browne S, Jadhav D, et al. Sistematski pregled: transplantacija bubrega u poređenju sa dijalizom u klinički relevantnim ishodima. Am J Transplant. 2011;11(10):2093–109.
3. Nordio M, Limido A, Maggiore U, Nichelatti M, Postorino M, Quintaliani G. Preživljavanje pacijenata liječenih dugotrajnom dijalizom u poređenju sa općom populacijom. Am J Kidney Dis. 2012;59(6):819–28.
4. Liyanage T, Ninomiya T, Jha V, Neal B, Patrice HM, Okpechi I, et al. Pristup liječenju završnog stadijuma bolesti bubrega širom svijeta: sistematski pregled. Lancet. 2015;385(9981):1975–82.
5. Bammens B, Evenepoel P, Keuleers H, Verbeke K, Vanrenterghem Y. Slobodne koncentracije u serumu retencionog rastvora p-krezola vezane za proteine predviđaju smrtnost pacijenata na hemodijalizi. Kidney Int. 2006;69(6):1081–7.
6. Cheung AK, Rocco MV, Yan G, Leypoldt JK, Levin NW, Greene T, et al. Nivoi beta{1}} mikroglobulina u serumu predviđaju smrtnost pacijenata na dijalizi: rezultati kućne studije. J Am Soc Nephrol. 2006;17(2):546–55.
7. Ito S, Osaka M, Higuchi Y, Nishijima F, Ishii H, Yoshida M. Indoksil sulfat indukuje interakcije leukocita i endotela kroz regulaciju selekcije naviše. J Biol Chem. 2010;285(50):38869–75.
8. Duranton F, Cohen G, De Smet R, Rodriguez M, Jankowski J, Vanholder R, et al. Normalne i patološke koncentracije uremičnih toksina. J Am Soc Nephrol. 2012;23(7):1258–70.
9. Panasyuk-Delaney T, Mirsky VM, Wolfbeis OS. Kapacitivni senzor kreatinina baziran na fotografisanom molekularno utisnutom polimeru. Elektroanaliza. 2002;14(3):221–4.
10. Vanholder R, De Smet R, Glorieux G, Argiles A, Baurmeister U, Brunet P, et al. Pregled uremičnih toksina: klasifikacija, koncentracija i interindividualna varijabilnost. Kidney Int. 2003;63(5):1934–43.
11. Itoh Y, Ezawa A, Kikuchi K, Tsuruta Y, Niwa T. Uremični toksini vezani za proteine kod pacijenata na hemodijalizi mjereni tečnom hromatografijom/tandemskom masenom spektrometrijom i njihovi efekti na proizvodnju endotelnog ros. Anal Bioanal Chem. 2012;403(7):1841–50.
12. Lin CJ, Pan CF, Liu HL, Chuang CK, Jayakumar T, Wang TJ, et al. Uloga uremijskih toksina vezanih na proteine u bolesti perifernih arterija i neuspjehu vaskularnog pristupa kod pacijenata na hemodijalizi. Ateroskleroza. 2012;225(1):173–9.
13. Wu PH, Lin YT, Chiu YW, Baldanzi G, Huang JC, Liang SS, et al. Odnos indoksil sulfata i p-krezil sulfata sa ciljnim kardiovaskularnim proteinima kod pacijenata na hemodijalizi. Sci Rep. 2021;11(1):3786.
14. Falconi CA, Junho CVDC, Fogaça-Ruiz F, Vernier ICS, Da Cunha RS, Stinghen AEM, et al. Uremični toksini: alarmantna opasnost za kardiovaskularni sistem. Front Physiol. 2021;12:686249.
15. Wu IW, Hsu KH, Lee CC, Sun CY, Hsu HJ, Tsai CJ, et al. P-krezil sulfat i indoksil sulfat predviđaju napredovanje hronične bolesti bubrega. Transplantacija Nephrol Dial. 2011;26(3):938–47.
16. Daneshamouz S, Eduok U, Abdelrasoul A, Shoker A. Uremijski toksini vezani za proteine (PBUTS) kod pacijenata s hroničnom bubrežnom bolešću (CKD): proizvodni put, izazovi i nedavni napredak u renalnom uklanjanju PBUTS-a. NanoImpact. 2021;21:100299.
17. Ghuman J, Zunszain PA, Petitpas I, Bhattacharya AA, Otagiri M, Curry S. Strukturna osnova specifičnosti vezanja lijeka humanog serumskog albumina. J Mol Biol. 2005;353(1):38–52.
18. Brettschneider F, Toelle M, von der Giet M, Passlick-Deetjen J, Steppan S, Peter M, et al. Uklanjanje hidrofobnih uremičnih toksina vezanih za proteine kombiniranom tehnikom odvajanja frakcionirane plazme i adsorpcije. Artif Organs. 2013;37(4):409–16.
19. Berge-Lefranc D, Chaspoul F, Cerini C, Brunet P, Gallice P. Termodinamička studija interakcije indoksil sulfata sa albuminom humanog seruma i kompetitivnog vezivanja sa p-krezil sulfatom. J Therm Anal Calorim. 2014;115(3):2021–6.
20. Yu S, Schuchardt M, Toelle M, van der Giet M, Zidek W, Dzubiella J, et al. Interakcija humanog serumskog albumina s uremičnim toksinima: termodinamička studija. RSC Adv. 2017;7(45):27913–22.
21. Baboolal K, McEwan P, Sondhi S, Spiewanowski P, Wechowski J, Wilson K. Troškovi renalne dijalize u UK okruženju--multicentrična studija. Transplantacija Nephrol Dial. 2008;23(6):1982–9.
22. Harris A, Cooper BA, Li JJ, Bulfone L, Branley P, Collins JF, et al. Isplativost ranog započinjanja dijalize: randomizirano kontrolirano ispitivanje. Am J Kidney Dis. 2011;57(5):707–15.
23. Young BA, Chan C, Blagg C, Lockridge R, Golper T, Finkelstein F, et al. Kako savladati barijere i uspostaviti uspješan kućni HD program. Clin J Am Soc Nephrol. 2012;7(12):2023–32.
24. Dinh DC, Recht NS, Hostetter TH, Meyer TW. Obložena ugljična hemoperfuzija osigurava ograničeni klirens otopljenih tvari vezanih za proteine. Artif Organs. 2008; 32(9):717–24.
25. Ash SR. Sorbenti u liječenju uremije: kratka povijest i velika budućnost. Semin Dial. 2009;22(6):615–22.
26. Gun'Ko VM, Betz WR, Patel S, Murphy MC, Mikhalovski SV. Adsorpcija lipopolisaharida na ugljičnim sitom. Karbon. 2006;44(7):1258–62.
27. Ash SR, Sullivan TA, Carr DJ. Sorbentne suspenzije u odnosu na sorbentne kolone za ekstrakorporalnu detoksikaciju kod zatajenja jetre. Ther Apher Dial. 2006;10(2):145–53.
28. Ye C, Gong Q, Lu F, Liang J. Adsorpcija uremičnih toksina na ugljičnim nanocijevima. Sep Purif Technol. 2007;58(1):2–6.
29. Lu C, Su F. Adsorpcija prirodne organske materije ugljeničnim nanocevima. Sep Purif Technol. 2007;58(1):113–21.
30. Spitalsky Z, Tasis D, Papagelis K, Galiotis C. Ugljenične nanocijevi-polimer kompoziti: hemija, obrada, mehanička i električna svojstva. Prog Polym Sci. 2010;35(3):357–401.
31. Liu Y, Peng X, Hu Z, Yu M, Fu J, Huang Y. Izrada novog poroznog ugljičnog adsorbenta koji sadrži dušik za uklanjanje uremičnih toksina vezanih za proteine. Mater Sci Eng C Mater Biol Appl. 2021;121:111879.
32. Soldatkin OO, Soy E, Errachid A, Jaffrezic-Renault N, Akata B, Soldatkin AP, et al. Utjecaj sastava zeolit/enzim nanobiokompozita na analitičke karakteristike urea biosenzora na bazi ion-selektivnih tranzistora sa efektom polja. Sens Lett. 2011;9(6SI):2320–6.
33. Wernert V, Schäf O, Ghobarkar H, Denoyel R. Adsorpcijska svojstva zeolita za primjenu umjetnih bubrega. Micropor Mesopor Mat. 2005;83(1): 101–13.
34. Bergé-Lefranc D, Pizzala H, Paillaud JL, Schäf O, Vagner C, Boulet P, et al. Adsorpcija malih molekula uremičkog toksina na zeolitima mfi tipa iz vodene otopine. Adsorpcija. 2008;14(2):377–87.
35. Bergé-Lefranc D, Vagner C, Calaf R, Pizzala H, Denoyel R, Brunet P, et al. In vitro eliminacija uremičkog toksina p-krezola vezanog na proteine zeolitima tipa mfi. Micropor Mesopor Mat. 2012;153:288–93.
36. Namekawa K, Tokoro Schreiber M, Aoyagi T, Ebara M. Proizvodnja zeolit-polimer kompozitnih nanovlakna za uklanjanje uremičnih toksina kod pacijenata sa zatajenjem bubrega. Biomater Sci-Uk 2014;2(5):674–9.
37. Lu L, Chen C, Samarasekera C, Yeow JTW. Utjecaj oblika i veličine čestica zeolita na njihovu sposobnost da adsorbiraju uremični toksin u obliku praha i kao punila u membranama. J Biomed Mater Res B Appl Biomater. 2017;105(6):1594–601.
38. Tantekin-Ersolmaz SB, Atalay-Oral C, Tatlier M, Erdem-Senatalar A, Schoeman B, Sterte J. Utjecaj veličine čestica zeolita na performanse polimernih zeolitnih mješovitih matričnih membrana. J Membrane Sci. 2000;175(2):285–8.
39. Wernert V, Schäf O, Faure V, Brunet P, Dou L, Berland Y, et al. Adsorpcija uremičnog toksina p-krezola na membrane za hemodijalizu i mikroporozni adsorbent zeolit silikalit. J Biotechnol. 2006;123(2):164–73.
40. Furukawa H, Cordova KE, O'Keeffe M, Yaghi OM. Hemija i primjena metalo-organskih okvira. Nauka. 2013;341(6149):974.
41. Haque E, Jun JW, Jhung SH. Adsorptivno uklanjanje metil narandže i metilen plavog iz vodenog rastvora metalno-organskim okvirnim materijalom, gvožđe tereftalatom (mof-235). J Hazard Mater. 2011;185(1):507–11.
42. Fletcher AJ, Thomas KM, Rosseinsky MJ. Fleksibilnost metalo-organskih okvirnih materijala: utjecaj na sorpcijska svojstva. J Solid State Chem. 2005;178(8):2491–510.
43. Cuchiaro H, Thai J, Schaffner N, Tuttle RR, Reynolds M. Istraživanje parametarskog prostora adsorpcije p-krezil sulfata u metal-organskim okvirima. ACS Appl Mater interfejsi. 2020;12(20):22572–80.
44. Tan J, Civalleri B. Metalno-organski okviri i hibridni materijali: od osnova do primjene. Crystengcomm. 2015;17(2):197–8.
45. Abdelhameed RM, Abdel-Gawad H, Taha M, Hegazi B. Odvajanje bioaktivnog chamazulena iz ekstrakta kamilice korištenjem metalno-organskog okvira. J Pharmaceut Biomed. 2017;146:126–34.
46. Mon M, Bruno R, Ferrando-Soria J, Armentano D, Pardo E. Metalno-organske okvirne tehnologije za remedijaciju vode: ka održivom ekosistemu. J Mater Chem A. 2018;6(12):4912–47.
47. Abdelhameed RM, Abdel-Gawad H, Elshahat M, Emam HE. Cu–btc@cotton kompozit: dizajn i uklanjanje etionskog insekticida iz vode. RSC Adv. 2016;6(48):42324–33.
48. Huxford RC, Della Rocca J, Lin W. Metalno-organski okviri kao potencijalni nosači lijekova. Curr Opin Chem Biol. 2010;14(2):262–8.
49. Rodenas T, Luz I, Prieto G, Seoane B, Miro H, Corma A, et al. Metalno-organski okvirni nano listovi u polimernim kompozitnim materijalima za odvajanje gasa. Nat Mater. 2015;14(1):48–55.
50. Kato S, Otake K, Chen H, Akpinar I, Buru CT, Islamoglu T, et al. Metalno-organski okviri na bazi cirkonija za uklanjanje uremičnog toksina vezanog na proteine iz humanog serumskog albumina. J Am Chem Soc. 2019;141(6):2568–76.
51. Abdelhameed RM, Rehan M, Emam HE. Figuracija kompozita mof@pamučne tkanine na bazi zr-a za potencijalnu primjenu u bubrezima. Carbohyd Polym. 2018; 195:460–7.
52. Dymek K, Kurowski G, Kuterasinski L, Jedrzejczyk R, Szumera M, Sitarz M, et al. U potrazi za efikasnim auto-66 metal-organskim okvirima za primjenu umjetnih bubrega. ACS Appl Mater Inter. 2021;13(38):45149–60.
53. Zhu J, Wu L, Bu Z, Jie S, Li B. UiO-66-nh2 (zr) metal-organski okviri modificirani polietileniminom: priprema i poboljšana selektivna adsorpcija CO2. ACS Omega. 2019;4(2):3188–97.
54. Chen H, Bian F, Sun L, Zhang D, Shang L, Zhao Y. Hijerarhijski molekularno utisnute porozne čestice za biomimetičko čišćenje bubrega. Adv Mater. 2020; 32(52):2005394.
55. Mejia-Ariza R, Grana-Suarez L, Verboom W, Huskens J. Supramolekularne nanočestice na bazi ciklodekstrina za biomedicinske primjene. J Mater Chem B. 2017;5(1):36–52.
56. Li J, Han L, Liu S, He S, Cao Y, Xie J, et al. Uklanjanje indoksil sulfata policiklodekstrinima rastvorljivim u vodi u dijalizi. Colloid Surface B. 2018;164:406–13.
57. Li J, Han L, Xie J, Liu S, Jia L. Višestruki policiklodekstrinski adsorbenti za uklanjanje uremičnih toksina vezanih za proteine u kombinaciji sa hemodijalizom. Carbohyd Polym. 2020;247:116665.
58. Gogotsi Y, Anasori B. Uspon mxena. ACS Nano. 2019;13(8):8491–4.
59. Zhao Q, Seredych M, Precetti E, Shuck CE, Harhay M, Pang R, et al. Adsorpcija uremičnih toksina korištenjem ti3c2tx men za regeneraciju dijalizata. ACS Nano. 2020;14(9):11787–98.
60. Dai C, Lin H, Xu G, Liu Z, Wu R, Chen Y. Biokompatibilni 2d titanijum karbid (mxenes) kompozitni nanosheetovi za ph-responzivnu MR vođenu hipertermiju tumora. Chem Mater. 2017;29(20):8637–52.
61. Wang T, Sun X, Guo X, Zhang J, Yang J, Tao S, et al. Ultraefikasno smirujuća citokinska oluja koristeći ti (3) c (2) t (x) mxene. Male metode. 2021;5(5): e2001108.
62. Tian H, Tang Z, Zhuang X, Chen X, Jing X. Biorazgradivi sintetički polimeri: priprema, funkcionalizacija i biomedicinska primjena. Prog Polym Sci. 2012;37(2):237–80.
63. Weber V, Linsberger I, Hauner M, Leistner A, Leistner A, Falkenhagen D. Neutralni stiren-divinilbenzen kopolimeri za adsorpciju toksina kod zatajenja jetre. Biomacromolecules. 2008;9(4):1322–8.
64. Jiang X, Xiang T, Xie Y, Wang R, Zhao W, Sun S et al. Funkcionalne polietersulfonske čestice za uklanjanje bilirubina. Časopis za nauku o materijalima: Materijali u medicini 2015;27(2):28.
65. Lu L, Samarasekera C, Yeow JTW. Kapacitet adsorpcije kreatinina elektrospunskih poliakrilonitrilnih (PAN)-zeolitnih membrana od nanovlakna za potencijalnu primjenu na umjetnim bubrezima. J Appl Polym Sci 2015;132(34): 42418- 26.
66. Lu L, Yeow JTW. Studija adsorpcije indoksil sulfata zeolitima i polietersulfon-zeolit kompozitnim membranama. Mater Design. 2017;120: 328–35.
67. Tijink MS, Wester M, Sun J, Saris A, Bolhuis-Versteeg LA, Saiful S, et al. Novi pristup za pročišćavanje krvi: membrane s miješanim matriksom koje kombiniraju difuziju i adsorpciju u jednom koraku. Acta Biomater. 2012;8(6):2279–87.
68. Tijink MSL, Wester M, Glorieux G, Gerritsen KGF, Sun J, Swart PC, et al. Mješovite matrične membrane od šupljih vlakana za uklanjanje toksina vezanih za proteine iz ljudske plazme. Biomaterijali. 2013;34(32):7819–28.
69. Pavlenko D, van Geffen E, van Steenbergen MJ, Glorieux G, Vanholder R, Gerritsen KGF et al. Nove mješovite matriksne membrane niskog protoka nude vrhunsko uklanjanje toksina vezanih za proteine iz ljudske plazme. Sci Rep 2016;6:34429.
70. Geremia I, Pavlenko D, Maksymow K, Rueth M, Lemke HD, Stamatialis D. Ex vivo evaluacija kompatibilnosti krvi membrana za hemodijalizu mješovitog matriksa. Acta Biomater. 2020;111:118–28.
71. Geremia I, Bansal R, Stamatialis D. In vitro procjena mješovite matriksne membrane za hemodijalizu za postizanje dijalizata bez endotoksina u kombinaciji sa visokim uklanjanjem uremičnih toksina iz ljudske plazme. Acta Biomater. 2019;90:100–11.
72. Nie C, Ma L, Xia Y, He C, Deng J, Wang L, et al. Nove kompozitne membrane od ugljičnih nanocijev/pes polimera koje oponašaju heparin za sigurno i efikasno pročišćavanje krvi. J Membrane Sci. 2015;475:455–68.
73. Zhang Y, Lim CT, Ramakrishna S, Huang Z. Nedavni razvoj polimernih nanovlakna za biomedicinske i biotehnološke primjene. J Mater Sci Mater Med. 2005;16(10):933–46.
74. Ramakrishna S, Fujihara K, Teo W, Yong T, Ma Z, Ramaseshan R. Elektrospun nanovlakna: rješavanje globalnih problema. Mater Today. 2006;9(3):40–50.
75. Huang Z, Zhang YZ, Kotaki M, Ramakrishna S. Pregled polimernih nanovlakna elektropredenja i njihove primjene u nanokompozitima. Compos Sci Technol. 2003;63(15):2223–53.
76. Fu GD, Xu LQ, Yao F, Zhang K, Wang XF, Zhu MF, et al. Pametna nanovlakna iz kombinovane žive radikalne polimerizacije, "klik hemije" i elektropredenja. ACS Appl Mater Inter. 2009;1(2):239–43.
77. Kim Y, Ebara M, Aoyagi T. Pametna mreža od nanovlakna koja hvata i oslobađa ćelije. Angew Chem Int Ed. 2012;51(42):10537–41.
78. Wang XY, Drew C, Lee SH, Senecal KJ, Kumar J, Samuelson LA. Electrospinning tehnologija: novi pristup primjeni senzora. J Macromol Sci Pure Appl Chem. 2002; A39(10):1251–8.
79. Barhoum A, Pal K, Rahier H, Uludag H, Kim IS, Bechelany M. Nanovlakna kao materijali nove generacije: od tehnika predenja i nano-predenja do novih aplikacija. Appl Mater danas. 2019;17:1–35.
80. Peh P, Lim NSJ, Blocki A, Chee SML, Park HC, Liao S, et al. Istovremena isporuka veoma raznovrsnih bioaktivnih jedinjenja iz mešavine elektropredenih vlakana za zarastanje kožnih rana. Bioconjugate Chem. 2015;26(7):1348–58.
81. Qi R, Guo R, Shen M, Cao X, Zhang L, Xu J, et al. Elektrospun poli (mliječna-ko-glikolna kiselina)/haloazit nanocijevi kompozitna nanovlakna za inkapsulaciju lijeka i produženo oslobađanje. J Mater Chem. 2010;20(47):10622–9.
82. Salalha W, Kuhn J, Dror Y, Zussman E. Enkapsulacija bakterija i virusa u elektrospun nanovlakna. Nanotehnologija. 2006;17(18):4675–81.
83. Luo Y, Nartker S, Miller H, Hochhalter D, Wiederoder M, Wiederoder S, et al. Površinska funkcionalizacija elektrospunskih nanovlakna za detekciju e. Coli o157:h7 i tjelesne ćelije u biosenzoru za prijenos direktnog naboja. Biosens Bioelectron. 2010;26(4):1612–7.
84. Esmaeili A, Haseli M. Elektropredenje nanovlakna termoplastične karboksimetil celuloze/poli (etilen oksida) za upotrebu u sistemima za oslobađanje lijekova. Mat Sci Eng C-Mater. 2017;77:1117–27.
85. Han D, Steckl AJ. Triaksijalne elektrospunirane membrane od nanovlakna za kontrolirano dvostruko oslobađanje funkcionalnih molekula. ACS Appl Mater Inter. 2013;5(16):8241–5.
86. Bahramimehr F, Esmaeili A. Proizvodnja hibridnih nanovlakna na bazi /pan/fe3o4/zeolita/biljnog ekstrakta koprive/ureaze i deformisanog koaksijalnog prirodnog polimera za smanjenje toksičnosti materijala u krvi pacijenata na dijalizi. J Biomed Mater Res A. 2019;107(8):1736–43.
87. Irfan M, Idris A, Yusof NM, Khairuddin NFM, Akhmal H. Modifikacija površine i poboljšanje performansi nano-hibridnih f-mwcnt/pvp90/pes membrana za hemodijalizu. J Membrane Sci. 2014;467:73–84.
88. Niyogi S, Hamon MA, Hu H, Zhao B, Bhowmik P, Sen R, et al. Hemija jednozidnih ugljičnih nanocijevi. Računi Chem Res. 2002;35(12):1105–13.
89. Raravikar NR, Schadler LS, Vijayaraghavan A, Zhao Y, Wei B, Ajayan PM. Sinteza i karakterizacija kompozitnih filmova ugljikovih nanocijev-polimer usklađenih po debljini. Chem Mater. 2005;17(5):974–83.
90. Valcárcel M, Cárdenas S, Simonet BM, Moliner-Martínez Y, Lucena R. Ugljične nanostrukture kao sorbentni materijali u analitičkim procesima. TrAC Trends Analyt Chem. 2008;27(1):34–43.
91. Tsuge M, Takahashi K, Kurimoto R, Fulati A, Uto K, Kikuchi A, et al. Izrada mreža od nanovlakna koje upijaju vodu za efikasno uklanjanje viška vode kod pacijenata sa zatajenjem bubrega. Vlakna. 2019;7(5):39.
92. Khan I, Saeed K, Khan I. Nanočestice: svojstva, primjena i toksičnost. Arab J Chem. 2019;12(7):908–31.
93. Wang L, Zhang Y, Li Y, Chen J, Lin W. Nedavni napredak u projektovanim nanomaterijalima za teranostiku akutne povrede bubrega. Nano Res. 2021;14(4):920–33.
94. Stamopoulos D, Bouziotis P, Benaki D, Kotsovassilis C, Zirogiannis PN. Upotreba nanobiotehnologije u hemodijalizi: lažni eksperimenti dijalize na homocisteinu. Transplantacija Nephrol Dial. 2008;23(10):3234–9.
95. Ma Y, Cai F, Li Y, Chen J, Han F, Lin W. Pregled primjene nanočestica u dijagnostici i liječenju hronične bolesti bubrega. Bioact Mater. 2020;5(3):732–43.
96. Cheah W, Ishikawa K, Othman R, Yeoh F. Nanoporozni biomaterijali za adsorpciju uremičkog toksina u sistemima umjetnih bubrega: pregled. J Biomed Mater Res B Appl Biomater. 2017;105(5):1232–40.
97. Abidin MNZ, Goh PS, Ismail AF, Said N, Othman MHD, Hasbullah H, et al. Visoko adsorptivne oksidirane nanočestice škroba za efikasno uklanjanje uree. Carbohyd Polym. 2018;201:257–63.
98. Cabello-Alvarado C, Andrade-Guel M, Pérez-Alvarez M, Cadenas-Pliego G, Cortés-Hernández DA, Bartolo-Pérez P, et al. Grafenske nanopločice modificirane amino grupama ultrazvučnim zračenjem promjenjive frekvencije za potencijalnu adsorpciju uremičnih toksina. NanomaterijaliBasel. 2019;9(9):1261.
99. Andrade-Guel M, Ávila-Orta CA, Cadenas-Pliego G, Cabello-Alvarado CJ, Pérez-Alvarez M, Reyes-Rodríguez P, et al. Sinteza nanokompozita najlon 6/modificirane čađe za primjenu u adsorpciji mokraćne kiseline. Materijali. 2020;13(22):5173.
100. Korsvik C, Patil S, Seal S, Self WT. Superoksid dismutaza oponašaju svojstva nanočestica cerije. Chem Commun. 2007; 10:1056–8.
101. Pirmohamed T, Dowding JM, Singh S, Wasserman B, Heckert E, Karakoti AS, et al. Nanocerije pokazuju mimetičku aktivnost katalaze ovisno o redoks stanju. Chem Commun. 2010;46(16):2736–8.
102. Xue Y, Luan Q, Yang D, Yao X, Zhou K. Direktni dokazi za aktivnost uklanjanja hidroksilnih radikala nanočestica cerijum oksida. J Phys Chem C. 2011; 115(11):4433–8.
103. Ni D, Wei H, Chen W, Bao Q, Rosenkrans ZT, Barnhart TE, et al. Nanočestice ceria susreću se sa ishemijom i reperfuzijom jetre: savršena nesavršenost. Adv Mater. 2019;31(40):1902956.
104. Fleming RE, Ponka P. Preopterećenje gvožđem kod ljudskih bolesti. New Engl J Med. 2012;366(4):348–59.
105. Hamilton JL, Kizhakkedathu JN. Polimerni nanonosači za tretman sistemskog preopterećenja gvožđem. Mol Cell Ther. 2015;3:3.
106. Kang H, Han M, Xue J, Baek Y, Chang J, Hu S et al. Nano kelatori koji se mogu očistiti putem bubrega za terapiju preopterećenja gvožđem. Nat Commun 2019;10(1):5134.
107. Mobarra N, Shanaki M, Ehteram H, Nasiri H, Sahmani M, Saeidi M, et al. Pregled kelatora željeza u liječenju sindroma preopterećenja željezom. Int J Hematol Oncol Stem Cell Res. 2016;10(4):239–47.
108. Shapiro SM. Toksičnost bilirubina u nervnom sistemu u razvoju. Pediatr Neurol. 2003;29(5):410–21.
109. Peng Z, Yang Y, Luo J, Nie C, Ma L, Cheng C, et al. Nanofibrozne polimerne kuglice od aramidnih vlakana za efikasno uklanjanje bilirubina. Biomater Sci-Uk. 2016;4(9):1392–401.
110. Yang M, Cao K, Sui L, Qi Y, Zhu J, Waas A, et al. Disperzije aramidnih nanovlakna: novi građevinski blok na nanorazmjeri. ACS Nano. 2011;5(9):6945–54.
111. Zhao C, Xue J, Ran F, Sun S. Modifikacija polietersulfonskih membrana - pregled metoda. Prog Mater Sci. 2013;58(1):76–150.
112. Goldberg AL. Razgradnja proteina i zaštita od pogrešno savijenih ili oštećenih proteina. Priroda. 2003;426(6968):895–9.
113. Furie B, Furie BC. Mehanizmi bolesti: mehanizmi nastanka tromba. New Engl J Med. 2008;359(9):938–49.
114. Arepally GM. Heparinom izazvana trombocitopenija. Krv. 2017;129(21):2864–72.
115. Ratner BD. Kompatibilnost krvi - perspektiva. J Biomat Sci-Polym E. 2000; 11(11):1107–19.
116. Mao C, Qiu YZ, Sang HB, Mei H, Zhu AP, Shen J, et al. Različiti pristupi modificiranju površina biomaterijala za poboljšanje hemokompatibilnosti. Adv Colloid Interface. 2004;110(1-2):5–17.
117. Werner C, Maitz MF, Sperling C. Trenutne strategije prema hemokompatibilnim premazima. J Mater Chem. 2007;17(32):3376–84.
118. Huang J, Xue J, Xiang K, Zhang X, Cheng C, Sun S, et al. Modifikacija površine polietersulfonskih membrana miješanjem triblok kopolimera metoksil poli (etilen glikol)-poliuretan-metoksil poli (etilen glikol). Colloid Surface B. 2011;88(1):315–24.
119. Liu X, Xu Y, Wu Z, Chen H. Poli(n-vinilpirolidon)-modificirane površine za biomedicinske primjene. Macromol Biosci. 2013;13(2):147–54.
120. Li X, Wang M, Wang L, Shi X, Xu Y, Song B, et al. Blok kopolimer-modificirane površine za konjugaciju biomakromolekula uz kontrolu količine i aktivnosti. Langmuir. 2013;29(4):1122–8.
121. Modi A, Verma SK, Bellare J. Hidrofilni zif-8 ukrašeni go nano listovi poboljšavaju biokompatibilnost i performanse odvajanja polietersulfonskih membrana od šupljih vlakana: potencijalni membranski materijal za primjenu biovještačke jetre. Mater Sci Eng C. 2018;91:524–40.
122. Said N, Abidin MNZ, Hasbullah H, Ismail AF, Goh PS, Othman MHD, et al. Nanočestice željeznog oksida poboljšale su biokompatibilnost i uklanjanje srednjeg molekula uremičkog toksina polisulfonskih membrana od šupljih vlakana. J Appl Polym Sci. 2019;136(48):48234.
123. Wang L, Gong T, Brown Z, Randle C, Guan Y, Ye W, et al. Magnetne nanočestice inspirirane ascidijanom, koje oponašaju heparin, s potencijalom za primjenu u hemodijalizi kao reciklažni antikoagulansi. ACS Biomater Sci Eng. 2020;6(4): 1998–2006.
124. Cheng C, Sun S, Zhao C. Napredak u heparinu i heparinu sličnim/imitirajućim polimer-funkcionaliziranim biomedicinskim membranama. J Mater Chem B. 2014; 2(44): 7649–72.
125. Nie S, Xue J, Lu Y, Liu Y, Wang D, Sun S, et al. Poboljšana kompatibilnost polietersulfonske membrane u krvi sa hidrofilnom i anjonskom površinom. Colloid Surface B. 2012;100:116–25.
126. Li L, Cheng C, Xiang T, Tang M, Zhao W, Sun S, et al. Modifikacija polietersulfonske membrane za hemodijalizu miješanjem poliuretana cijepljenog limunskom kiselinom i njegovog antikoagulantnog djelovanja. J Membrane Sci. 2012;405:261–74.
127. Wang LR, Qin H, Nie SQ, Sun SD, Ran F, Zhao CS. Direktna sinteza polimera (eter sulfon) sličnog heparinu i njegova kompatibilnost u krvi. Acta Biomater. 2013;9(11):8851–63.
128. Nie S, Tang M, Cheng CS, Yin Z, Wang L, Sun S, et al. Biološki inspirisan dizajn membrane sa interfejsom sličnim heparinu: produžena koagulacija krvi, inhibirana aktivacija komplementa i bio-vještačka proliferacija ćelija vezana za jetru. Biomater Sci-Uk. 2014;2(1):98–109.
129. Ma L, Qin H, Cheng C, Xia Y, He C, Nie C, et al. Samooblaganje inspirirano dagnjama na makro sučelju s poboljšanom biokompatibilnošću i bioaktivnošću putem dopaminskih polimera sličnih heparinu i heparina. J Mater Chem B. 2014;2(4):363–75.
130. Meyer TW, Peattie JWT, Miller JD, Dinh DC, Recht NS, Walther JL, et al. Povećanje klirensa otopljenih tvari vezanih za protein dodatkom sorbenta dijalizatu. J Am Soc Nephrol. 2007;18(3):868–74.
131. Patzer J. Principi dijalize vezanih rastvora. Ther Apher Dial. 2006;10(2):118–24.
132. Agar JWM. Zelena dijaliza: ekološki izazovi pred nama. Semin Dialysis. 2015;28(2):186–92.
133. Madsen B, Britt DW, Ho C, Henrie M, Ford C, Stroup E, et al. Hemodijaliza površine hemodijalizne membrane kao barijera za prijenos lipopolisaharida. J Appl Polym Sci. 2015;132(4155021).
134. Lonnemann GR. Kvalitet dijalizata: integrirani pristup. Kidney Int. 2000;5876:S112–9.
135. Susantitaphong P, Riella C, Jaber BL. Utjecaj ultračistog dijalizata na markere upale, oksidativnog stresa, ishranu i parametre anemije: meta-analiza. Nephrol Dial Transpl. 2013;28(2):438–46.
136. Gorbet MB, Sefton MV. Endotoksin: nepozvani gost. Biomaterijali. 2005; 26(34):6811–7.
137. Schepers E, Glorieux G, Eloot S, Hulko M, Boschetti-de-Fierro A, Beck W, et al. Procjena povezanosti između povećanja veličine pore membrane i propusnosti endotoksina korištenjem nove eksperimentalne simulacijske postavke dijalize. BMC Nephrol. 2018;19(1):1–0.
138. Glorieux G, Hulko M, Speidel R, Brodbeck K, Krause B, Vanholder R. Pogled izvan endotoksina: Komparativna studija zadržavanja pirogena ultrafilterima koji se koriste za pripremu sterilne dijalizne tekućine. Sci Rep 2014;4:6390.
139. van Tellingen A, Grooteman M, Schoorl M, Bartels P, Schoorl M, van der Ploeg T, et al. Interkurentni klinički događaji predviđaju nivoe c-reaktivnog proteina u plazmi kod pacijenata na hemodijalizi. Kidney Int. 2002;62(2):632–8.
140. Darkow R, Groth T, Albrecht W, Lutzow K, Paul D. Funkcionalizirane nanočestice za vezivanje endotoksina u vodenim otopinama. Biomaterijali. 1999;20(14):1277–83.
141. Murphy MC, Patel S, Phillips GJ, Davies JG, Lloyd AW, Gun'Ko VM, et al. Adsorpcija upalnih citokina i endotoksina mezoporoznim polimerima i aktivnim ugljem. U: Rodriguez Reinoso F, McEnaney B, Rouquerol J, Unger K, urednici. Studije o površinskoj znanosti i katalizi; 2002. str. 515–20.
Cui Gao1, Qian Zhang1, Yi Yang1,2,3, Yangyang Li4,5 i Weiqiang Lin1,3
1 Centar za bubrežne bolesti, Prva pridružena bolnica, Medicinski fakultet Univerziteta Zhejiang, Hangzhou 310003, Zhejiang, Kina.
2 Odsjek za nefrologiju, Četvrta pridružena bolnica, Medicinski fakultet Univerziteta Zhejiang, Yiwu 322000, Zhejiang, Kina.
3 Međunarodna instituta za medicinu, Četvrta pridružena bolnica, Medicinski fakultet Univerziteta Zhejiang, Yiwu 322000, Zhejiang, Kina.
4 Ključna laboratorija za istraživanje reproduktivnog zdravlja žena u provinciji Zhejiang, Ženska bolnica, Medicinski fakultet Univerziteta Zhejiang, Hangzhou 310006, Zhejiang, Kina.
5 Cancer Center, Univerzitet Zhejiang, Hangzhou 310058, Zhejiang, Kina.






