Dio Ⅰ Učinci nivoa proteina i vlakana u ishrani na performanse rasta, pojavu gihta, crijevne mikrobne zajednice i imunoregulaciju u osi guslinga
May 06, 2023
Abstract
Trenutna studija je procijenila efekte dijetetskih proteina i vlakana na učinak rasta, pojavu gihta, crijevne mikrobne zajednice i imunoregulaciju u osovini crijeva i bubrega guščara. Potpuno randomizirani faktorski dizajn od 2 £ 3 je usvojen sa 2 nivoa CP (180 [18CP] i 220 [22CP] g/kg) i 3 nivoa sirovih vlakana (CF) (30 [nizak CF], 50 [srednji CF], i 70 [visoki CF] g/kg). Dijeta s visokim CP ili niskim CF predisponirala je guske na giht. Dijeta bogata proteinima pogoršala je funkciju bubrega; koncentracije UA i Cr u serumu, kao i aktivnost XOD kod 9-dnevnih guščara hranjenih 22 posto CP dijeta su značajno povećane. Iako razine CF od 3 do 7 posto nisu direktno utjecale na zdravlje bubrega, povećanje razine CF moglo bi ubrzati povećanje probiotika u slijepom crijevu guščara i spriječiti zlonamjerne bakterije, ublažavajući crijevnu disbiozu uzrokovanu ishranom s visokim sadržajem proteina. Analiza mikrobiote cekalnog crijeva putem sekvenciranja 16Sr RNK otkrila je da je brojnost Enterococcus u 22CP grupi bila veća od one u 18CP grupi, ali se smanjivala s povećanjem nivoa CF na d 9. Obilje Lactobacillusa se povećavalo s povećanjem nivoa CF. Osim toga, više koncentracije LPS-a i proinflamatornih citokina u serumu i povećani nivoi ekspresije mRNA u tkivima cekalnog crijeva, krajnika i bubrega ukazuju na to da ishrana s visokim sadržajem proteina može aktivirati TLR4/MyD88/NFkB put i inducirati i crijevnu i bubrežnu upalu kod mladih guščara. Utvrđeno je da se koncentracije LPS u serumu na d 9 smanjuju s povećanjem CF, iako promjena nivoa CF u ishrani nije direktno uticala na serumske imunološke indekse gušara. U zaključku, ishrana sa visokim CP je imala negativan uticaj na pojavu gihta, mikrobne zajednice i imunoregulaciju u osovini creva i bubrega kod gušara, dok je odgovarajuće povećan nivo dijetalnih vlakana pomogao u održavanju ravnoteže creva i smanjenju koncentracije LPS u serumu. Predlažemo ishranu od 18 posto CP u kombinaciji sa 5 posto CF kao optimalnu kombinaciju za hranu za guske.
Ključne riječi
sirova vlakna, proteini, gušći giht, crijevne mikrobne zajednice, osovina crijevo-bubreg,Cistancheove prednosti.

Kliknite ovdje da saznatekakvi su efekti Cistanchea na bubrege
Uvod
Guske, koje su biljojedi, zavise od dijetalnih vlakana za obavljanje normalnih aktivnosti. Poznato je da umjereni nivoi sirovih vlakana (CF) u ishrani povećavaju otpornost na bolesti i podstiču rast peradi modulacijom crijevne mikroekološke ravnoteže i jačanjem imunoloških funkcija (Jha i Mishra, 2021.) Wils-Plotz et al. (2013). izvijestili su da je uključivanje pektina u ishrani povećalo ekspresiju IL- 12 u ilealnoj sluzokoži i povećalo proizvodnju interferona-g u slepim krajnicima. Nekoliko studija je pokazalo da ishrana sa niskim sadržajem CF smanjuje mikrobnu raznolikost, kao i relativno obilje korisne mikrobiote u ceka gusaka na d 70, čime negativno utiče na performanse rasta, iskorišćenost nutrijenata i imunitet crevne sluzokože ovih gusaka (Li et al., 2017; Li et al., 2018a). Dijetalna CF može pomoći u održavanju funkcije crijevne barijere jačanjem strukture i funkcije sluznice, kao i povećanjem populacije i raznolikosti komenzalnih bakterija u gastrointestinalnom traktu. Što je još važnije, mlade ptice su navodno osjetljivije na promjene nutrijenata i crijevnih mikrobnih zajednica od odraslih (Gao et al., 2017). Međutim, studije o učinku CF u ishrani na mikrobiotu crijeva i otpornost na bolesti kod gusaka su rijetke.
Performanse rasta kod ptica manje su osjetljive na promjene u nivou proteina nego na promjene u energiji hrane u hrani kako bi se zadovoljila njihova prvobitna voljna priroda (Shi et al., 2006). Prijavljeno je da nije primećena značajna razlika u povećanju telesne težine kod gusaka sa nivoom proteina u ishrani u rasponu od 16 do 22 procenta, što se čini previše uopštenim po obimu (Summers et al., 1986). Suprotno tome, koncentracije proteina u ishrani imaju snažan učinak na ravnotežu crijevne flore i otpornost na bolesti peradi (Lee et al., 2020). Visceralni giht, koji se javlja uglavnom kod ptica, je metabolička bolest uzrokovana oštećenom funkcijom bubrega, praćenom nakupljanjem kristala urata u različitim organima (Zhang et al., 2018). Naša prethodna studija pokazala je da je ishrana bogata proteinima bila uključena u ozljedu bubrega i disbiozu crijevne mikrobiote povezane s gihtom kod gušara (Xi et al., 2020a). Rezultati ove studije pokazali su da su, u poređenju sa gušćima hranjenim dijetom sa 16 i 18 posto sirovih proteina (CP), guščići hranjeni hranom sa 22 posto CP pretrpjeli ozljedu epitelnih stanica crijeva i disbiozu cekalne mikrobiote, što je dovelo do ozljede bubrega ili čak gihta. Čini se da mikrobiota gastrointestinalnog trakta i njeni metaboliti igraju središnju ulogu u jačanju imuniteta osovine crijeva i bubrega kod peradi (De Cesare et al., 2019.; Xi et al., 2020.b). Stoga, identificiranje odgovarajućeg programa ishrane, koji se fokusira na efekte CF i CP u ishrani, može pomoći da se minimizira incidenca gihta i poboljša imunitet održavanjem crijevne mikroekološke ravnoteže i poboljšanjem relativne imunološke regulacije kod gusaka.
Intestinalni mikrobiom ima dubok uticaj na imunološku regulaciju crijeva, što utiče na sistemski imunitet i doprinosi imunološkoj ravnoteži. Promjene u sastavu ishrane, uključujući nivoe CP i CF, utiču na sastav i metaboličke aktivnosti mikrobiote koja se prilagođava crijevnoj sredini (Liu et al., 2014). Kod peradi svaki poremećaj mikrobioma može izazvati neravnotežu u sistemskom imunitetu, doprinoseći smanjenju otpornosti na bolesti. U našoj prethodnoj studiji otkrili smo da disbioza crijevne mikrobiote povećava rizik od visceralnog gihta kod gusaka povećanjem upale, kao i translokacijom lipopolisaharida dobivenog iz crijeva (LPS) u osovini crijeva i bubrega. U ovoj složenoj kaskadi, LPS ligacija aktivira nuklearni faktor, kapa-light-lanac-pojačivač puta aktiviranih B stanica (NF-kB) i proizvodnju pro-upalnih citokina, kao što su interleukin 1b (IL1b) i faktor nekroze tumora a (TNFa), čime se potiče razvoj imunološke tolerancije u crijevima i bubrezima guščara (Xi et al., 2019.). Ova studija se fokusirala na istraživanje mikrobnih zajednica koje naseljavaju cekum gusaka koji su hranjeni različitim nivoima CP i CF u ishrani, i mjerila je promjene u pojavi gihta analizom imunoregulacije i upalnih odgovora induciranih u osovini crijeva i bubrega.

Standardized Cistanche
materijali i metode
1. Etičko odobrenje
Studiju je odobrio Istraživački komitet Jiangsu akademije poljoprivrednih nauka i sprovedena je u skladu sa propisima Uprave za poslove koji se odnose na eksperimentalne životinje (Naredba br. 63 Jiangsu akademije poljoprivrednih nauka od 8. jula 2014.). Svi eksperimenti su provedeni prema smjernicama ARRIVE (Animal Research: Reporting of In vivo Experiments).
2. Eksperimentalni dizajn
Ovo istraživanje je sprovedeno od 2. do 17. novembra 2020 u Centru za eksperimentalne životinje Jiangsu akademije poljoprivrednih nauka (Nanjing, Kina). Ukupno 1,620 jednodnevnih Taizhou gusaka (Anser domestica, 100 posto ,), koje je nabavila Tianzhijiao Breeding Geese Limited Company (Chuzhou, Kina), nasumično je dodijeljeno 6 eksperimentalnih grupa. Svaki tretman je imao 6 ponavljanja, a svaka replika je sadržavala 45 ptica. Za eksperiment je korišten potpuno randomizirani faktorski dizajn od 2 £ 3. Pripremljeno je šest dijeta sa 2 nivoa CP i tri nivoa CF (Tabela 1). 2 nivoa CP su bila 180 (18CP) i 220 (22CP) g/kg, a tri nivoa CF su bila 30 (nizak CF), 50 (srednji CF) i 70 (visok CF) g/kg. Svi guščari su uzgajani u termostatskoj kućici sa kavezima od nerđajućeg čelika identične veličine (1,20 £ 1,00 £ 0,50 m3, 9 gusaka po kavezu, gustina nasada: 7,5 jedinki/m2), koji su postavljeni 0,50 m iznad zemlje. Guščići su hranjeni pod standardnim uslovima upravljanja hranom za pelete i vodom ad libitum. Broj visećih hranilica i pojilica za bradavice u svakom kavezu bio je dovoljan tokom čitave studije. Temperatura okoline je održavana na 30 stepeni od d 0 do 3, 29 stepeni od d 4 do 6, 28 stepeni od d 7 do 9 i 26 stepeni od d 10 do kraja eksperimenta. Relativna vlažnost tokom 21-d eksperimentalnog perioda bila je približno 60 posto. Izvori svetlosti (belo svetlo, 400 −760 nm) su izjednačeni sa osvetljenošću od 15 § 0,3 luksa na nivou ptičije glave, sa svetlosnim rasporedom od 22 h svetlosti od d 0 do 3, 18 h svetlosti od d 4 do 14 i 16 h svjetlosti od d 15 do 21 u ciklusu 24-h.
The basal diet was formulated to meet or exceed National Research Council (NRC, 1994) nutrient requirements for growing geese. The composition of experimental diets is presented (Table 1). Dietary samples (>1 posto svježe hrane) nasumično nabavljeno sa 5 lokacija pomiješano je za analizu. CP i CF su mjereni prema GB/T6432 (Kineski nacionalni standard: Određivanje sirovih proteina u hrani za životinje) i GB/T6434 (Kineski nacionalni standard: Određivanje sirovih vlakana u hrani).

ADFI i BW (živa težina) gusaka su zabilježeni pomoću elektronske vage (YP60001, Hengji, Šangaj, Kina) prije hranjenja tokom testa, a ADG i omjer konverzije hrane (FCR) su izračunati na kraju eksperimenta. Osim toga, kumulativni morbiditet gihta svih replika (svaka replika sadržavala je 45 ptica) među različitim tretmanima je sumirana nakon eksperimentalnog perioda. Standard selekcije za giht je definiran kao guščić koji pokazuje velike lezije bubrega i koncentraciju mokraćne kiseline u serumu (UA) iznad granične vrijednosti prezasićenosti urata (mužjak, 416 mmol/L i ženka, 357 mmol/L). Tipične preovlađujuće velike lezije bubrega su blijedi, mrljasti i natečeni, a bubrežni tubuli i ureteri su prošireni viškom urata (Xi et al., 2020a).

Herba Cistanche
3. Mjerenje metabolita u serumu
Trideset i šest guščića (n=6 guščića/tretman) je nasumično odabrano za trenutno uzimanje krvi (5 mL/guščić), nakon dekapitacije, preko epruveta za prikupljanje krvi bez antikoagulansa na d 9 i 18, respektivno. Svi uzorci krvi su inkubirani na 37 stepeni 2 h nakon sakupljanja i centrifugirani na 1,5{{10}0 £ g tokom 15 minuta. Dobijeni serumi su čuvani u Eppendorf epruvetama od 0,6 mL na 80 stepeni do dalje analize. Nivoi UA u serumu određeni su kolorimetrijom fosfovolframske kiseline. Koncentracije kreatinina (Cr) i dušika uree (UN), kao i aktivnost ksantin oksidaze (XOD) određene su enzimskom kolorimetrijom pomoću spektrofotometra za mikroploče (Promega Corporation, Madison, WI). Ove komplete je isporučio Institut za bioinženjering Jiancheng (Nanjing, Kina); kodovi su bili C012 (UA), C011-2 (Cr), C013-2 (UN) i A002 (XOD). Koncentracije IgM, IgA i IgG u serumu eksperimentalnih gusaka mjerene su korištenjem kompleta ELISA imunoglobulina guske kupljene od Shanghai J&I Biotechnology Co., Ltd (Šangaj, Kina). Imuni kompleksi koji cirkuliraju u serumu (CIC), IL-1b i TNF-a koncentracija su određivani korištenjem komercijalnog ELISA kompleta za gusku (Jiancheng Bioengineering Institute, Nanjing, Kina). Aktivnost diamin oksidaze (DAO) mjerena je enzimskom kolorimetrijom pomoću automatskog biohemijskog analizatora (Hitachi, Tokio, Japan). LPS u serumu mjeren je tradicionalnim Limulus testom (Limulus Assay Biotechnology Company Ltd., Xiamen, Kina). Opseg detekcije LPS-a u testu Limulus kretao se od 0,015 do 0,6 EU/mL. Svi materijali korišteni za prikupljanje krvi i mjerenje endotoksina bili su bez pirogena. Svi testovi su obavljeni prema uputama proizvođača. Uzorci seruma su testirani u tri primjerka. Koeficijenti varijacije unutar i među testovima za testove su bili<10% and <15%, respectively.
4. Histomorfološka opservacija
Slijepa crijeva (dužine {{0}} cm) od 36 gusaka (n=6 gusaka/tretman) su sakupljena nakon uzimanja uzoraka krvi na d 9 i 18 za histološku analizu. Uzorci sakupljeni od guščara fiksirani su u 4 posto paraformaldehida, usađeni u parafin i izrezani (debljina kriške: 3 mm; 4 kriške po guščaru). Patološke promjene na cekumu (otprilike 7 cm distalno od piloričnog sfinktera) pregledane su pod svjetlosnim mikroskopom (OLYMPUS, Tokyo, Japan) nakon bojenja hematoksilinom i eozinom (HE). Visina resica i dubina kripte cekuma mjerene su korištenjem softvera ImageJ (verzija 1.8.0; National Institutes of Health, Bethesda, MD). Zabilježeno je osam mjerenja različitih intaktnih resica po krišku (8 mjerenja u 3 uzastopna vidna polja). Statističke analize histoloških mjerenja vršene su na osnovu prosjeka od 32 mjerenja po gusku (4 kriške po gusku i 8 mjerenja po krišku). Gustina peharastih ćelija je izračunata kao broj peharastih ćelija podeljen sa odgovarajućom dužinom resica, koja je zatim usrednjena i izražena kao broj peharastih ćelija na 100 mm dužine resica.

Cistanche tubulosa
5. 16S rRNA Sekvenciranje sadržaja cekuma
Sadržaj cekuma gusaka (6 gusaka/tretman £ 6 grupa £ uzorkovanje dva puta=72 gusaka) sakupljen je na d 9 i d 18 u 2 mL sterilne kriogene bočice sa unutrašnjim navojem i odmah pohranjen u tečnom dušiku za analizu 16S rDNK . DNK iz uzoraka sadržaja cekuma ekstrahirana je korištenjem MicroElute Genomic DNK kompleta (D3096-01, Omega Biotek Inc., Norcross, GA) prema uputama proizvođača. Prazni uzorci koji se sastoje od neiskorištenih briseva obrađeni su ekstrakcijom DNK i provjereno je da ne proizvode 16S amplikon. Ukupna DNK je eluirana u 50 mL pufera za eluiranje korištenjem modificirane procedure koju je opisao proizvođač (QIAGEN, Dusseldorf, Njemačka) i čuvana na 80 stepeni.
Koristeći ukupnu DNK uzoraka kao šablon i 16S rDNK prajmere (343F - 50 - TACGGRAGGCAGCAG -30; 798R - 50 - AGGGTATCTAATCCT-30), pojačali smo V3-V4 regiju bakterije 16S rRNA. Sve reakcije su izvedene u mješavini od 25 mL (ukupni volumen) koja je sadržavala 25 ng ekstrakta genomske DNK, 12,5 mL PCR premiksa, 2,5 mL svakog prajmera i vodu za PCR za podešavanje volumena. PCR proizvodi su normalizovani korišćenjem AxyPrep Mag PCR normalizatora (Axygen Biosciences, Union City, CA), što je omogućilo preskakanje koraka kvantifikacije, bez obzira na količinu PCR-a dostavljenu na sekvenciranje. Pulovi amplikona su pripremljeni za sekvenciranje korištenjem AMPure XT kuglica (Beckman Coulter Genomics, Danvers, MA; izvodi OebioTech Co., Ltd, Šangaj, Kina). Veličina i količina biblioteke amplikona procijenjeni su korištenjem LabChip GX (Perkin Elmer, Waltham, MA) i Kapa Library Quantification Kit za Illumina (Kapa Biosciences, Woburn, MA), respektivno. PhiX Control biblioteka (v3) (Illumina) je kombinovana sa bibliotekom amplikona (očekivano 30 procenata). Biblioteka je bila grupisana pri gustini od približno 570 K/mm2. Biblioteke su sekvencionirane na 300PE MiSeq serijama, gdje je jedna biblioteka sekvencionirana sa oba protokola korištenjem standardnih prajmera za sekvenciranje Illumina, čime je eliminirana potreba za trećim (ili četvrtim) čitanjem indeksa. Očitavanja su filtrirana pomoću kvantitativnih uvida u filtere kvaliteta mikrobne ekologije (QIIME;). Cjevovod CDHIT je korišten za odabir operativnih taksonomskih jedinica (OTU) pripremom OTU tablice. OTU-ovima su dodijeljene sekvence sa 97 posto sličnosti. Reprezentativne sekvence su odabrane za svaki OTU, a taksonomski podaci su zatim dodijeljeni svakoj reprezentativnoj sekvenci koristeći klasifikator Ribosomal Database Project (RDP). GenBank pristupni broj ovih OTU nukleotidnih sekvenci je SAMN21014082. Za procjenu alfa raznolikosti, OTU tabela je rarificirana i izračunate su sljedeće 4 metrike: Chao1 metrika za procjenu bogatstva; metrika posmatrane vrste kao broj jedinstvenih OTU pronađenih u uzorku; Shannon indeks; i Simpsonov indeks.
6. PCR u realnom vremenu
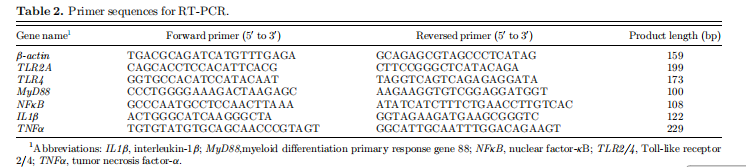
(n {{0}} guščića/tretman) prikupljeni su 9. i 18. dana za PCR (RT-PCR) analizu u realnom vremenu. Ukupna RNK je ekstrahovana iz tkiva, korišćenjem TRIzol reagensa (Life Technologies, Grand Island, NY), i reverzno transkribovana pomoću kompleta za nivoe reverzne transkripcije (TaKaRa, Dalian, Kina), prema protokolu proizvođača. b-aktin je korišten kao invarijantna kontrola. Prajmeri su dizajnirani pomoću softvera Primer Premier 5.0 i njihove sekvence su navedene (Tablica 2). RT-PCR je izveden upotrebom SYBR Premix Ex Taq (Roche, Basel, Švicarska). Svi RT-PCR-ovi su izvedeni u tri primjerka. Relativni nivoi ekspresije ciljnih gena određeni su pomoću 2 DDCt metode.
7. Analiza podataka
Eksperimentalni podaci izvedeni iz 6 ponavljanja po tretmanu analizirani su korištenjem programa IBM SPSS Statistics 16 (IBM Corporation, Somers, NY). Svaka replika je razmatrana kao eksperimentalna jedinica, a korištena statistička procedura je multivarijantna analiza varijanse korištenjem procedure generalnog linearnog modela (GLM). Kada su utvrđene značajne razlike, razdvojena su sredina tretmana i upoređena korišćenjem Duncanovog testa višestrukog opsega. Dvostrani test se smatra statistički značajnim pri nivou vjerovatnoće manjim od 5 posto (P < 0.05).
Yumeng Xi *, Yuanpi Huang, y Yue Li *, Yunmao Huang #, Junshu Yan * i Zhendan Shi *.
* Ključna laboratorija za integrisanu poljoprivredu i stočarstvo Ministarstva poljoprivrede i ruralnih poslova, Institut za stočarstvo, Jiangsu akademija poljoprivrednih nauka, Nanjing 210014, Kina;
# College of Animal Science, Zhongkai University of Agriculture and Engineering, Guangzhou 510000, Kina.
