Prvi dio Disfunkcija endotelnih stanica i povećani kardiovaskularni rizik kod pacijenata s kroničnom bubrežnom bolešću
Jun 07, 2023
Abstract
Endotel se smatra čuvarom zida krvnih sudova, koji održava i reguliše vaskularni integritet. Kod pacijenata s kroničnom bubrežnom bolešću, zaštitne funkcije endotelnih stanica su narušene zbog proinflamatornog, protrombotičkog i uremičnog okruženja uzrokovanog padom funkcije bubrega, što doprinosi povećanju kardiovaskularnih komplikacija u ovoj ranjivoj populaciji pacijenata. U ovom pregledu razmatramo funkcionisanje endotelnih ćelija u zdravim uslovima i doprinos disfunkcije endotelnih ćelija kardiovaskularnim bolestima. Nadalje, sumiramo fenotipske promjene endotela kod pacijenata s kroničnom bubrežnom bolešću i odnos disfunkcije endotelnih stanica i kardiovaskularnog rizika kod kronične bubrežne bolesti. Također razmatramo mehanizme koji leže u osnovi endotelnih promjena kod kronične bolesti bubrega i razmatramo potencijalne farmakološke intervencije koje mogu poboljšati zdravlje endotela.
Ključne riječi
ateroskleroza, kardiovaskularne bolesti, hronične bolesti bubrega, endotelne ćelije, vaskularna ukočenost.

Kliknite ovdje da kupite dodatak Cistanche
POVEĆAN KARDIOVASKULARNI RIZIK KOD HRONIČNE BOLESTI BUBREGA
Hronična bolest bubrega (CKD) je definirana oštećenjem bubrega ili smanjenom funkcijom filtracije bubrega (brzina glomerularne filtracije<60 mL/minute per 1.73 m²) for a period beyond 3 months that affects health.1 With a global prevalence of ≈13.4%,2 CKD imposes a serious burden on our socioeconomic and healthcare system. CKD is a progressive disease, classified into stages 1 to 5 based on the reduction in kidney function (Figure 1A).1 In end-stage kidney disease (CKD stage 5: glomerular filtration rate <15 mL/minute per 1.73 m²), patients require kidney support therapy as dialysis or kidney transplantation to replace the failing kidney function.

Treba napomenuti da su pacijenti sa umjerenom do uznapredovalom CKD-om pod povećanim kardiovaskularnim rizikom u usporedbi s općom populacijom i pacijentima s blagom kroničnom bubregom, sa nižom procijenjenom stopom glomerularne filtracije i višom albuminurijom identifikovanim kao faktorima rizika za smrtnost od svih uzroka i kardiovaskularne smrtnosti, neovisno o tradicionalnoj kardiovaskularnoj smrti. faktori rizika.5,6 Sve u svemu, 33,3 do 37,1 procenat pacijenata sa CKD3(a/b) i 39,9 procenata pacijenata sa CKD4 umire od kardiovaskularnih bolesti (KVB) u poređenju sa 21,7 procenata do 26 procenata opšte populacije (Slika 1B). 3 Za pacijente sa završnom stadijumom bubrežne bolesti u dobi od 25 do 34 godine, godišnji mortalitet je čak povećan 500 do 1000 puta u poređenju sa kontrolnom skupinom slične dobi sa zdravom funkcijom bubrega i uporediv je sa 85-godišnjacima u općoj populaciji, naglašavajući visoko kardiovaskularno opterećenje kod CKD.6
U opštoj populaciji, infarkt miokarda i cerebrovaskularni događaji su najvažniji kardiovaskularni uzroci smrti, koji leže u osnovi ≈75 procenata svih smrtnih slučajeva povezanih sa KVB (Slika 1C).4 Takođe, kod pacijenata sa CKD5 na dijalizi (CKD5D), ovi tipovi KVB ostaju važni jer čine 45 posto (infarkt miokarda) i 13 posto (cerebrovaskularni događaji) smrti od kardiovaskularnih uzroka, iako uz zajedničku odgovornost od ≈58 posto svih smrtnih slučajeva povezanih s KVB, njihova relativna važnost je smanjena u usporedbi s općim stanovništva. Umjesto toga, pacijenti sa CKD5D pokazuju relativno povećanje iznenadne srčane smrti i zatajenja srca, odgovorni su za 28 posto i 9 posto svih smrtnih slučajeva povezanih s KVB u poređenju sa 2 posto i 7 posto kao što je uočeno u općoj populaciji (slika 1C).4 Ovo otkriva visok porast, posebno u riziku od iznenadne srčane smrti kod uznapredovale CKD.4
1. Ateroskleroza i infarkt miokarda
Glavni osnovni uzrok i infarkta miokarda i moždanog udara je ateroskleroza, upalna bolest arterija srednje i velike veličine uzrokovana lipidima koja izaziva razvoj aterosklerotskih lezija.7 Ove lezije postepeno rastu s vremenom i na kraju mogu ograničiti protok krvi ili pokrenuti trombozu kroz ruptura plaka ili erozija.7,8 Pacijenti sa CKD3-5D pokazuju povećanu prevalenciju subkliničkih aterosklerotskih lezija u poređenju sa općom populacijom, sa većim povećanjem uznapredovalih stadijuma CKD nakon prilagođavanja spolu, starosti i dijabetesu. 9,10 Nadalje, u usporedbi s pacijentima bez progresije CKD, pacijenti sa progresijom CKD-a tokom 24 mjeseca češće su pokazivali i progresiju aterosklerotskih lezija kao što je detektirano ultrazvukom.10,11 Nakon akutnog infarkta miokarda, pacijenti sa CKD pokazuju smanjeno preživljavanje tokom vremena u poređenju sa pacijentima koji nemaju CKD, sa povećanim rizikom od smrti, kao i nefatalnim srčanim događajima sa povećanjem stadijuma CKD.12
2. Iznenadna srčana smrt i uremička kardiomiopatija
U općoj populaciji, koronarna bolest srca je odgovorna za 80 posto iznenadnih srčanih smrti.13 Disproporcionalno povećanje iznenadne srčane smrti kod pacijenata sa uznapredovalom CKD ukazuje na razlike u njenoj patofiziologiji i uzrocima opadanja funkcije bubrega. Hipertrofija lijeve komore značajno je povezana s povećanim rizikom od iznenadne srčane smrti u općoj populaciji14 i može biti uzrokovana preopterećenjem srca (preopterećenje intravaskularnim volumenom), srčanim naknadnim opterećenjem (preopterećenjem pritiskom) ili faktorima koji ne ovise o naknadnom opterećenju/preopterećenju.15 Pacijenti s CKD češće se javlja hipertrofijom lijeve komore, s prevalencijom do 40 posto pa čak i 75 posto kod pacijenata s CKD5D.16 Zajedno sa srčanom fibrozom, hipertrofija lijeve komore jedno je od obilježja uremičke kardiomiopatije i može izazvati srčane električne poremećaje i smrtonosno aritmije.15

Cistanche tubulosa
3. Endotelna (ćelijska) disfunkcija kao doprinos kardiovaskularnom riziku
Glavni faktor koji doprinosi povećanom kardiovaskularnom riziku je disfunkcija endotelnih ćelija, koja obuhvata čitav niz maladaptivnih promena u funkcionalnom fenotipu endotelnih ćelija povezanih sa povećanim kardiovaskularnim rizikom. Ovaj termin je predložen u izvrsnoj recenziji Gimbronea et al17 kako bi se napravila razlika od užeg pojma "endotelna disfunkcija", koji se obično koristi za označavanje endotelnih abnormalnosti koje izazivaju smanjenje bioraspoloživosti dušikovog oksida i povezanu vaskularnu relaksaciju. Značajna heterogenost endotela postoji u cijelom vaskularnom stablu, na primjer, kada se uporede arterije i vene, kao i mikrovaskulatura (uključujući velike elastične, kao i mišićne arterije) u odnosu na mikrovaskulaturu (uključujući kapilare, arteriole i venule) i oboje disfunkcija endotelnih ćelija na makro- i mikrovaskularnom nivou doprinosi povećanom kardiovaskularnom riziku. U ovom pregledu raspravljamo o doprinosu disfunkcije endotelnih ćelija KVB sa posebnim fokusom na pacijente sa CKD. Pregledavamo nalaze o molekularnim mehanizmima koji leže u osnovi disfunkcije endotelnih ćelija u CKD, kao i raspravljamo o utjecaju farmakoloških intervencija.
DISFUNKCIJA ENDOTELIJALNIH ĆELIJA KAO DOPRINOS KARDIOVASKULARNOM RIZIKU
1. Disfunkcija endotelnih ćelija i rizik od ateroskleroze
Sloj endotelnih ćelija vaskulature pruža polupropusnu barijeru koja omogućava regulisanu razmenu tečnosti, molekula i ćelija i igra važnu ulogu u održavanju vaskularnog zdravlja (Slika 2). Disfunkcija makrovaskularnih endotelnih ćelija je rani događaj u razvoju aterosklerotskih lezija. S jedne strane, na njega utiču hemodinamski faktori: u područjima arterija otpornim na aterosklerozu, laminarni protok krvi doprinosi zaštitnom fenotipu endotelnih ćelija. Međutim, regije arterijske vaskulature sklone aterosklerozi izložene su poremećenom, oscilatornom protoku krvi i povezanom niskom vremenskom prosječnom stresu smicanja, koji inducira oksidativni stres, endotelne fenotipske promjene i promjene staničnih spojeva, kao i promet endotelnih stanica ( detaljnije u pregledu Gimbronea et al17). Nadalje, inflamatorni pokretači kao što su proinflamatorni citokini, oxLDL (oksidirani protein niske gustoće) kao i različiti kardiovaskularni faktori rizika kao što su metabolički poremećaji i pušenje, doprinose disfunkciji endotelnih stanica. Također, prekomjerno rastezanje krvnih žila može izazvati endotelnu permeabilnost, upalne odgovore i oksidativni stres.18 U kombinaciji, ovo pokreće proinflamatornu signalizaciju u endotelnim stanicama uz pojačanu regulaciju proinflamatornih citokina (npr. IL [interleukin]-1 {8}}), hemokini (npr. CC motiv hemokinski ligand 2) i endotelno-leukocitni adhezioni molekuli (VCAM-1 [molekula adhezije vaskularnih stanica 1], ICAM-1 [međustanični adhezioni molekul 1] , P-selektin), smanjuje endotelnu proizvodnju ateroprotektivnog dušikovog oksida i povećava propusnost endotela. Kao rezultat toga, upalni leukociti se regrutuju, prianjaju na upaljeni endotel i infiltriraju u vaskularni zid, gdje zajedno sa akumuliranim lipidima doprinose razvoju i progresiji aterosklerotskih lezija.7 Ateroprotektivni fenotip endotela reguliraju glavni transkriptni faktori. kao KLF (faktor sličan Krupelu)-2, KLF-4 i NRF (faktor povezan s nuklearnim faktorom eritroida 2-)-2, dok NF-κB (nuklearni faktor-κB ) je ključni faktor transkripcije koji pokreće upalu endotela.17 Nadalje, endotelne ćelije pokazuju dediferencijaciju i povećanu heterogenost tokom progresije ateroskleroze, sa također znakovima tranzicije endotela u mezenhim. Prelaz iz endotela u mezenhim karakteriše sticanje funkcija mezenhimskih ćelija kao proizvodnja ECM (ekstracelularnog matriksa) i uglavnom je vođen transkripcionim faktorima Puž, Slug i Twist1. Njegov opseg je povezan s ozbiljnošću plakova ateroskleroze u ljudskim arterijama,19,20, a studije na životinjama koje su istraživale ključne regulatore endotelne-mezenhimalne tranzicije sugerirale su važnu ulogu u progresiji plaka20 i kalcifikacije,21 kao što je detaljno razmotreno u odličnom pregledu. od Souilhol et al.22

Treba napomenuti da disfunkcija endotelnih stanica ne doprinosi samo inicijaciji plaka, progresiji i destabilizaciji s naknadnom rupturom plaka, već i eroziji aterosklerotskog plaka, za koju se očekuje da je odgovorna za jednu trećinu akutnih koronarnih sindroma. Ovdje, kronična endotelna aktivacija niskog stupnja pomoću na primjer TLR (toll-like receptor)-2 liganda u kombinaciji sa apoptozom endotelnih ćelija i katabolizmom komponenti bazalne membrane može izazvati odvajanje endotelnih ćelija sa naknadnim formiranjem tromba na denudiranom području.8
2. Disfunkcija endotelnih ćelija i rizik od tromboze
Zdrav, funkcionalan endotelni sloj na makro- i mikrovaskularnom nivou je ključan u regulaciji hemostaze i interferira kako na nivou primarne tako i na sekundarnoj hemostazi kako bi se spriječila neželjena aktivacija i koagulacija trombocita (Slika 2). Na nivou primarne hemostaze, endotel izaziva snažnu inhibiciju trombocita kontinuiranim lučenjem dušikovog oksida (NO) i prostaciklina, što uzrokuje povećanje intratrombocitnog cGMP (ciklički gvanozin monofosfat) i cAMP (ciklički adenozin monofosfat) radi prevencije.23 aktivacija trombocita ekstracelularnim ATP-om i ADP-om, endotelni sloj eksprimira CD39 i CD73, egzonukleaze koje pretvaraju ATP i ADP u adenozin, inhibitor trombocita koji povećanjem nivoa cAMP-a trombocita podiže prag aktivacije trombocita.24 Osim toga, endotel odbija trombocite putem glikokalija. njegov negativni naboj i kao takav pomaže u prevenciji adhezije trombocita.25,26 Na nivou sekundarne hemostaze, unutar glikokaliksa, heparan sulfat proteoglikani vezuju i podstiču aktivnost ATIII (antitrombina III), snažnog inhibitora više faktora koagulacije uključujući trombin, FIXa, FXa, FXIa i FXIIa.26,27 Nadalje, endotelne ćelije eksprimiraju TFPI (inhibitor puta tkivnog faktora), serinsku proteazu koja – kako joj ime sugerira – ometa koagulaciju izazvanu TF (faktorom tkiva) i time ograničava aktivnost ekstrinzičnog puta.27 Pored TFPI, endotelne ćelije konstitutivno eksprimiraju trombomodulin, membranski vezan protein koji hvata trombin iz cirkulacije i nakon vezivanja povećava afinitet trombina za antikoagulantni protein C. Zajedno sa proteinom S, aktivira se protein C onemogućava FVa i FVIIIa.27

Nakon poremećaja metabolizma lipida, upale, oksidativnog stresa i patofiziološkog stresa na smicanje, razvija se disfunkcija endotelnih stanica, koju karakterizira smanjenje antitrombotičkih i protuupalnih svojstava i degradacija glikokaliksa. Istovremeno, disfunkcionalni endotel poprima proinflamatorne i protrombotičke karakteristike (Slike 3 i 4).27 Kao rezultat, proizvodnja NO i prostaciklina se smanjuje, dok se lučenje protrombotičkih i proinflamatornih molekula poput vWF-a (von Willebrand-ov faktor) i CC-ov faktora ligand 2 se povećava.27 Nadalje, ekspresija trombomodulina je snažno smanjena nakon disfunkcije endotelnih stanica što rezultira smanjenjem regulacije aktivacije proteina C, dok je ekspresija TF-a pojačana što favorizira aktivaciju koagulacije.27 Već tokom ranih faza neutropogeneze, ekstracelularne zamke su uključene u disfunkciju endotelnih stanica i potiču tromboinflamatorni odgovor.28

Sve u svemu, ovi protrombotički i proinflamatorni odgovori disfunkcionalnog endotela izmiču kontroli, stvarajući začarani krug u kojem disfunkcija endotelnih stanica napreduje i vaskularni integritet se gubi, što rezultira snažno povećanim rizikom od tromboze.
3. Endotelna disfunkcija, smanjena vazorelaksacija, povećana vaskularna ukočenost i kardiovaskularni rizik
Starenje, kao i patofiziološko remodeliranje vaskularnog zida od kardiovaskularnih faktora rizika (npr. hipertenzija, dijabetes, bolest bubrega) induciraju ukrućenje arterija, što smanjuje arterijsku podlogu i povećava pulsativni smicanje i pritisak na vaskulaturi. Na strukturnom nivou, ukočenost arterija karakteriše taloženje kolagena i degradacija elastina u ECM-u.29 Nadalje, tonus vaskularnih glatkih mišićnih ćelija (VSMC) i endotelna disfunkcija utiču na vaskularnu reaktivnost, sa smanjenim kapacitetom opuštanja VSMC-a, kao i smanjenim endotelom. -zavisna vazorelaksacija koja doprinosi ukočenosti arterija. Endotelne ćelije igraju važnu ulogu u vazorelaksaciji kroz proizvodnju NO pomoću eNOS-a (endotelna NO sintaza; Slika 2), sa smanjenom proizvodnjom i/ili biodostupnošću NO ili drugih vazodilatatornih supstanci koje smanjuju kapacitet vaskularne relaksacije (Slika 5).

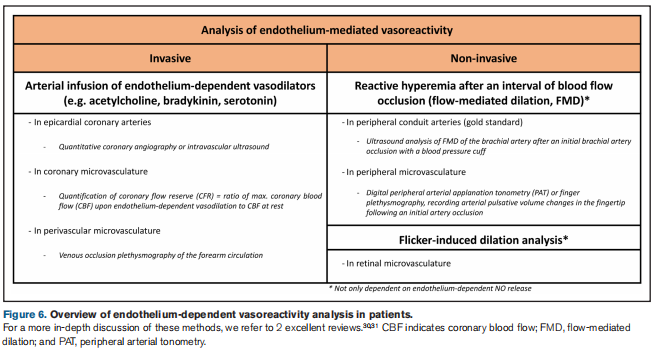
Zlatni standard za kvantifikaciju arterijske krutosti je analiza brzine protoka krvi, mjerene kao brzina pulsnog talasa (PWV, analizirana kao karotidno-femoralni PWV ili brahijalno-skočni PWV). Alternativno, oblik talasnog oblika arterijskog pritiska (analiza pulsnog talasa) pruža uvid u krutost arterija kroz kvantifikaciju indeksa povećanja. Funkcija endotela u smislu vazodilatacijskih odgovora može se mjeriti bilo invazivno ili neinvazivno unutar epikardijalnih koronarnih arterija, perifernih provodnih arterija (analizirajući proširenje brahijalne arterije posredovano protokom [FMD] kao zlatni standard) ili unutar koronarne ili periferne mikrovaskulature ( Slika 6). Prijavljeno je da periferna i koronarna endotelna disfunkcija koreliraju jedna s drugom,30,32 iako su drugi prijavili prilično skromne korelacije između periferne i koronarne endotelne disfunkcije i sugerirali potencijalni odraz različitih patologija ili vaskularnih kreveta.33 Nadalje, dok PWV i povećanje Pokazalo se da indeks dobro korelira, to nije uvijek bio slučaj za indeks povećanja i "indeks reaktivne hiperemije" kao neinvazivno očitavanje endotelijalne funkcije na periferiji, potencijalno zbog utjecaja drugih faktora osim funkcije endotela na vaskularnu krutost.34
Vaskularna ukočenost je rani prognostički marker koronarne bolesti srca.35 Vaskularna ukočenost povećava opterećenje srca; podstiče veću potražnju za energijom za srčanu ejekciju i pokreće srčanu hipertrofiju.29 Uz povećanu ukočenost arterija koja je povezana sa smanjenom Windkessel funkcijom (tj. smanjenjem elastičnog puferskog kapaciteta potrebnog za ublažavanje fluktuacija krvnog tlaka), arterijska krutost također nameće povećanu pulsiranje na mikrocirkulaciji i pojačano ciklično rastezanje endotelnih ćelija. Nedavno je pokazano da potonji pokreće lučenje proteina GAS6 (specifičan za zaustavljanje rasta 6) od strane endotelnih ćelija sa naknadnom proinflamatornom GAS6/Axl signalizacijom u monocitima i njihovom transformacijom u makrofage i dendritske ćelije. Kao što je prikazano na mišjem modelu kroničnog remodeliranja aorte izazvanog angiotenzinom II, ovo je potom doprinijelo vaskularnoj upali i upali bubrega,36,37 povezujući ukočenost arterija s daljnjim oštećenjem krajnjih organa.
Kako je endotelna disfunkcija rani događaj u KVB koji prethodi makrovaskularnim komplikacijama, također su endotelne funkcionalne analize u smislu regulacije vaskularnog tonusa intenzivno proučavane za prediktivni kapacitet kardiovaskularnog rizika izvan tradicionalnih kardiovaskularnih faktora rizika. U više studija, makro i mikrovaskularna endotelna disfunkcija mogla bi nezavisno predvidjeti kardiovaskularne događaje kod pacijenata s rizikom od koronarne bolesti.31 Na primjer, u odnosu na endotelnu reaktivnost arterija kanala (mikrovaskularna), srednja do niska endotelna funkcija zabilježena FMD brahijalne arterije je bio povezan sa povećanim rizikom od srčanih događaja kod pacijenata sa bolešću perifernih arterija koji su bili podvrgnuti vaskularnoj operaciji.38 Takođe kod pacijenata sa hroničnom srčanom insuficijencijom, endotelna disfunkcija analizirana brahijalnom i radijalnom FMD bila je povezana sa budućim srčanim događajima ili mortalitetom.39–41 Drugi su pokazali zdrava endotelna funkcija zabilježena brahijalnim FMD-om kod naizgled zdravih osoba kako bi rezultirala značajno većim preživljavanjem tokom 5-godišnje praćenja, čak i nakon prilagođavanja tradicionalnim faktorima rizika.42,43 Dakle, disfunkcija endotelnih stanica može dodati važne informacije na kardiovaskularni rizik izvan tradicionalnih faktora rizika.30 Treba napomenuti da je na ovu vrijednost analize endotelne disfunkcije za predviđanje kardiovaskularnog rizika utjecala analizirana kohorta pacijenata, budući da drugi nisu mogli potvrditi vrijednost predviđanja kardiovaskularnog rizika za analizu endotelne disfunkcije zasnovanu na FMD-u u starijoj kohorti, potencijalno zbog smanjene arterijske usklađenosti (tj. vaskularne sposobnosti da se proširi nakon povećanja pritiska) kod starijih subjekata.44 Ipak, ova studija je prijavila povezanost periferne mikrovaskularne endotelne disfunkcije s povećanim kardiovaskularnim rizikom, o čemu se govori u sljedećem pasus detaljnije.

Cistanche prah
4. Mikrovaskularna disfunkcija i kardiovaskularni rizik
Dok su veće arterije pretežno zahvaćene aterosklerotskim promjenama, disfunkcija mikrovaskulature – mreže arteriola, kapilara i venula koje omogućavaju perfuziju tkiva – je drugačija. Mikrovaskularna disfunkcija (MVD) može se razviti na nivou koronarne mikrocirkulacije kao i na periferiji u odsustvu ili prisustvu opstruktivne arterijske bolesti većih krvnih sudova. Razvoj MVD je multifaktorski i može biti rezultat funkcionalnih ili strukturnih promjena ili njihove kombinacije, ovisno o osnovnoj bolesti. U smislu funkcionalnih promjena, poremećeni vazodilatacijski odgovori – barem djelimično zavisni od endotela – leže u osnovi MVD. Nadalje, povećanje nivoa vazokonstriktivnih supstanci u kombinaciji sa pojačanom reakcijom na ove podražaje je uključeno u MVD, što doprinosi pojavi vaskularnih grčeva. Strukturne promjene povezane s MVD-om obuhvataju luminalno suženje mikrovaskulature zbog nepovoljnog vaskularnog remodeliranja i perivaskularne fibroze; mikrovaskularna kompresija; mikrovaskularna refakcija koja rezultira gubitkom koherentnih mikrovaskularnih stabala (kapilara, malih arteriola i venula); i mikroembolizacija aterosklerotskog i trombotičkog materijala.45–48
Što se tiče makrovaskularne endotelne disfunkcije, i mikrovaskularna endotelna disfunkcija je povezana s kardiovaskularnim rizikom.49 To je, na primjer, bio slučaj u populacijskoj prospektivnoj studiji, u kojoj je periferna mikrovaskularna endotelna disfunkcija – ali ne i analiza funkcije endotelnih arterija posredovana FMD-om. —u korelaciji sa kardiovaskularnim događajima (infarkt miokarda, moždani udar ili smrt) kod starijih pacijenata tokom 5 godina praćenja, čak i izvan glavnih kardiovaskularnih faktora rizika iz Framingham skora rizika.44 Na istoj liniji, periferna mikrovaskularna endotelna disfunkcija predviđa ishemijsko srce bolesti i čak je bio bolji u budućem predviđanju kardiovaskularnog rizika kod neobstruktivne koronarne arterijske bolesti u poređenju sa drugim rezultatima rizika.50 Takođe, disfunkcija endotela arteriola retine nezavisno je predvidela MACE kod pacijenata sa ili sa visokim rizikom od koronarne bolesti.51
Također o srčanoj insuficijenciji, kako pacijenti sa srčanom insuficijencijom sa smanjenom ejekcionom frakcijom lijeve komore, tako i pacijenti sa srčanom insuficijencijom sa očuvanom ejekcionom frakcijom prisutna sa mikrovaskularnom disfunkcijom. U slučaju neuspjeha sa smanjenom ejekcionom frakcijom lijeve komore, analiza periferne mikrovaskularne endotelne funkcije povezana je s povećanom stopom događaja povezanih s HF.52 Pacijenti sa srčanom insuficijencijom sa očuvanom ejekcionom frakcijom prisutna je i s velikim krvnim žilama i s mikrovaskularnom disfunkcijom.53 Nadalje, oni pokazuju smanjenje srčane mikrovaskularne gustoće54 kao i povećanje markera disfunkcije endotelnih ćelija u biopsijama miokarda, uključujući povećanje regulacije endotelnih adhezivnih molekula (E-selektin, ICAM-1), prooksidativnih regulatora (NOX{{ 7}}) i odvajanje eNOS-a.55 Predloženo je da koronarna mikrovaskularna disfunkcija doprinosi ukrućenju srčanog zida i dijastoličkoj disfunkciji kod srčane insuficijencije kod pacijenata sa očuvanom ejekcijskom frakcijom. Međutim, ostaje rasprava o tome da li ovo uključuje stvarnu uzročnu vezu ili radije ne-uzročnu povezanost između koronarne mikrovaskularne disfunkcije i srčane insuficijencije sa očuvanom ejekcionom frakcijom.56,57 Treba napomenuti da koronarna mikrovaskularna disfunkcija također može imati patofiziološku i prognostičku ulogu u drugim tipovima KVB, za koji se pozivamo na odličnu nedavnu recenziju Del Buono et al.46

Herba Cistanche i ekstrakt Cistanche
5. Disfunkcija endotelnih ćelija i vaskularno starenje
Disfunkcija endotelnih ćelija sa smanjenim kapacitetom endotelne vazodilatacije, povećanom upalom i permeabilnosti i poboljšanim protrombotičkim svojstvima, sve je gore opisano, važan je znak starenja krvnih sudova. Disfunkcija endotelnih ćelija se ne opaža samo u makrocirkulaciji, već doprinosi i mikrovaskularnoj disfunkciji nakon starenja. Vaskularno starenje nadalje karakteriziraju funkcionalne i strukturne promjene vaskularnog zida i adventicije procesima npr. upale, vaskularne kalcifikacije i remodeliranja ECM, što dodatno doprinosi povećanju vaskularne krutosti i kardiovaskularnog rizika.58
REFERENCE
1. Inker LA, Astor BC, Fox CH, Isakova T, Lash JP, Peralta CA, Kurella Tamura M, Feldman HI. KDOQI US komentar na KDIGO smjernice kliničke prakse iz 2012. za procjenu i upravljanje CKD. Am J Kidney Dis. 2014;63:713–735. doi: 10.1053/j.ajkd.2014.01.416
2. Hill NR, Fatoba ST, Oke JL, Hirst JA, O-Callaghan CA, Lasserson DS, Hobbs FDR. Globalna prevalencija hronične bolesti bubrega – sistematski pregled i meta-analiza. PLoS One. 2016;11:e0158765. doi: 10.1371/journal.pone.0158765
3. Thompson S, James M, Wiebe N, Hemmelgarn B, Manns B, Klarenbach S, Tonelli M; Alberta mreža za bolesti bubrega. Uzrok smrti kod pacijenata sa smanjenom funkcijom bubrega. J Am Soc Nephrol. 2015;26:2504–2511. doi: 10.1681/ASN.2014070714
4. Roberts MA, Polkinghorne KR, McDonald SP, Ierino FL. Sekularni trendovi u stopama kardiovaskularnog mortaliteta pacijenata koji su na dijalizi u poređenju sa općom populacijom. Am J Kidney Dis. 2011;58:64–72. doi: 10.1053/j.ajkd.2011.01.024
5. van der Velde M, Matsushita K, Coresh J, Astor BC, Woodward M, Levey A, de Jong P, Gansevoort RT, Matsushita K, Coresh J, et al; Konzorcij za prognozu hronične bolesti bubrega. Niža procijenjena stopa glomerularne filtracije i veća albuminurija povezani su sa smrtnošću od svih uzroka i kardiovaskularnim mortalitetom. Saradnička meta-analiza populacijskih kohorti visokog rizika. Kidney Int. 2011;79:1341–1352. doi 10.1038/ki.2010.536
6. Jankowski J, Floege J, Fliser D, Bohm M, Marx N. Kardiovaskularna bolest u hroničnoj bubrežnoj bolesti: patofiziološki uvidi i terapijske opcije. Cirkulacija. 2021;143:1157–1172. doi: 10.1161/CIRCULATIONAHA.120.050686
7. Weber C, Noels H. Ateroskleroza: trenutna patogeneza i terapijske opcije. Nat Med. 2011;17:1410–1422. doi: 10.1038/nm.2538
8. Quillard T, Franck G, Mawson T, Folco E, Libby P. Mehanizmi erozije aterosklerotskih plakova. Curr Opin Lipidol. 2017;28:434–441. doi: 10.1097/MOL.0000000000000440
9. Betrui A, Martinez-Alonso M, Arcidiacono MV, Cannata-Andia J, Pascual J, Valdivielso JM, Fernández E; Istraživači iz NEFRONA studije. Prevalencija subkliničke ateromatoze i pridruženi faktori rizika kod hronične bolesti bubrega: studija NEFRONA. Transplantacija Nephrol Dial. 2014;29:1415–1422. doi 10.1093/ndt/gfu038
10. Valdivielso JM, Rodríguez-Puyol D, Pascual J, Barrios C, BermúdezLópez M, Sánchez-Niño MD, Pérez-Fernández M, Ortiz A. Ateroskleroza kod hronične bolesti bubrega: više, manje ili samo drugačije?. Arterioscler Thromb Vasc Biol. 2019;39:1938–1966. doi: 10.1161/ATVBAHA.119.312705
11. Gracia M, Betrui A, Martinez-Alonso M, Arroyo D, Abajo M, Fernández E, Valdivielso JM; NEFRONA Investigators. Prediktori supkliničke progresije ateromatoze tokom 2 godine kod pacijenata sa različitim stadijumima CKD. Clin J Am Soc Nephrol. 2016;11:287–296. doi: 10.2215/CJN.01240215
12. Anavekar NS, McMurray JJV, Velazquez EJ, Solomon SD, Kober L, Rouleau JL, White HD, Nordlander R, Maggioni A, Dickstein K, et al. Veza između bubrežne disfunkcije i kardiovaskularnih ishoda nakon infarkta miokarda. N Engl J Med. 2004;351:1285–1295. doi: 10.1056/NEJMoa041365
13. Myerburg RJ, Junttila MJ. Iznenadna srčana smrt uzrokovana koronarnom bolešću. Cirkulacija. 2012;125:1043–1052. doi: 10.1161/CIRCULATIONAHA.111.023846
14. Haider AW, Larson MG, Benjamin EJ, Levy D. Povećana masa lijeve komore i hipertrofija povezani su sa povećanim rizikom od iznenadne smrti. J Am Coll Cardiol. 1998;32:1454–1459. doi: 10.1016/s0735-1097(98)00407-0
15. Glassock RJ, Pecoits-Filho R, Barberato SH. Masa lijeve komore kod kronične bolesti bubrega i ESRD-a. Clin J Am Soc Nephrol. 2009;4:S79–S91. doi: 10.2215/CJN.04860709
16. Middleton R, Parfrey PS, Foley RN. Hipertrofija lijeve komore u bubrežnog bolesnika. J Am Soc Nephrol. 2001;12:1079–1084. doi 10.1681/ASN.V1251079
17. Gimbrone MA Jr, Garcia-Cardena G. Disfunkcija endotelnih ćelija i patobiologija ateroskleroze. Circ Res. 2016;118:620–636. doi: 10.1161/CIRCRESAHA.115.306301
18. Meza D, Musmacker B, Steadman E, Stransky T, Rubenstein DA, Yin W. Biomehanički odgovori endotelnih ćelija zavise i od napona na smicanje tečnosti i od vlačne deformacije. Cell Mol Bioeng. 2019;12:311–325. doi 10.1007/s12195-019-00585-0
19. Evrard SM, Lecce L, Michelis KC, Nomura-Kitabayashi A, Pandey G, Purushothaman KR, d'Escamard V, Li JR, Hadri L, Fujitani K, et al. Prelaz endotela u mezenhim čest je kod aterosklerotskih lezija i povezan je s nestabilnošću plaka. Nat Commun. 2016;7:11853. doi: 10.1038/ncomms11853
20. Chen PY, Qin L, Baeyens N, Li G, Afolabi T, Budatha M, Tellides G, Schwartz MA, Simons M. Prelazak endotela u mezenhim pokreće progresiju ateroskleroze. J Clin Invest. 2015;125:4514–4528. doi: 10.1172/JCI82719
21. Bostrom KI, Yao J, Guihard PJ, Blazquez-Medela AM, Yao Y. Endotelna mezenhimska tranzicija u kalcifikacije aterosklerotskih lezija. Ateroskleroza. 2016;253:124–127. doi 10.1016/j.aterosclerosis.2016.08.046
22. Souilhol C, Harmsen MC, Evans PC, Krenning G. Endotelno-mezenhimalna tranzicija u aterosklerozi. Cardiovasc Res. 2018;114:565–577. doi: 10.1093/cvr/cvx253
23. Mitchell JA, Ali F, Bailey L, Moreno L, Harrington LS. Uloga dušikovog oksida i prostaciklina kao vazoaktivnih hormona koje oslobađa endotel. Exp Physiol. 2008;93:141–147. doi: 10.1113/expphysiol.2007.038588
24. Johnston-Cox HA, Ravid K. Adenozin i krvni trombociti. Purinergic Signal. 2011;7:357–365. doi: 10.1007/s11302-011-9220-4
25. Born GV, Palinski W. Neobično visoke koncentracije sijaličnih kiselina na površini vaskularnog endotela. Br J Exp Pathol. 1985;66:543–549.
26. Reitsma S, Slaaf DW, Vink H, van Zandvoort MAMJ, oude Egbrink MGA. Endotelni glikokaliks: sastav, funkcije i vizualizacija. Pfugers Arch. 2007;454:345–359. doi 10.1007/s00424-007-0212-8
27. Yau JW, Teoh H, Verma S. Endotelna ćelijska kontrola tromboze. BMC Cardiovasc Disord. 2015;15:130. doi: 10.1186/s12872-015-0124-z
28. Döring Y, Soehnlein O, Weber C. Neutrofilne ekstracelularne zamke u aterosklerozi i aterotrombozi. Circ Res. 2017;120:736–743. doi: 10.1161/CIRCRESAHA.116.309692
29. Zieman SJ, Melenovsky V, Kass DA. Mehanizmi, patofiziologija i terapija ukočenosti arterija. Arterioscler Thromb Vasc Biol. 2005;25:932– 943. doi 10.1161/01.ATV.0000160548.78317.29
30. Flammer AJ, Anderson T, Celermajer DS, Creager MA, Deanfield J, Ganz P, Hamburg NM, Lüscher TF, Shechter M, Taddei S, et al. Procjena funkcije endotela: od istraživanja do kliničke prakse. Cirkulacija. 2012;126:753–767. doi: 10.1161/CIRCULATIONAHA.112.093245
31. Alexander Y, Osto E, Schmidt-Trucksass A, Shechter M, Trifunović D, Duncker DJ, Aboyans V, Back M, Badimon L, Cosentino F, et al. Funkcija endotela u kardiovaskularnoj medicini: konsenzus radnih grupa Evropskog kardiološkog društva za aterosklerozu i vaskularnu biologiju, bolesti aorte i perifernih krvnih žila, koronarnu patofiziologiju i mikrocirkulaciju i trombozu. Cardiovasc Res. 2021;117:29–42. doi: 10.1093/cvr/cvaa085
32. Lerman A, Zeiher AM. Funkcija endotela: srčani događaji. Cirkulacija. 2005;111:363–368. doi 10.1161/01.CIR.0000153339.27064.14
33. Schnabel RB, Schulz A, Wild PS, Sinning CR, Wilde S, Eleftheriadis M, Herkenhoff S, Zeller T, Lubos E, Lackner KJ, et al. Neinvazivno mjerenje vaskularne funkcije u zajednici: odnosi presjeka i poređenje metoda. Circ Cardiovasc Imaging. 2011;4:371–380. doi: 10.1161/CIRCIMAGING.110.961557
34. Perrault R, Omelchenko A, Taylor CG, Zahradka P. Uspostavljanje zamjenjivosti arterijske krutosti, ali ne i parametara funkcije endotela kod zdravih osoba. BMC Cardiovasc Disord. 2019;19:190. doi: 10.1186/s12872-019-1167-3
35. Bonarjee VVS. Ukočenost arterija: prognostički marker koronarne bolesti srca. Dostupne metode i klinička primjena. Front Cardiovasc Med. 2018;5:64. doi: 10.3389/fcvm.2018.00064
36. Van Beusecum JP, Barbaro NR, Smart CD, Patrick DM, Loperena R, Zhao S, de la Visitacion N, Ao M, Xiao L, Shibao CA, et al. Specifično zaustavljanje rasta-6 i Axl koordiniraju upalu i hipertenziju. Circ Res. 2021;129:975–991. doi: 10.1161/CIRCRESAHA.121.319643
37. Chen W, Van Beusecum JP, Xiao L, Patrick DM, Ao M, Zhao S, Lopez MG, Billings FT, Cavinato C, Caulk AW, et al. Uloga Axl-a u upali i oštećenju ciljnog organa zbog hipertenzivnog remodeliranja aorte. Am J Physiol Heart Circ Physiol. 2022;323:H917–H933. doi: 10.1152/ajpheart.00253.2022
38. Huang AL, Silver AE, Shvenke E, Schopfer DW, Jahangir E, Titas MA, Shpilman A, Menzoian JO, Watkins MT, Raffetto JD, et al. Prediktivna vrijednost reaktivne hiperemije za kardiovaskularne događaje kod pacijenata sa bolešću perifernih arterija koji su podvrgnuti vaskularnoj operaciji. Arterioscler Thromb Vasc Biol. 2007;27:2113–2119. doi: 10.1161/ATVBAHA.107.147322
39. Fischer D, Rossa S, Landmesser U, Spiekermann S, Engberding N, Hornig B, Drexler H. Endotelna disfunkcija kod pacijenata sa hroničnom srčanom insuficijencijom je nezavisno povezana sa povećanom incidencom hospitalizacije, transplantacije srca ili smrti. Eur Heart J. 2005;26:65–69. doi: 10.1093/eurheartj/ehi001
40. Meyer B, Mörtl D, Strecker K, Hülsmann M, Kulemann V, Neunteufl T, Pacher R, Berger R. Vazodilatacija posredovana protokom predviđa ishod kod pacijenata sa hroničnom srčanom insuficijencijom: poređenje sa B-tipom natriuretskog peptida. J Am Coll Cardiol. 2005;46:1011–1018. doi 10.1016/j.jacc.2005.04.060
41. Katz SD, Hryniewicz K, Hriljac I, Balidemaj K, Dimayuga C, Hudaihed A, Yasskiy A. Vaskularna endotelna disfunkcija i rizik od smrtnosti kod pacijenata sa hroničnom srčanom insuficijencijom. Cirkulacija. 2005;111:310–314. doi 10.1161/01.CIR.0000153349.77489.CF
42. Yeboah J, Crouse JR, Hsu FC, Burke GL, Herrington DM. Dilatacija posredovana brahijalnim protokom predviđa incidentne kardiovaskularne događaje kod starijih odraslih osoba: Studija kardiovaskularnog zdravlja. Cirkulacija. 2007;115:2390–2397. doi: 10.1161/CIRCULATIONAHA.106.678276
43. Yeboah J, Folsom AR, Burke GL, Johnson C, Polak JF, Post W, Lima JA, Crouse JR, Herrington DM. Prediktivna vrijednost dilatacije posredovane brahijalnim protokom za incidentne kardiovaskularne događaje u studiji zasnovanoj na populaciji: multietnička studija ateroskleroze. Cirkulacija. 2009;120:502–509. doi: 10.1161/CIRCULATIONAHA.109.864801
44. Lind L, Berglund L, Larsson A, Sundström J. Funkcija endotela u arterijama otpora i provodnika i 5-godišnji rizik od kardiovaskularnih bolesti. Cirkulacija. 2011;123:1545–1551. doi: 10.1161/CIRCULATIONAHA.110.984047
45. Vancheri F, Longo G, Vancheri S, Henein M. Koronarna mikrovaskularna disfunkcija. J Clin Med. 2020;9:2880. doi: 10.3390/jcm9092880
46. Del Buono MG, Montone RA, Camili M, Carbone S, Narula J, Lavie CJ, Niccoli G, Crea F. Koronarna mikrovaskularna disfunkcija kroz spektar kardiovaskularnih bolesti: JACC State-of-the-Art pregled. J Am Coll Cardiol. 2021;78:1352–1371. doi 10.1016/j.jacc.2021.07.042
47. Ehling J, Babickova J, Gremse F, Klinkhammer BM, Baetke S, Knuechel R, Kiessling F, Floege J, Lammers T, Boor P. Kvantitativna mikro-kompjuterska tomografija vaskularne disfunkcije u progresivnim bolestima bubrega. J Am Soc Nephrol. 2016;27:520–532. doi 10.1681/ASN.2015020204
48. Prommer HU, Maurer J, von Websky K, Freise C, Sommer K, Nasser H, Samapati R, Reglin B, Guimaraes P, Pries AR, et al. Hronična bolest bubrega izaziva sistemsku mikroangiopatiju, tkivnu hipoksiju i disfunkcionalnu angiogenezu. Sci Rep. 2018;8:5317. doi: 10.1038/s41598-018-23663-1
49. Querfeld U, Mak RH, Pries AR. Mikrovaskularna bolest kod kronične bolesti bubrega: osnova ledenog brega u kardiovaskularnom komorbiditetu. Clin Sci (Lond). 2020;134:1333–1356. doi 10.1042/CS20200279
50. Matsuzawa Y, Sugiyama S, Sugamura K, Nozaki T, Ohba K, Konishi M, Matsubara J, Sumida H, Kaikita K, Kojima S, et al. Digitalna procjena funkcije endotela i ishemijske bolesti srca kod žena. J Am Coll Cardiol. 2010;55:1688–1696. doi 10.1016/j.jacc.2009.10.073
51. Tamo JD, Al-Fiadh AH, Amirul Islam FM, Patel SK, Burrell LM, Wong TY, Farouque O. Oštećena mikrovaskularna funkcija retine predviđa dugoročne neželjene događaje kod pacijenata sa kardiovaskularnim bolestima. Cardiovasc Res. 2021;117:1949–1957. doi: 10.1093/cvr/cvaa245
52. Fujisue K, Sugiyama S, Matsuzawa Y, Akiyama E, Sugamura K, Matsubara J, Kurokawa H, Maeda H, Hirata Y, Kusaka H, et al. Prognostički značaj periferne mikrovaskularne endotelne disfunkcije kod srčane insuficijencije sa smanjenom ejekcijskom frakcijom lijeve komore. Circ J. 2015;79:2623–2631. doi: 10.1253/circa.CJ-15-0671
53. Maréchaux S, Samson R, van Belle E, Breyne J, de Monte J, Dédrie C, Chebai N, Menet A, Banfi C, Bouabdallaoui N, et al. Vaskularna i mikrovaskularna endotelna funkcija kod zatajenja srca sa očuvanom ejekcionom frakcijom. J Card Fail. 2016;22:3–11. doi: 10.1016/j.cardfail.2015.09.003
54. Mohammed SF, Hussain S, Mirzoyev SA, Edwards WD, Maleszewski JJ, Redfield MM. Koronarna mikrovaskularna refakcija i fibroza miokarda kod zatajenja srca sa očuvanom ejekcionom frakcijom. Cirkulacija. 2015;131:550– 559. doi: 10.1161/CIRCULATIONAHA.114.009625
55. Franssen C, Chen S, Unger A, Korkmaz HI, De Keulenaer GW, Tschöpe C, Leite-Moreira AF, Musters R, Niessen HWM, Linke WA, et al. Miokardna mikrovaskularna inflamatorna endotelna aktivacija kod zatajenja srca sa očuvanom ejekcionom frakcijom. JACC Heart Fail. 2016;4:312–324. doi: 10.1016/j.jchf.2015.10.007
56. D'Amario D, Migliaro S, Borovac JA, Restivo A, Vergallo R, Galli M, Leone AM, Montone RA, Niccoli G, Aspromonte N, et al. Mikrovaskularna disfunkcija kod zatajenja srca sa očuvanom ejekcionom frakcijom. Front Physiol. 2019;10:1347. doi: 10.3389/Phys.2019.01347
57. Cornuault L, Rouault P, Duplàa C, Couffinhal T, Renault MA. Endotelna disfunkcija kod zatajenja srca sa očuvanom ejekcionom frakcijom: koji su eksperimentalni dokazi? Front Physiol. 2022;13:906272. doi: 10.3389/Phys.2022.906272
58. Harvey A, Montezano AC, Alves Lopes R, Rios F, Touyz RM. Vaskularna fibroza u starenju i hipertenziji: molekularni mehanizmi i kliničke implikacije. Can J Cardiol. 2016;32:659–668. doi 10.1016/j.cjca.2016.02.070
Constance CFMJ Baaten, Sonja Vondenhoff, Heidi Noels






