MikroRNA u razvoju i bolesti bubrega Ⅰ
Apr 30, 2024
Uvod
MikroRNA (miRNA) su endogene male nekodirajuće RNK koje su obično dugačke 19-22 nukleotida. Ljudski genom sadrži 1917 označenih prekursora ukosnica i 2654 zrele miRNA (1), koje regulišu preko 60% gena koji kodiraju ljudski protein (2). MiRNA regulišu ekspresiju gena na posttranskripcijskom nivou, kako kroz translacijsku represiju tako i kroz destabilizaciju mRNA (3-5). Od otkrića funkcije prve identificirane miRNA, za koju se pokazalo da regulira odluke o staničnoj liniji kod nematode Caenorhabditis elegans, 1993. (6, 7), pokazalo se da miRNA moduliraju različite biološke procese, uključujućimorfogeneza bubrega. Disregulacija ekspresije miRNAometa rani razvoj bubregai uključen je u patogenezu razvojabolesti bubrega. U ovom pregledu sumiramo trenutno znanje o biogenezi, funkciji i ciljanju miRNA. Zatim se fokusiramo na ulogu miRNA u morfogenezi bubrega irazvojne bolesti bubrega, uključujućikongenitalne anomalijeof thebubrega i urinarnog trakta(CAKUT) iWilmsov tumor. Dodatna zanimljiva područja istraživanja, uključujući ulogu miR NA u nizu drugih bubrežnih bolesti, kao što su akutna ozljeda bubrega (8-10), policistična bolest bubrega (11) i transplantacija bubrega (10), opširno su obrađena u druge nedavne kritike. Konačno, zaključujemo raspravom o korisnosti miRNA kao potencijalno novih biomarkera i terapeutskih agenasa.

KOLIKO JE TREBA DA CISTANCHE proradi KOD BOLESNIKA BUBREGA?
biogeneza i funkcija miRNA
Biogeneza miRNA počinje u jezgru, gdje RNA polimeraza II transkribuje gene koji kodiraju miRNA u zatvorene i poliadenilirane transkripte ukosnice, nazvane primarne miRNA ili pri-miRNA (Slika 1) (12, 13). U zavisnosti od njihove genomske lokacije, geni koji kodiraju miRNA mogu se klasifikovati kao intrageni (locirani unutar introna gena domaćina; ref. 14) ili intergeni (transkribovani nezavisno od gena domaćina i imaju svoje transkripcione regulatorne elemente; ref. 15). Osim toga, neke miRNA postoje u klasterima i transkribiraju se kao policistronski transkripti (16).
Nakon transkripcije, pri-miRNA se cijepa enzimom DROSHA sličnom ribonukleazi III zajedno sa podjedinicom mikroprocesorskog kompleksa DGRC8 u 70-nukleotidnu strukturu ukosnice, nazvanu pre-miRNA (17-20). Nuklearni protein koji se veže za eksportin 5/GTP izvozi pre-miRNA u citoplazmu (21, 22), gdje pre-miRNA prolazi kroz cepanje svoje terminalne petlje pomoću RNase III DICER i TRBP (ili TARBP2) kako bi se proizvela { {14}}dupleks nukleotida miRNA koji se sastoji od vodiča i suvozača (miRNA:miRNA*, respektivno). U sljedećem koraku, miRNA dupleks se stavlja na protein argonauta (AGO) kako bi se formirao RISC (23). Nakon odabira i odmotavanja lanca, putnički lanac se oslobađa i degradira (24), dok lanac vodiča ostaje u RISC-u i pokreće prepoznavanje ciljane mRNA kroz Watson-Crick bazno uparivanje
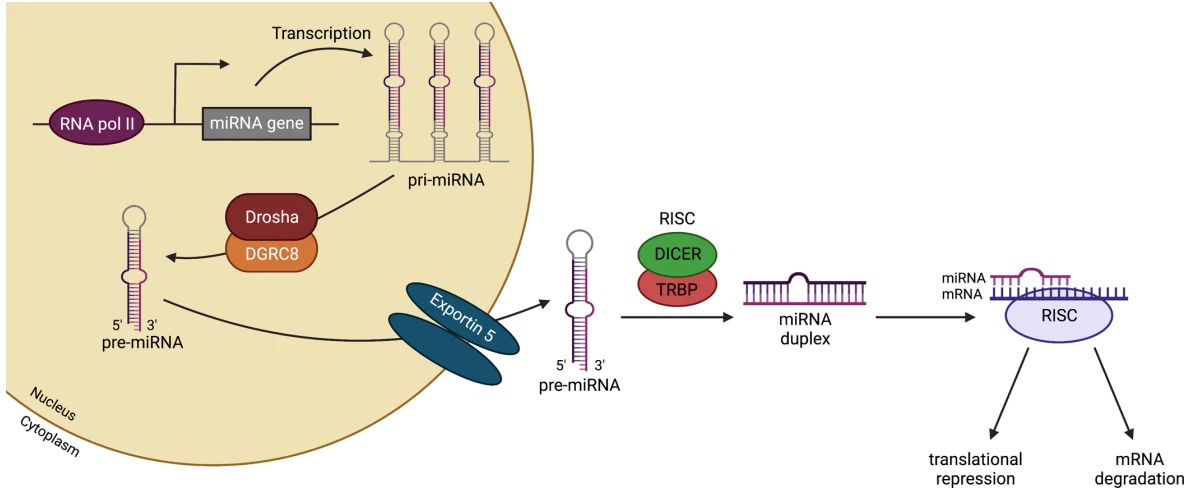
Slika 1. Biogeneza miRNA. Geni koji kodiraju miRNA se transkribiraju pomoću RNA polimeraze II u primarnu miRNA (pri-miRNA). Zatim, kompleks formiran od RNA-vezujućeg proteina DGRC8 i enzima RNase III Drosha cijepa pri-miRNA, stvarajući prekursor miRNA (pre-miRNA), koja se izvozi u citoplazmu putem exportina 5. Jednom u citoplazmi, Dicer /TRBP kompleks cijepa pre-miRNA, oslobađajući zrelu miRNA. Konačno, zrela miRNA se učitava u RISC, pokrećući prepoznavanje ciljne mRNA kroz Watson-Crick uparivanje baza, što kulminira utišavanjem gena kroz translacijsku represiju ili degradaciju mRNA. DGRC8, DiGeorgeov sindrom kritična regija 8; RISC, RNA-inducirani kompleks za utišavanje; TRBP, TAR RNA-vezujući protein. Kreirano sa BioRender.com.

Većina studija pokazuje da domen na 5′ kraju miRNA (nazvan sekvenca sjemena, koja se proteže od nukleotidnih pozicija 2 do 7) stupa u interakciju sa specifičnim regionom na 3′ neprevedenom regionu (3′UTR) njihove ciljne mRNA kako bi inducirao translaciona represija i/ili mrtvilacija i raspad mRNA (3–5). Međutim, mjesta vezivanja miRNA također su identificirana u drugim regijama, uključujući 5′UTR (25, 26), kodirajuće sekvence (27) i promotore gena (28-30). Iako su miRNA prvenstveno povezane sa represijom gena, posttranskripcijska regulacija miRNA također se može dogoditi pod određenim okolnostima (28, 31-33).

Postoji nekoliko jedinstvenih karakteristika povezanih sa regulacijom gena posredovanom miRNA (34, 35). Prvo, jedna miRNA može ciljati i potisnuti stotine mRNA, iako tipično u relativno blagom stepenu za svaku metu. Stoga se smatra da miRNA funkcioniraju za fino podešavanje ekspresije gena. Međutim, kako svaka mRNA može obuhvatiti više mjesta vezivanja za iste ili različite miRNA, rezultirajući kombinovani efekat je snažniji (36-38). Štaviše, više komponenti unutar datog signalnog puta mogu se modulirati pojedinačnim miRNA ili miRNA klasterima (39, 40). Drugo, represija posredovana miRNA javlja se relativno brzo, jer miRNA blokiraju sintezu proteina na nivou ribosoma (41). Treće, miRNA se mogu koncentrirati u specifične subcelularne kompartmente kako bi regulisali translaciju proteina specifičnog za mjesto (42, 43). Konačno, mala podskupina miRNA dominira u ukupnom miRNA u različitim tipovima ćelija, što sugerira da one mogu funkcionirati kao glavne miRNA (44). U skladu sa ovom idejom, čini se da nekoliko najzastupljenijih miRNA čini većinu posttranskripcione regulacije posredovane AGO proteinima u mnogim tipovima ćelija (44, 45). Na primjer, u besmrtnoj ljudskoj embrionalnoj ćelijskoj liniji bubrega (HEK293T), miRNA koje su bile eksprimirane ispod 100-1000 čitanja na milion nisu pokazale supresivnu aktivnost korištenjem biblioteke miRNA senzora visoke propusnosti (45).
Biogeneza miRNA je pod strogom prostornom i vremenskom kontrolom kako bi se osigurala odgovarajuća ekspresija miRNA kao odgovor na različite ćelijske signale. Regulacija biogeneze miRNA događa se na više nivoa, uključujući vezivanje faktora transkripcije za pojačivače i/ili promotore miRNA gena, DROSHA obradu pri-miRNA, DICER obradu pre-miRNA, metilaciju RNK, uređivanje prekursora miRNA, adenilaciju, uridilaciju, RNK raspad i mnogi drugi mehanizmi. Za detaljan pregled, pogledajte Ha i Kim (46). Nedavno su se pojavili i super-pojačivači kao nova klasa regulatornih elemenata koji kontrolišu biogenezu miRNA tako što poboljšavaju transkripciju i DROSHA/DGCR8-posredovanu pri-miRNA obradu. U kombinaciji sa širokim H3K4me3 potpisom, aktivnost super-pojačivača oblikuje obrasce i funkcije miRNA specifične za tkivo (47).

