Udio koncentrata u ishrani muznih krava u ranoj laktaciji ima suprotan učinak na cirkulirajuće leukocitne globalne transkriptomske profile, zdravlje i plodnost prema paritetu
Dec 26, 2023
sažetak:Funkcionalnost cirkulirajućih leukocita kod mliječnih krava je potisnuta nakon teljenja, uz negativan energetski bilans kao faktor rizika. Transkriptomski profili leukocita upoređivani su odvojeno kod 44 višeporodnih (MP) i 18 prvorotkinja (PP) holštajn-frizijskih krava koje su dobile hranu koja se razlikovala u proporciji koncentrata kako bi se ispitalo da li se imunološka disfunkcija može ublažiti odgovarajućom ishranom. Nakon teljenja, kravama je ponuđen ili (1) niski koncentrat (LC); (2) srednje koncentrovane (MC) ili (3) visokokoncentrirane (HC) dijete sa proporcijama koncentrata i silaže trave od 30%:70%, 50%:50% i 70%:30%, respektivno. Prikupljeni podaci o fenotipu krava uključivali su cirkulirajuće metabolite, prinos mlijeka i evidenciju o zdravlju i plodnosti. Urađeno je RNK sekvenciranje cirkulirajućih leukocita na 14 dana u mlijeku. HC dijeta je poboljšala energetski balans u obe starosne grupe. Bilo je više različito eksprimiranih gena u PP nego u MP krava (460 naspram 173, HC vs. LC poređenje) uz nekoliko preklapanja. Krave MP na LC ishrani su pokazale pojačanu regulaciju kaskade komplementa i koagulacije i urođene imunološke odbrambene mehanizme protiv patogena i imale su trend više slučajeva mastitisa i slabije plodnosti. Nasuprot tome, PP krave na HC ishrani su pokazale veći imunološki odgovor na osnovu ekspresije gena i fenotipskih podataka i dužeg intervala od teljenja do začeća. Stoga su leukociti krava MP i PP različito reagirali na ishranu između starosti, opskrbe nutrijentima i imuniteta, što je utjecalo na njihovo zdravlje i kasniju plodnost.

cistanche koristi za muškarce - jača imuni sistem
Kliknite ovdje za pregled proizvoda Cistanche Enhance Immunity
【Zatražite više】 Email:cindy.xue@wecistanche.com / Whats App: 0086 18599088692 / Wechat: 18599088692
Ključne riječi:postporođajna imunosupresija; urođeni imunitet; metabolizam; leukociti; dijete za laktaciju; transkriptom; reprodukcija; krave
1. Uvod
Rani postpartum, mliječne krave karakterizira imunosupresija koja utječe na urođeni i adaptivni imunitet, uključujući i ćelijski posredovan i humoralni imunitet. Cirkulirajući leukociti se regrutuju u tkiva kao što su mlečna žlezda i endometrijum tokom upale. Prethodne studije su, međutim, pokazale smanjenje i broja leukocita i njihovog funkcionalnog kapaciteta tokom peripartalnog perioda [1,2]. Prijavljeni efekti uključuju oštećenu fagocitozu i aktivnost oksidativnog pucanja [3–5], smanjenu reakciju cirkulirajućih T-ćelija na mitogene agense i smanjenu proizvodnju imunoglobulina od strane B-ćelija [6,7]. Uzroci su višefaktorni, ali izgleda da su povezani sa podjelom nutrijenata u korist proizvodnje mlijeka na početku laktacije, što ugrožava imunološku funkciju [8-10]. Leukociti zahtijevaju adekvatnu opskrbu glukozom, raznim masnim kiselinama i kolesterolom ili oksisterolima za njihovo održavanje i funkcionalnost [8,11,12]. Dostupna opskrba hranjivim tvarima je, međutim, prioritetna za mliječnu žlijezdu nakon teljenja, zahtijevajući približno 25% više metabolične energije i proteina nego što se obezbjeđuje unosom hrane [8,13,14]. Osim toga, porođaj karakteriziraju upalni procesi povezani s promjenama u lučenju različitih prostaglandina, steroida i citokina i mogućim ozljedama tijekom samog procesa porođaja [15–17]. Upalni odgovori na teljenje i metaboliti koji se oslobađaju tokom mobilizacije tkiva imaju snažne anoreksične efekte, dodatno smanjujući unos i pogoršavajući negativnu ravnotežu energije (NEB) [18]. Kada unos hrane ne može zadovoljiti rastuću potražnju za energijom, krave ulaze u period NEB, pri čemu neke osobe postaju metabolički neuravnotežene [19–21]. NEB je povezan sa insulinskom rezistencijom, smanjenom ekspresijom jetrenog hormona rasta (GH) receptora i nižom sintezom IGF-1 u jetri [22,23]. Odvajanje GH s inzulinom kod krava nakon porođaja je adaptacija koja daje prioritet opskrbi glukozom u tkiva kao što su epitelne stanice mliječne žlijezde, u kojima je uzimanje neovisno o inzulinu [8]. U ovoj situaciji, konkurencija za snabdijevanje energijom između mliječne žlijezde i imunološkog sistema je neizbježna jer se oba oslanjaju na iste esencijalne supstrate i oba su glavni potrošači energije. Kvidera i dr. [24] su pokazali da je za aktivaciju punog imunološkog odgovora kod krava potrebno 2,5 do 3,1 kg glukoze dnevno. Ovo je slično procijenjenoj potrebi od 2,7 kg/d glukoze koju preuzimaju epitelne ćelije dojke za proizvodnju mlijeka od 40 kg/d [8].
Mobilizacija tkiva je također povezana s povećanjem cirkulirajućih koncentracija neesterificiranih masnih kiselina (NEFA), beta-hidroksibutirata (BHB) i smanjenog IGF-1, što sve doprinosi imunološkoj disfunkciji [5,9,10,20 ]. Na primjer, naša nedavna studija je ilustrovala da je adhezija leukocita između stanica bila inhibirana kada je koncentracija NEFA premašila 750 µM [25]. Iako je mobilizacija tkiva normalna adaptacija sisara za podršku laktaciji, mnoge studije su pokazale da teški NEB ima veliki utjecaj na kasniju sposobnost krave da pravovremeno zatrudni [26]. Ovo može biti uzrokovano raznim faktorima uključujući kašnjenje u obnavljanju odgovarajućeg okruženja materice [2]; produženi period anovulacije [27], loša intrafolikularna sredina [28] i narušen kvalitet oocita [29]. Mliječne junice se općenito tele na oko 90% svoje zrele tjelesne težine [30]. Naša prethodna studija je pokazala da su krave prvorotkinje (PP) imale višu koncentraciju inzulina, IGF-1 i leptina u cirkulaciji, niže koncentracije metabolita u krvi (BHB, NEFAs i urea) i veće koncentracije glukoze od višerodnih (MP ) krave najmanje 7 sedmica nakon teljenja [31,32]. Ovo ukazuje da postoji manje odvajanje somatotrofne ose u ranoj laktaciji kod PP krava u odnosu na krave MP, što je povezano sa slabijim prioritetom hranljivih materija u mlečnoj žlezdi, što omogućava nastavak rasta. Profili ekspresije gena u cirkulirajućim leukocitima takođe se razlikuju između PP i MP krava tokom rane laktacije [33].

cistanche tubulosa-poboljšava imuni sistem
Optimizacija upravljanja ishranom tokom sušnog perioda može povećati unos suve materije (DMI), smanjiti učestalost periporođajnih bolesti i poboljšati plodnost [34]. Postoje opće smjernice o tome kako smanjiti rizik od bolesti povezan s hranjenjem i upravljanjem [35]. Međutim, postoji malo dostupnih informacija o prehrambenim formulacijama za pojedinačnu kravu u metaboličkom disbalansu tokom postporođajnog perioda koji može poboljšati imunološku funkciju, smanjiti učestalost bolesti i poboljšati naknadni reproduktivni učinak. Formuliranje dijete s visokim potencijalom unosa nutrijenata je praktičan pristup [36]. U ovoj studiji, kravama u ranoj laktaciji ponuđena je niska (LC), srednje (MC) ili visokokoncentrirana (HC) ishrana zasnovana na proporcijama koncentrata u travnatoj silaži, i efektima na metaboličko zdravlje i bolest, i sistemski imunitet ( procjenom globalnih profila ekspresije gena cirkulirajućih leukocita). Podaci za krave PP i MP analizirani su odvojeno kako bi se izbjegao bilo kakav zbunjujući efekat koji proizlazi iz pariteta. Naša hipoteza je bila da će dijeta visoke koncentracije poboljšati imunološku funkciju i doprinijeti plodnosti.

cistanche tubulosa-poboljšava imuni sistem
2. Rezultati
2.1. Utjecaj dijeta na unos suhe materije, prinos mlijeka, energetski balans i metabolite u krvi
Parametri mlijeka, tjelesna težina (BW), DMI, rezultat tjelesne kondicije (BCS), energetska ravnoteža (EBAL) i metaboliti u krvi za krave MP i PP nakon oko 14 dana u mlijeku (DIM) su sažeti u Tabeli 1. DMI za MP krave su se značajno razlikovale između tri grupe ishrane sa redoslijedom HC > MC > LC (p < 0.01–0.0{{11 }}1). Prinos mlijeka kod MP krava koje su primale HC hranu bio je značajno veći od onih koje su primale LC hranu (p < 0.05). Razlika u energetski korigovanoj mliječnosti (ECM) između LC i HC grupa je bila značajna (p < 0.05), sa srednjim vrijednostima u MC grupi. Vrijednosti EBAL-a u sve tri MP grupe bile su negativne, ali su one kod MC i HC krava bile značajno bolje (manje negativne) nego u LC krava (p < 0,01). Cirkulirajuće koncentracije glukoze (p < 0,01) i IGF-1 (p < 0,001) kod HC krava bile su značajno veće nego kod LC krava. Krave MP koje su nudile HC ishranu takođe su proizvele manje cirkulišuće uree (p < 0,001), BHB (p < 0,05) i NEFA od onih koje su nudile LC ishrane sa koncentracijama LC > MC > HC, iako su razlike u koncentracijama NEFA između grupa u ishrani nisu bili statistički značajni.
Tabela 1. Ukupni unos suhe tvari, parametri mlijeka, tjelesna težina, energetska ravnoteža, rezultat tjelesne kondicije i metaboliti u krvi oko 14 dana nakon teljenja, analizirano prema paritetu i ishrani 1,2

Kod PP krava, one koje su primale MC ili HC ishranu imale su veći DMI od onih koje su primale LC hranu (p < {{0}}.01). Prinosi mlijeka se nisu značajno razlikovali. EBAL je bio pozitivan kod krava kojima je ponuđena MC ili HC ishrana, dok je za one kojima je ponuđena LC prehrana bio negativan. Razlike u EBAL-u između HC i LC PP krava bile su značajne (p < 0,05). Od izmjerenih metabolita, samo su se koncentracije ureje razlikovale između grupa, koje su bile niže kod krava HC (LC > MC > HC, p < 0,001 za LC u odnosu na HC ili MC).
2.2. Utjecaj dijeta na inflamatorne parametre
Učinci prehrane na inflamatorne parametre mjerene u materici i mliječnoj žlijezdi prikazani su u Tabeli 2. Kod krava PP, omjer polimorfonuklearnih leukocita i epitelnih ćelija materice (PMN: UEC) prikupljenih iz materice pomoću citočetkice bio je značajno veći za krave na HC u poređenju sa LC ishranom (p < 0.05). Kod krava MP, trend je bio u istom pravcu, sa LC < MC < HC, ali nije postigao statističku značajnost. U mlijeku, MP krave na LC hrani imale su značajno veći SCC od onih na MC ili HC hrani (p < 0.05), dok je kod PP krava neznatan trend bio u suprotnom smjeru. . Koncentracije N-acetil- -d-glukozaminidaze (NAGase) i laktat dehidrogenaze (LDH) u mlijeku, enzima mlijeka koji ukazuju na mastitis, pratili su iste opšte trendove kao i vrijednosti SCC, ali nisu bile značajne razlike. Ovi rezultati su potkrijepljeni zdravstvenim kartonima. Krave MP na HC ishrani nisu imale nijedan slučaj mastitisa (0/15), dok je kod 4/14 (28,6%) krava na LC ishrani dijagnosticiran klinički mastitis unutar 16 dana od teljenja. Trend je ponovo bio u suprotnom smjeru za PP krave sa jednom od šest (16,7%) na LC ishrani sa kliničkim mastitisom u poređenju sa jednim slučajem kliničkog i dva slučaja subkliničkog mastitisa na HC ishrani (50%).
Tabela 2. Inflamatorni parametri oko 14 dana nakon teljenja prema paritetu i ishrani 1,2.

2.3. Podaci o plodnosti
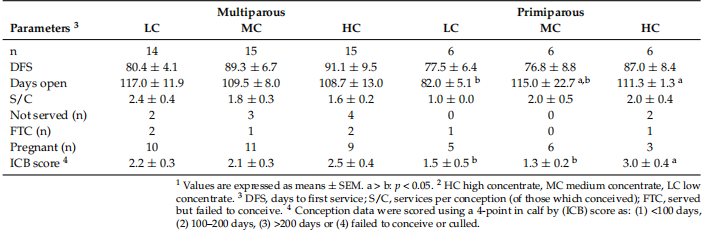
Detalji podataka o plodnosti dati su u tabeli 3. Za krave MP krave, onima na LC ishrani je trebalo nešto duže da začete i zahtijevale su više usluga po začeću nego krave HC (2,4 ± 0.42 naspram 1,6 ± 0.23), iako veći broj HC krava ili nije opslužen (odluka uprave) ili uopće nisu začeti (6{{10}}.0% vs 71,4%). Međutim, nijedna od ovih razlika nije bila značajna. Za PP krave, bilo je obrnuto, sa LC kravama najkraći interval do začeća od 29 dana (p < {{20}}.05), pri čemu je pet od šest životinja začeto svoju prvu uslugu . Nasuprot tome, polovina grupe HC ili nije bila uslužena (n=2) ili nije uspjela zatrudnjeti (n=1), a tri koje su zatrudnjele zahtijevale su 2,0 ± 0,41 usluge po začeću. Ovo je dovelo do toga da je HC grupa imala značajno veći skor "in calf by" (ICB) (p < 0,05).
Tabela 3. Podaci o plodnosti prema paritetu i ishrani 1,2
2.4. Transkriptomski profili leukocita kod krava koje su nudile različite proporcije koncentrata
Referentni goveđi genom ARS-UCD 1.2 koji je dao RefSeq (https://www.ncbi.nlm.nih.gov/assembly, pristupljeno 1. maja 2022.) sadrži 35.158 gena, od kojih je 19.001 gen leukocita bio kvantificiran kada je sekvenciranje glasilo u FASTQ fajlovima su mapirani na njega. Vulkanski grafikoni koji pokazuju profile ekspresije i kod MP i PP krava koje su primale tri različite dijete su predstavljene na slici 1. Kod krava MP, bilo je 173 različito eksprimiranih gena (DEG) u poređenju između HC i LC, 126 između MC i LC krava. LC i 68 za HC naspram MC (dodatni fajl S1A–C). Venov dijagram je pokazao da nijedan gen (uobičajeni DEG) nije bio značajan u sva tri poređenja ishrane (slika 2A). Kod PP krava, bilo je 460 DEG u poređenju HC u odnosu na LC, 178 između MC i LC i 128 između HC i MC (dodatni fajl S2A-C). Samo jedan zajednički gen (DCN, fold change (FC)=-7.3) bio je značajan u sva tri poređenja ishrane (slika 2B). Ovo kodira dekorin, protein koji igra ulogu u sklapanju kolagenih vlakana. Sve u svemu, bilo je primjetno da je veći broj DEG-ova pronađen u ishrani ekspresije gena leukocita u PP nego kod krava MP uprkos manjim veličinama grupa, pri čemu je većina ovih gena povećana na HC ishrani. Štaviše, bilo je malo preklapanja u genima identifikovanim između različitih starosnih grupa, kao što je ilustrovano u Venovim dijagramima na slici 3. Ovo sugeriše da su ishrane imale različite efekte na transkriptom leukocita kod PP i MP krava. U obe starosne grupe, najveće razlike su utvrđene između krava koje su ponuđene na LC vs. HC ishrani, pa smo se u narednim analizama fokusirali na ovo poređenje.


Slika 1. Vulkanski grafikoni pokazuju profile ekspresije i kod MP i PP krava koje su dobile tri različite dijete. (A) MP krave HC vs. LC, (B) MP krave HC vs. MC, (C) MP krave MC vs. LC, (D) PP HC naspram LC, (E) PP HC vs. MC i (F ) PP MC vs. LC. HC: visoki koncentrat (n=6 kod PP krava i n=14 kod MP krava), MC: srednji koncentrat (n=5 kod PP krava i n=15 kod MP krava ), i LC: niski koncentrat (n=6 kod PP krava i n=14 kod MP krava). Promjene preklopa su log2-transformirane. Zelene tačke označavaju niže regulisane gene sa p (BH) < 0.05 i višestruke promjene manje od ili jednake -1,5, a crvene tačke označavaju povećane gene sa p (BH) < {{ 16}}.05 i fold promjene veće ili jednako 1,5. Narandžaste tačke označavaju gene sa p (BH) < 0,05 ali apsolutnim promjenama nagiba < 1,5.

Slika 2. Vennovi dijagrami koji pokazuju različito eksprimirane gene od strane cirkulirajućih leukocita između tri grupe ishrane kod (A) višeporodnih (MP) krava i (B) prvorotki (PP) krava. HC: visoki koncentrat (n=6 kod PP krava i n=14 kod MP krava), MC: srednji koncentrat (n=5 kod PP krava i n=15 kod MP krava ) i LC: niski koncentrat (n=6 kod PP krava i n=14 kod MP krava).

Slika 3. Vennovi dijagrami koji pokazuju različito eksprimirane gene cirkulirajućih leukocita između krava PP i MP u poređenju (A) visokog koncentrata (HC) sa niskim koncentratom (LC); (B) HC sa srednjim koncentratom (MC) i (C) MC sa LC. HC: n=6 kod PP krava i n=14 kod MP krava, MC: n=5 kod PP krava i n=15 kod MP krava i LC: n {{5 }} kod PP krava i n=14 kod MP krava
2.5. Poređenje profila ekspresije gena leukocita između višerodnih krava koje primaju hranu s visokim ili niskim koncentratom
20 najboljih reguliranih i niže reguliranih DEG-ova rangiranih prema vrijednostima p (prilagođeno za BH) kod krava MP hranjenih HC u poređenju s onima koje su hranjene LC ishranom date su u Dodatnom fajlu S1D, E. Među povišenim DEG-ovima, većina je bila uključena u GO funkcije procesa imunološkog sistema, metabolizma i odgovora na stimulans, pri čemu mnogi kodirajući proteini imaju višestruke uloge. Na primjer, ALAS2 (kodira 50 -aminolevulinat sintazu 2) ima ulogu u metaboličkom procesu, odgovoru na stimulans i razvojnom procesu. COL1A1 (kolagen tip I alfa 1 lanac) i DAB2 su uključeni u metabolizam, odgovor na stimulans, višećelijski organizam, lokomociju i razvoj. Prvih 20 gena sa smanjenom regulacijom ilustruju jasnu temu promjena u imunitetu sa 14 povezanih DEG-ova. Od njih, DMTB1, FGA, FGB i TF kodiraju antimikrobne peptide, ALB i TF kodiraju negativne proteine akutne faze (APP), a FGA i FGG kodiraju pozitivne APP. Osam gena igra ulogu u metabolizmu, a 10 je uključeno u odgovor na stimulans.

cistanche biljka koja povećava imuni sistem
DEG leukocita dobijeni iz poređenja HC sa LC grupom su zatim podvrgnuti analizi obogaćivanja GO. 76 povišenih DEG-ova značajno je obogaćeno sa 208 funkcija, od kojih je 20 najboljih na osnovu rezultata obogaćivanja prikazano na slici 4A. Oni su bili povezani sa različitim aspektima ćelijske funkcije, sa vezivanjem faktora rasta koji je izveden iz trombocita na vrhu. Mnoge funkcije bile su vezane za metabolizam proteina i aminokiselina (uključujući APLP1, COL1A1, COL1A2, COL3A1, HTR1B i P2RY12 u većini njih), biomineralizaciju i obradu kolagena (uključujući COL1A1, COL1A2, SPP1 i TUFT1) i staničnu komunikaciju. Nasuprot tome, glavne funkcije 97 DEG-ova sniženom regulacijom imale su jasnu temu različitih imunoloških odbrambenih procesa (Slika 4B) koji su uglavnom bili povezani sa 20 DEG-a. Od njih, FGA (pozitivan APP) je smanjen 85- puta u poređenju HC i LC. Alat GO pretraživača sažeo je biološke funkcije i gore i dole regulisanih DEG-ova u osam značajnih kategorija (tabela 4). Osim biomineralizacije, sve ostale biološke funkcije, posebno one povezane sa imunološkom odbranom, bile su pretežno povezane sa smanjenim DEG-ovima.

Slika 4. Top 20 GO funkcija povezanih sa DEG-ovima izvedenim iz HC i LC poređenja. (A) MP naviše regulisani DEG, (B) MP niže regulisani DEG, (C) PP regulisani DEG naviše i (D) PP niže regulisani DEG.
Tabela 4. Sažetak glavnih funkcija obogaćivanja GO DEG-ova leukocita u poređenju između višerodnih krava koje su u ranoj laktaciji primale hranu s visokim (n=14) i niskim (n=14) koncentratom.

Tabela 4. Nast.

Kombinovani gore i dole regulisani DEG (n=173) su značajno obogaćeni sa 23 KEGG puta koji su se uglavnom odnosili na različite imunološke i metaboličke procese (Tabela 5). Kaskade komplementa i koagulacije bile su na vrhu sa osam smanjenih DEG-ova (CFB, FGA, FGB, FGG, KNG1, PROC, SERPINA1 i VTN). Upalni put NOD-like signalizacije bio je povezan sa šest DEG-ova (IFNB1, MAPK10, OAS1X, OAS1Y, OAS1Z i OAS2), od kojih su svi osim MAPK10 bili smanjeni. Put varenja i apsorpcije proteina sadržavao je šest DEG, od kojih su tri (COL1A1, COL1A2 i COL3A1) bile povišene, a tri niže (CELA2A, COL5A3 i ELN). Pet sniženih DEG-a bilo je uključeno u signalni put receptora aktiviranih proliferatorom peroksizoma (PPARs) (APOA2, APOC3, FABP1, HMGCS2 i PCK1). Putevi interakcije ekstracelularnog matriksa i receptora, fokalne adhezije i sfingolipidne signalizacije uključeni su u održavanje strukture ćelije i tkiva.
Tabela 5. Značajni putevi identificirani obogaćivanjem KEGG puteva povezani s različito eksprimiranim genima leukocita u višerodnih krava nudili su visokokoncentratnu ishranu (n=14) u poređenju sa onima koji su nudili ishranu sa niskim sadržajem (n=14).

2.6. Poređenje obrazaca ekspresije gena leukocita između krava prvorotki koje su primale hranu s visokim ili niskim koncentratom
Najboljih 20 cirkulirajućih DEG-ova leukocita u PP kravama koje su hranjene HC u poređenju sa LC dijetama su navedene u Dodatnoj datoteci S2D, E. Imuni i metabolički procesi su dominirali biološkim funkcijama najviše reguliranih DEG-a, koji sadrže 11 i 12 DEG respektivno. Među njima, ACSL6, MMP9 i SLC11A1 su uključeni u proliferaciju leukocita, a ACSL6, ADGRG3, COL1A2, DUSP1, HCK, MMP9 i PADI4 u procesu razvoja. SLC40A1 je glavni transporter gvožđa koji igra ključnu ulogu u balansiranju ćelijskih i sistemskih nivoa gvožđa. Neki od ovih DEG-ova kodiraju proteine s višestrukim funkcijama. Na primjer, MMP9, DUSP1, SLC11A1 i COL1A2 su povezani s većinom gore navedenih GO funkcija. Biološke funkcije DEG reguliranih odozgo prema dolje bile su raznovrsnije. Bilo je osam DEG-a uključenih u proces imunološkog sistema, pet je igralo ulogu u metabolizmu, a dva su povezana sa proliferacijom leukocita i razvojnim procesom (EPCAM i FCRL3). Opet, neki DEG, na primjer CD96 i FCRL3, kodiraju proteine s višestrukim ulogama.
Kod PP krava, 382 povećana DEG-a izvedena iz HC i LC poređenja bila su značajno povezana sa 690 GO funkcija, sa 20 najboljih prikazanih na slici 4C. Sve ovo je uključivalo 116 DEG (dodatni fajl S2F) sa različitim imunološkim aktivnostima. Glavna funkcija je bio signalni put receptora na površini ćelije. Ovo je bilo povezano sa 43 DEG koji su uključivali gene koji kodiraju mnoge receptore za imune ligande, kao što su CXCR1, CXCR2, IL17RD i IL1RAP. Ova funkcija je imala šest značajnih podfunkcija uključujući signalni put posredovan lipopolisaharidima (LPS) (PTAFR, TLR4 i SCARB1) i signalni put receptora ćelijske površine reguliran imunološkim odgovorom. Glavna podfunkcija unutar regulacije višećelijskog procesa u organizmu bila je regulacija proizvodnje citokina, sa 24 povišena DEG-a, kao što su MARK13, LTF i TLR4. Bilo je manje smanjenih DEG-ova (samo 78) koji su bili povezani sa 298 značajnih GO funkcija, sa nižim rezultatima obogaćivanja i raznovrsnijim biološkim procesima. Slika 4D prikazuje 20 najboljih funkcija. Jedan broj njih je bio povezan sa aspektima imuniteta, kao što su adhezija ćelija, regulacija proizvodnje medijatora imunog odgovora, odgovor na LPS i odgovor na molekule bakterijskog porekla. Drugi su se odnosili na održavanje homeostaze, kao što su površina ćelije, citoliza, transmembranski transport i endopeptidaza serinskog tipa. Sumiranje značajnih bioloških funkcija povezanih i sa povišenim i sniženim DEG-ovima je stvorilo sedam kategorija (Tabela 6), s procesom imunološkog sistema na vrhu i većinom drugih funkcija koje su također povezane sa imunološkom odbranom. Na primjer, kretanje je obogaćeno DEG-ovima s hemotaktičkim i imunološkim svojstvima i interakcijom među vrstama između organizama, što uključuje ubijanje invaziranih patogena. I ćelijski proces i biološka regulacija bili su povezani sa velikim brojem DEG. Ćelijski proces (n=239 DEGs) uključivao je mnoge podfunkcije povezane sa adhezijom ćelija, ubijanjem ćelija, aktivacijom imunoloških ćelija i proliferacijom ćelijske populacije. Biološka regulacija (125 DEG) takođe uključuje mnoge imunološke aktivnosti, kao što je regulacija procesa imunološkog sistema, lokomocija i odgovor na stimulans. Sve ove funkcije su sadržavale pretežno povišene DEG na HC dijeti.
Tabela 6. Sažetak glavnih funkcija DEG obogaćivanja GO u poređenju između krava prvorotki koje su nudile hranu s visokim (n=6) i niskim (n=6) koncentratom u ranoj laktaciji.

Tabela 6. Nast.

Kombinovani povišeni i smanjeni DEG (460) kod PP krava obogaćeni su sa 35 značajnih KEGG puteva (Tabela 7). Mnogi su bili povezani s metaboličkim procesima koji uključuju aminokiseline (valin, leucin, izoleucin, arginin i glutation), proteine, lipide (arahidonsku kiselinu, glicerolipid i kolesterol), vitamin B6 i neke hormone (aldosteron, kortizol, štitnjaču i hormon rasta ). Ovi metabolički putevi su bili pretežno obogaćeni DEG-ima koji su povećani na HC dijeti. Na primjer, biosinteza aminokiselina bila je povezana sa pet povišenih DEG-ova (ARG2, ASS1, GPT2, SDS i SDSL), put sinteze, sekrecije i djelovanja hormona rasta obogaćen je sa šest pojačano reguliranih (ADCY6, CREB3L2, CREB5, FOS , MAPK13 i SOCS3) i jedan smanjeni (BCAR1) DEG, a metabolizam arahidonske kiseline sadržavao je pet povišenih DEG (CYP2J2, GGT5, GPX3, PLB1 i TBXAS1). Nekoliko puteva povezanih s imunološkim/upalnim procesom također je značajno obogaćeno, opet uglavnom povišenim DEG-ovima. To uključuje signalne puteve hemokina, MAPK i TNF i kaskade komplementa i koagulacije. Na primjer, signalni put hemokina sadržavao je osam naviše reguliranih (ADCY6, CCL16, CCR1, CXCL13, CXCR1, CXCR2, GNG7 i HCK) i dva niže regulirana DEG-a (BCAR1 i CCR5), TNF signalni put je sadržavao šest povišeno reguliranih DEG2 (CRCREB35 DEG2). , FOS, MAPK13, MMP9 i SOCS3), a signalni putevi MAPK sadržavali su 12 povišenih DEG-ova, uključujući IL1A, MAP3K6 i MAPK13.
Tabela 7. Značajni putevi identificirani obogaćivanjem Keggovog puta povezani s različito eksprimiranim genima leukocita kod krava prvorotkinje nudile su visokokoncentratnu ishranu (n=6) u poređenju sa onima koje su nudile ishranu sa niskim sadržajem (n=6).

3. Diskusija
Mliječne krave nakon porođaja imaju homeostatske mehanizme za kontrolu raspodjele nutrijenata između laktacije i drugih važnih životnih funkcija, kao što su imunitet i rast [8]. Mobilizacija tkiva je normalna adaptacija sisara da podrži laktaciju, ali neke krave postaju metabolički neuravnotežene [35,37]. Takve životinje doživljavaju pretjeranu mobilizaciju masnog tkiva, inzulinsku rezistenciju i sistemsku upalu što doprinosi smanjenju imuniteta koji se često opaža u ovom trenutku [38]. Ovo je povezano sa inflamatornim medijatorima kao što su TNF i IL6 [39,40]. Dana 14. nakon teljenja, kada su sakupljeni uzorci cirkulirajućih leukocita u ovoj studiji, ćelije su stoga bile izložene periodu upalne stimulacije. Koristeći sekvencioniranje i bioinformatičku analizu nove generacije, pokazali smo da su ishrane sa različitim udjelima koncentrata proizvele različite efekte na cirkulirajući transkriptom leukocita kod PP i MP krava u ranoj laktaciji. To je bilo povezano s razlikama u njihovom zdravlju i plodnosti. Ove informacije su dodale nova otkrića našem prethodnom izvještaju o učincima ishrane na proizvodnju mlijeka i imunitet [32].
3.1. Poređenje efekata ishrane sa visokim i niskim koncentratom kod višerodnih krava
Krave MP na HC ishrani su imale veći DMI od MC i LC krava i to je bilo povezano sa višim koncentracijama glukoze i IGF{{0}} u cirkulaciji. To je dovelo do toga da su HC krave bile u manje ozbiljnom NEB i davale su više mlijeka. HC ishrana je formulisana da zadovolji potrebe za energijom i proteinima za laktaciju i održavanje telesne homeostaze, a merenja metabolita su potvrdila da je njihov metabolički status zaista bio bolji nego kod LC krava, sa manjim zahtevom za mobilizacijom tkiva kako bi se zadovoljile energetske potrebe. Ovo bi trebalo pomoći da se ubrza rješavanje postporođajnih upalnih procesa, jer su mnoge upalne bolesti u ranoj laktaciji povezane ili uzrokovane metaboličkim poremećajima [38], a ranije smo pokazali da se upala maternice brže rješavala kod krava s boljim statusom energetske ravnoteže. [2]. U ovoj studiji nije bilo razlike u odnosu PMN-a i epitelnih ćelija u lumenu materice prema ishrani kod krava MP. Ovaj indeks se često uzima kao indikator citološkog endometritisa [41]. Razlike prema ishrani su, međutim, uočene u mliječnoj žlijezdi jer su LC krave imale veći SCC i to je bilo povezano s većim udjelom njih koji su doživjeli klinički mastitis tokom prvih 16 DIM (28,6% naspram 0% u LC vs. HC grupe).
Većina DEG-ova identifikovanih u analizi transkriptoma leukocita bila je uključena u imunološke i/ili metaboličke procese, kao što se i očekivalo u populaciji imunih ćelija. Najznačajniji KEGG put bio je komplementarna i koagulaciona kaskada, koja je uključivala šest gena sa najnižom regulacijom kod HC krava. Od toga, CFB kodira faktor B komplementa, komponentu alternativnog puta aktivacije komplementa. FGA, FGB i FGG kodiraju tri podjedinice faktora koagulacije fibrinogen, ključne komponente krvnog ugruška koja je također važna u vezivanju bakterija za trombocite [42]. Visokomolekularni oblik kininogena, kodiran KNG1, također je bitan za zgrušavanje krvi, a kininogen oslobađa bradikinin, peptid s različitim funkcijama uključujući antibakterijsko i antifungalno djelovanje. Vitronektin, kodiran VTN, također je uključen u regulaciju puta koagulacije i zacjeljivanja rana, dok njegov domen koji vezuje heparin pruža antimikrobna svojstva. PROC kodira glikoprotein plazme čiji aktivirani oblik sadrži domen serin proteaze koji funkcionira u razgradnji aktiviranih oblika faktora koagulacije V i VIII, dok SERPINA1 kodira inhibitor serinske proteaze čiji ciljevi uključuju plazmin, trombin i aktivator plazminogena. Povećanje regulacije komplementa i kaskade koagulacije je ranije prikazano u tkivu dojke kao rani odgovor domaćina na E. coli ili Staph. aureus infekcija [43]. Kako je ovaj put bio izraženiji kod krava na LC ishrani, to podržava dokaze o većoj incidenci mastitisa kod ovih životinja.

cistanche tubulosa-poboljšava imuni sistem
Još jedna vrhunska funkcija koju je sažeo GO pretraživač bio je proces ubijanja patogena (međuvrstska interakcija između organizama), koji je bio povezan sa 14 sniženih DEG-ova kod HC krava (tabela 4). Ovo uključuje niz gena uključenih u antivirusnu aktivnost (IFI6, IFNB1, ISG15, MX2, OAS1Y, OAS1Z, OAS2 i RSAD2) koji su bili izraženi na nižim nivoima. Od njih, IFNB1 kodira interferon beta 1, dok su ostali svi geni stimulirani interferonom [44,45]. Svi su oni također dio signalnog puta NOD-like receptora (NLR). NLR su receptori za prepoznavanje citosolnog uzorka koji se aktiviraju različitim nesamostalnim komponentama uključujući bakterijski peptidoglikan, potencijalno inicirajući NF-kappa B-/AP{21}}zavisnu ekspresiju proinflamatornih citokina, ekspresiju interferona tipa I, autofagiju i upala [46]. Naša nedavna studija je pokazala da je ovaj put povećan u leukocitima krava zaraženih E. coli [47]. Drugi identificirani gen je MPO, koji kodira mijeloperoksidazu, enzim pohranjen u azurofilnim granulama PMN-a i makrofaga. Oslobađa se u ekstracelularnu tečnost tokom upalnih procesa i koristi se kao marker upale i oksidativnog stresa [48]. IL1R2 kodira člana porodice receptora interleukina 1 i bio je jedan od najznačajnije sniženih DEG identifikovanih kod krava MP. Ovo može vezati receptore IL1A, IL1B i interleukina 1, tipa I (IL1R1/IL1RA), ali djeluje kao mamac za inhibiranje aktivnosti liganda.
Gen sa najznačajnijom diferencijalnom ekspresijom između krava MP na različitim ishranama bio je FCER1A, sa nižom ekspresijom kod krava HC. Ovo kodira podjedinicu IgE receptora, koji je inicijator alergijskih odgovora koji su mogli evoluirati kako bi promovirali odbranu domaćina od parazita kroz oslobađanje medijatora kao što je histamin [49]. Zanimljivo je da je FCER1A bio jedan od samo 18 gena čiji je nivo ekspresije identificiran kao diskriminirajući između plodnosti goveđih junica [50]. Njegova precizna uloga u govedima ostaje neutvrđena, ali u ispitivanju vakcine na teladi eksperimentalno zaraženoj ekonomski važnom parazitskom nematodom Ostertagia ostertagi, nivoi njene ekspresije u krvi su u pozitivnoj korelaciji sa brojem mastocita i negativno sa brojem crva [51]. Tri druga pojačano regulirana gena kod HC krava s nekom imunološkom funkcijom su ALAS2, GZMB i LIF. ALAS2 kodira 50 -aminolevulinat sintazu 2, mitohondrijski lociran enzim specifičan za eritroide koji katalizira prvi korak koji ograničava brzinu u biosintetskom putu hema. Hem je esencijalni kofaktor u nizu ključnih procesa uključujući transport kisika, dok su mutacije ovog gena povezane s raznim ljudskim bolestima uključujući anemiju [52]. GZMB kodira preprotein koji luče prirodne ćelije ubice i citotoksični T limfociti i koji se obrađuje kako bi se stvorila aktivna proteaza koja inducira apoptozu ciljne ćelije i također obrađuje citokine i razgrađuje proteine ekstracelularnog matriksa [53]. Inhibicijski faktor citokinske leukemije, kodiran LIF-om, prvobitno je identificiran kroz uključenost u diferencijaciju makrofaga, ali se također pokazalo da igra važnu ulogu u razvoju embriona i uspostavljanju trudnoće kod raznih vrsta uključujući goveda [54].
DEG dobijeni iz HC i LC poređenja kod krava MP takođe su obogaćeni sa nekoliko značajnih puteva povezanih sa metabolizmom glukoze, proteina i masnih kiselina. Ovo uključuje četiri smanjena DEG-a uključena u PPAR signalne puteve (APOA2, APOC3, FABP1 i PCK1). U ovoj studiji, tri glavne PPAR izoforme (A, D, G) su otkrivene u populaciji leukocita. Iako na ekspresiju samih PPAR-ova nije utjecala prehrana, ovaj put može utjecati na ekspresiju gena uključenih u metabolizam glukoze i lipida, diferencijaciju adipocita i upalne odgovore [55,56] i doprinosi metaboličkoj adaptaciji na ograničenu opskrbu hranjivim tvarima. inducirajući gene uključene u -oksidaciju [57]. Metabolički put retinola je također smanjen u HC kravama, sa nižom ekspresijom RBP4 i TTR (kodiraju protein koji vezuje retinol i transtiretin, respektivno), a oba djeluju kao transporteri retinola u krvi. Interakcija retinola s PPAR signalnim putem utječe na transkripciju mnogih drugih gena koji se nalaze u nizu [58]. APOA2 i APOC3 zajedno sa APOH su takođe deo metaboličkog puta holesterola. Holesterol je glavna komponenta plazma membrane i utiče na njenu organizaciju i funkciju [59,60]. Nedavne studije su podvukle sve veću ulogu holesterola kao važnog modulatora urođene i adaptivne imunološke aktivnosti [61].
Put glikolize/glukoneogeneze bio je povezan sa tri smanjena DEG kod krava hranjenih HC (ADH1C, ALDOB i PCK1). Od njih, PCK1 kodira fosfoenolpiruvat karboksikinazu 1 koja djeluje kao glavna kontrolna tačka za regulaciju glukoneogeneze. Ovaj enzim, zajedno sa GTP, katalizira stvaranje fosfoenolpiruvata iz oksaloacetata, uz oslobađanje ugljičnog dioksida i GDP. Aktivacija imunoloških/inflamatornih puteva promoviše transkripciju glukoneogenih gena preko toll-like receptora 4 (TLR4) [62]. Ovo može uzrokovati da imunološke stanice prebace svoj metabolizam glukoze sa oksidativne fosforilacije na glikolizu kako bi proizvele energiju i hranjive tvari potrebne za proliferaciju i proizvodnju imunoloških molekula [12,63]. To dovodi do povećane potražnje za glukozom koja se nadmeće sa potrebama proizvodnje laktata [64].
Ukratko, razlike u ekspresiji gena između MP krava na HC i LC ishrani daju dokaze veće pojačane imunološke aktivnosti i upale kod LC krava. Ovo je bilo praćeno većom incidencom mastitisa. Nasuprot tome, geni koji kodiraju neke proteine koji će vjerovatno biti od koristi za zdravlje i plodnost, kao što su ALAS2 i LIF, bili su pojačano regulirani kod HC krava. Ovo podržava izmjerene metaboličke indekse koji pokazuju da je došlo do poboljšanog EBAL statusa kod krava MP na HC ishrani, što je vjerovatno pomoglo u njihovoj zaštiti od razvoja infektivnih ili metaboličkih bolesti.
3.2. Poređenje efekata ishrane sa visokim i niskim koncentratom kod prvorotkih krava
Slično MP kravama, PP krave na HC ishrani takođe su imale veći DMI, za oko 4 kg/d, ali prinos mleka nije značajno povećan. Nije bilo značajnih razlika u cirkulirajućim koncentracijama glukoze, NEFA, BHB ili IGF-1, pri čemu je samo urea bila veća na LC dijeti. Nasuprot tome, bilo je značajnijih razlika u ekspresiji leukocitnih gena između grupa u ishrani nego kod krava MP krava, sa 460 naspram 173 DEG identifikovanih u HC i LC poređenjima, od kojih je 83% povećano kod PP krava na HC ishrani. Samo mali dio DEG-ova se preklapao između dvije starosne grupe (Slika 3), što sugerira da su promjene u funkciji leukocita u ranoj laktacijskoj ishrani bile osjetljivije kod PP krava nego kod MP krava. Očekivali smo da će HC ishrana imati koristi za PP krave povećanjem njihovog DMI i potpuno ispunjavanjem izračunatih prehrambenih nerazgradivih i metaboličnih proteina. EBAL je zaista poboljšan na HC dijeti, ali analiza ekspresije gena pokazala je mnogo veću regulaciju gena uključenih u imunološku odbranu. Krave hranjene HC također su imale veći omjer PMN-a: UEC u maternicama zajedno s brojčano većim SCC i više slučajeva mastitisa. To sugerira da su zapravo bili više, a ne manje skloni bolesti. Prethodno smo otkrili da neutrofili prikupljeni od PP krava u ovoj studiji u prve tri sedmice laktacije imaju značajno veći fagocitni indeks i indeks oksidativnog pucanja u poređenju sa MP kravama, ali 2-način na koji način ishrana i paritet utiču na ova mjerenja nisu prijavljena [32].
Procesi imunog sistema identifikovani u poređenju HC sa LC uključivali su povećanje regulacije receptora ćelijske površine i signalnih puteva za prepoznavanje obrazaca, hemotaksiju, proizvodnju citokina i migraciju leukocita kod krava hranjenih HC. Identifikovani DEG bili su povezani sa različitim mehanizmima imunološke odbrane, uključujući razne antimikrobne peptide (AMP) (CATHL6, CXCL13, DEFB1, LTF, PGLYRP1, PGLYRP4, SA100A8, SA100A9, S100A1 i SLC11A1). Oni ne samo da mogu direktno ubiti invaziju organizme, već i pomoći modulacijom drugih imunoloških i antimikrobnih procesa [65–67]. Povećana regulacija antimikrobnih peptida u transkriptomskim profilima leukocita je ranije dokazana kod krava sa kliničkim mastitisom [47,68] i metritisom/endometritisom [69,70]. Funkcija adhezije leukocita bila je povezana sa 16 povišenih i pet smanjenih DEG kod životinja hranjenih HC. Adhezija leukocita na zidove kapilara važan je prvi korak u omogućavanju transmigriranja iz krvi i prometa prema mjestima oštećenja tkiva, infekcije i upale [71]. Interakcije stanica-ćelija i stanica-matriks utječu na fenotip leukocita, a disregulacija adhezionih puteva može dovesti do uporne aktivacije leukocita s neriješenom upalom [72]. Od identifikovanih povišenih DEG, ADAM8, ANGPTL3, CD24, ICAM3 i THY1 su svi uključeni u ekstravazaciju [73,74] dok FN1, NRP1, TNFAIP6 i VCAN imaju potencijalnu ulogu u prometu ćelija leukocita i funkciji u upaljenim tkivima [72, 75]. Geni koji kodiraju hemokinske receptore CXCR1 i CXCR2 su takođe pojačano regulisani kod krava hranjenih HC; oba su važna za stimulaciju hemotakse PMN prema mjestima infekcije, kao i za aktiviranje biokemijskih procesa koji ubijaju invazivne bakterije [76].
Od gena sa smanjenom regulacijom povezanih sa adhezijom kod krava hranjenih HC, BCAR1 kodira multifunkcionalni protein poznat kao cas sa uključenošću u ćelijsku pokretljivost, apoptozu i kontrolu ćelijskog ciklusa [77]. Polimorfizmi u BCAR1 su ranije bili povezani sa rezistencijom na SCC i mastitis [78]. ADGRG1 (također poznat kao GPR56) kodira receptor povezan sa G proteinom koji vezuje kolagen 3 i transglutaminazu 2, obe komponente strome tkiva. Pokazalo se da ADGRG1 igra ulogu u ljudskim prirodnim ćelijama ubica (NK), u kojima inhibira njihovu citotoksičnost [79]. Njegova vlastita ekspresija je smanjena nakon aktivacije izazvane citokinom, što bi bilo u skladu sa ovdje prikazanim rezultatima. CD96 protein takođe deluje kao inhibitorni receptor kontrolne tačke na NK ćelijama [80]. Prethodne studije o promenama u transkriptomu leukocita tokom prelaznog perioda takođe su pronašle promene u ekspresiji gena u vezi sa transendotelnom migracijom, iako sa različitim zaključcima, izveštavajući ili o aktivaciji nakon teljenja [81] ili o inhibiciji [82], respektivno. Naša analiza je također identificirala brojne razlike u signalnim putevima znakova metabolizma aminokiselina kod krava PP na HC ishrani u usporedbi s onima na LC ishrani, povezane s enzimima kodiranim sa pet povišenih DEG-ova (ARG2, ASS1, GPT2, SDS i SDSL) . Od njih, ASS1 kodira arginin sukcinat sintazu 1, koja katalizira pretposljednji korak biosintetskog puta arginina, dok ARG2 kodira arginazu, katalizujući hidrolizu arginina u ornitin i ureu. L-arginin se također može pretvoriti u dušikov oksid, signalni molekul koji igra ključnu ulogu u patogenezi upale [83]. Glutaminsko-piruvična transaminaza 2 (GPT2) je mitohondrijski enzim koji katalizuje reverzibilnu transaminaciju između alanina i 2-oksoglutarata za stvaranje piruvata i glutamata. Ovaj gen je pojačan u uslovima metaboličkog stresa i igra ulogu u pokretanju glukoneogeneze iz metabolizma aminokiselina [84]. Serin dehidrataza (SDS) kodira enzim koji pretvara L-serin u piruvat i amonijak, dok se predviđa da će serin dehidrataza (SDSL) biti uključena u put biosinteze izoleucina iz treonina.
Put metabolizma holesterola bio je povezan sa četiri povišena DEG-a na HC dijeti (ANGPTL3, LRP1, SCARB1 i SORT1). To može dovesti do nakupljanja kolesterola u leukocitima krava hranjenih HC-om i promovirati upalu, uključujući povećanje TLR signalizacije, aktivaciju inflamasoma i veću proizvodnju monocita i neutrofila u koštanoj srži i slezeni [85]. Put metabolizma arahidonske kiseline sa pet povišenih DEG-ova (kao što je prethodno navedeno) dovodi do proizvodnje kaskada pro- i anti-inflamatornih proizvoda, kao što su prostaglandini i leukotrieni [86]. Put metabolizma glicerolipida bio je povezan sa četiri povišena DEG-a (DGAT2, DGKG, GK i GPAT3) koji kodiraju lipogene gene uključene u sintezu triacilglicerola. Njegovo nakupljanje može izazvati aktivaciju leukocita i upalu [87,88]. Svi ovi nalazi podupiru zaključak da je HC dijeta povećala metaboličke puteve leukocita kod PP krava na način koji je povećao njihov imunološki/inflamatorni odgovor. Prethodni rad na kravama bio je fokusiran uglavnom na sušni period i pokazao je da prekomjerno hranjenje i visok BCS u ovom trenutku pospješuju naknadnu mobilizaciju lipida i povećanu inflamatornu reakciju tokom peripartalnog perioda [34]. U ovoj studiji, omjer PMN:UEC maternice i trend prema većem SCC podržavaju sugestiju da je došlo do povećane migracije leukocita u matericu i mliječnu žlijezdu kod PP krava koje su primale HC ishranu. Iako je ovo bitna komponenta imunološke odbrane, prekomjerna aktivacija može doprinijeti hiper-upali. Potrebna je daljnja studija s većom veličinom uzorka kako bi se potvrdili ovi nalazi.
3.3. Sličnosti u odgovoru na ishranu višerodnih i prvorodnih krava
In terms of metabolic changes, both the MP and PP cows had higher circulating concentrations of urea when on the LC diet. Blood urea in both late pregnancy and early lactation may rise following mobilization of amino acids stored in skeletal muscle [89] or when dietary protein supply exceeds energy availability or protein needed [90], so these situations could have applied here. Elevated levels of urea have been associated with reduced fertility, but only at >4,5 mmol/L, više od koncentracija koje su postignute kod životinja hranjenih LC u ovoj studiji [91]. Što se tiče podataka o transkripciji gena leukocita, zanimljivo je napomenuti da su DEG izvedeni iz HC i LC poređenja u obje starosne grupe bili obogaćeni putem varenja i apsorpcije proteina, u kojem geni koji kodiraju različite izoforme kolagena igraju važnu ulogu. . Među njima, bila su tri pojačano regulirana kolagena gena (COL1A1, COL1A2 i COL3A1) i kod MP i PP krava, i jedan smanjeni (COL5A3) gena za kolagen u MP krava. Njihove vrijednosti ekspresije u uzorcima su bile male, ali su razlike bile značajne. Dio ove RNK može doći od fibrocita, ćelijske populacije koja se sastoji od samo 0.1–0,5% neeritrocitnih ćelija u perifernoj krvi [92,93]. Kolagen je dugo uspostavljeni imunološki pojačivač uključen u mnoge imunološke/upalne procese [93,94]. Njegova povećana proizvodnja u cirkulirajućoj krvi HC dijetom može stoga utjecati na funkciju leukocita.
3.4. Implikacije za plodnost
Mnoge prethodne studije su izvijestile da međusobno povezani metabolički i imunološki status i učestalost bolesti krava u ranoj laktaciji imaju veliki utjecaj na njihovu kasniju plodnost (npr. [38,95]). Naš vlastiti rad je pokazao da krave MP sa niskom koncentracijom IGF-1 na 14 DIM imaju manju vjerovatnoću da će uopšte zatrudnjeti [37]. Nedavno smo izvijestili da je 63% krava sa niskim IGF-1 u ovom trenutku imalo više od jednog zdravstvenog problema tokom svojih prvih 35 DIM u poređenju sa samo 26% krava sa visokim IGF-1. To je uključivalo više životinja s infekcijama maternice i kliničkim mastitisom [10]. Foley et al. [69] razlikovali su zdrave krave, koje su bile u stanju da povrate homeostazu u roku od 3 sedmice nakon teljenja, i druge koje su doživjele ozbiljniji i produženi upalni odgovor koji je potom razvio klinički endometritis. Povezanost s perifernom krvlju demonstrirali su Galvão et al. [96] koji su pokazali da neutrofili krava sa lošijim EBAL-om imaju niži sadržaj glikogena na sedam DIM-a i da su ove životinje iskusile više bolesti materice, potencijalno povezane sa smanjenom dostupnošću oksidativnog goriva za imunološki odgovor. Klinički mastitis u ranoj laktaciji je također povezan s povećanom stopom gubitka embriona prije implantacije, uz neke indikacije da nizak BCS dodatno povećava rizik [97]. Predloženi su brojni mehanizmi povezani sa proizvodnjom citokina i prostaglandina i drugih inflamatornih medijatora koji bi mogli utjecati na jajnik i/ili uzrokovati nepovoljno okruženje materice [98,99]. Podaci o plodnosti krava u našoj studiji podržali su nalaze koji se odnose na njihov imunološki status i zdravlje u ranoj laktaciji. Krave MP na LC ishrani zahtijevale su brojčano više S/C u skladu sa njihovim lošijim EBAL-om, zajedno sa dokazima iz analize transkriptoma leukocita o aktivnijoj imunološkoj odbrani u toku, što je potkrijepljeno njihovom većom incidencom mastitisa. Nasuprot tome, PP kravama na HC ishrani trebalo je znatno duže da zatrudne i manje ih je ostalo gravidno u poređenju sa kravama hranjenim LC. Imale su više dokaza o upali u ranoj trudnoći iako je njihov izračunati EBAL bio bolji. Trenutno, osnovni mehanizmi koji uzrokuju njihovo loše zdravstveno stanje i plodnost su neizvjesni iako smo također pronašli dokaze zasnovane na globalnoj ekspresiji gena povećane upale jetre i fibroze (Cheng, Little, Ferris, Takeda, Ingvartsen, Crowe i Wathes, neobjavljena zapažanja) .
3.5. Ograničenja studije
Na raspolaganju je bilo manje PP krava po grupi, što je smanjilo statističku moć analiza koje se odnose na fenotipove. Stoga je potrebna daljnja studija s većom veličinom uzorka kako bi se potvrdili učinci ishrane na reprodukciju i bolesti. U ovoj studiji smo ekstrahovali svu RNK iz pune periferne krvi koristeći Tempus epruvete i njen sistem za izolaciju. Ovo nudi lakoću prikupljanja za velike farmske studije, ali ne razdvaja tipove ćelija, koje će uključivati T i B limfocite, prirodne ćelije ubice, trombocite, monocite, granulocite (neutrofile, eozinofile i bazofile) i fibrocite. Predstavljeni podaci o ekspresiji gena su stoga bili pod uticajem mogućih efekata tretmana na relativne proporcije određenih tipova ćelija pored njihovih pojedinačnih transkripcionih promena. Ovi rezultati su takođe zasnovani na nivoima transkripcije gena i ne uključuju informacije o njihovoj posttranslacionoj obradi, koja će takođe uticati na to koliko se funkcionalnog proteina proizvodi.
4. Materijali i metode
4.1. Životinje i dijeta
Sve procedure su sprovedene u skladu sa Zakonom o životinjama (naučne procedure) iz 1986. i pokrivene licencom Home Office Project broj PPL2754 i potvrdom o određivanju za osnivanje. Rad je također odobrio Komitet za etiku i dobrobit Instituta za poljoprivrednu hranu i biološke nauke (AFBI, Belfast, Sjeverna Irska, UK). Iz stada AFBI-a regrutovane su 62 holštajn-frizijske krave. Među njima je bilo 18 PP (laktacija 1) i 44 MP sa laktacionim brojevima 2–7 (3,5 ± 1,28) i sve krave su bile zdrave prema veterinarskom pregledu. Težina teljenja je bila 680 ± 62 (srednja ± STD) kg za MP krave i 550 ± 39 kg za PP krave. Nakon teljenja, PP i MP krave su odvojeno raspoređene u tri grupe ishrane, pri čemu je raspodela u svakoj starosnoj grupi bila uravnotežena za predviđenu sposobnost prenosa masti plus proteina (kg), BW pre teljenja i BCS. MP krave su također izbalansirane za paritet i prethodnu laktaciju 305-dnevnog prinosa mlijeka. Kravama je ponuđen ili (1) niski koncentrat (LC, 30% koncentrata plus 70% travnata silaža, n=6 za PP i n=14 za MP); (2) srednji koncentrat (MC, 50% koncentrat plus 50% travnata silaža, n=6 za PP i n=15 za MP) ili (3) visoki koncentrat (HC, 70% koncentrat plus 30% travna silaža, n=6 za PP i n=15 za MP) ishrane (procenti na bazi suhe materije). Koncentrat za svaki tretman je formuliran tako da se postigne uobičajena ukupna koncentracija sirovog proteina (CP) u ishrani za svaki od LC, MC i HC (152, 152 i 154 g/kg DM respektivno), dok je izračunata ukupna metabolljiva energija ishrane ( ME) sadržaji su bili 12,0, 12,4 i 12,8 MJ/kg DM. Procijenjeno je da ishrana obezbjeđuje 1556, 1997 i 2420 g/d efektivnih razgradivih proteina iz buraga; 559, 733 i 888 g/d nerazgradivih proteina u ishrani i 1346, 1817 i 2275 g/d metaboličnih proteina za LC, MC i HC, respektivno. Pristup obrocima za tretman kontrolisan je sistemom za ishranu Calan Broadbent (American Calan Inc., Northwood, NH, SAD) koji je bio povezan sa elektronskim identifikacionim sistemom, koji je omogućavao da se pojedinačni unos krava bilježi dnevno. Dijeta za svaki tretman je ponuđena na 107% unosa prethodnih dana kako bi se osigurala konzumacija ad libitum. Svim kravama je također ponuđeno dodatnih 0,5 kg koncentrata pri svakoj mužnji putem sistema hranjenja u salonu kako bi se održao efikasan protok krava. Ova studija je bila dio šireg projekta i puni detalji ponuđene prehrane, upravljanja ishranom i sastava hrane su prethodno opisani [32].
4.2. Prikupljanje podataka o fenotipu krava
Tjelesna težina je zabilježena dva puta sedmično pomoću vage. BCS je procijenjen na oko 14 DIM [100]. Sve krave su muuzene dva puta dnevno i evidentirani su njihovi dnevni prinosi. Uzorci mlijeka analizirani su dva puta sedmično korištenjem srednje infracrvene analize na koncentracije proteina, masti i laktoze, a brojane su i somatske ćelije mlijeka. Dodatni jutarnji uzorci mlijeka (2 × 8 mL) sakupljani su dva puta sedmično i čuvani na -18 ◦C za analizu LDH (EC. 1.1.1.27) i NAGase (EC 3.2.1.30) korištenjem fluorometrijskih testova [101]. Energetski korigovani prinos mleka (ECM; kg/dan) izračunat je prema metodama koje smo koristili u našoj grupi [32]. EBAL svake krave je procijenjen koristeći prethodno opisanu metodu [102].
Klinički mastitis je dijagnosticiran standardnim metodama zasnovanim na svakodnevnim opažanjima abnormalnih promjena u izgledu mlijeka (npr. ljuspice, ugrušci), kvaliteti, prinosu mlijeka i upalnim reakcijama dojke (crvenilo, otok, vrućina ili bol). Očitavanje SCC mlijeka zajedno sa kliničkim dijagnozama korišteno je za kategorizaciju krava u tri grupe. Zdrave krave su definirane kao one sa SCC < 100,000 ćelija/mL mlijeka i bez kliničkih simptoma. Subklinički mastitične krave su definirane kao one koje imaju SCC između 100,000 i 400,000 ćelija/mL mlijeka i nemaju očigledne kliničke simptome. Krave kod kojih je dijagnosticiran klinički mastitis imale su SCC > 400,000 ćelija/mL mlijeka i pokazale su neke od gore navedenih kliničkih simptoma. Krave su osjemenjivane u uočenom estrusu koristeći uobičajenu praksu stada, a podaci o plodnosti za vrijeme naredne laktacije ili dok životinja nije bila izbačena su preuzeti iz evidencije stada. Prijavljeni podaci su uključivali dane do prvog servisa (DFS), dane do začeća (dani otvoreni), usluge po začeću i udio krava koje su začete. Pored toga, podaci o začeću su ocijenjeni korištenjem 4-boda u listovima prema (ICB) rezultatom kao (1)<100 days, (2) 100–200 days, (3) >200 dana, ili (4) nije uspjela zatrudnjeti ili odstreljena.
4.3. Citološka analiza materice
Uzorak citočetkice materice (Minitube, Minitüb GmbH, Tiefenbach, Njemačka) uzet je od svake krave oko 14 DIM da bi se procijenila citologija endometrija, kao što je prethodno opisano [103]. Dvostruko zaštićena citočetkica je vođena ručno kroz cerviks u matericu, unutrašnji štitnik je ekstrudiran iz vanjskog štitnika, a četkica je lagano rotirana prema zidu endometrijuma. Četkica je zatim uvučena u unutrašnji štitnik i uklonjena. Slajdovi za citološko ispitivanje pripremljeni su namotavanjem citočetkice na čisto stakleno mikroskopsko stakalce i fiksiranjem uzorka Fisherbrand™ CytoPrep™ Cytology Fixative (Fishers Scientific, Blanchardstown, Irska). Fiksni preparati su poslani na UCD School of Veterinary Medicine, University College Dublin, Irska na obradu i obojeni modifikovanom Giemsa bojom. Citološka procjena je izvršena prebrojavanjem PMNs UEC-a pri 400x uvećanju (Leitz Labourlux-S, Wetzlar, Njemačka) i određivanjem njihovog omjera, u prosjeku brojanjem 10 polja velike snage po slajdu.
4.4. Analiza cirkulirajućih metabolita i IGF-1
14 ± 2 (srednja ± STD) dana nakon teljenja, 10 mL uzoraka krvi sakupljeno je iz jugularne vene svih krava u Na heparin epruvete za plazmu i obične epruvete za serum. Nakon odvajanja plazme ili seruma centrifugiranjem, čuvani su na -20 ◦C do analize. Koncentracije glukoze, uree, BHB, NEFA i holesterola u plazmi mjerene su metodama koje su prethodno opisane [20,25]. Ukratko, koncentracija NEFA u serumu je određena metodom ACS-ACOD koristeći NEFA C komplete (Wako, Neuss, Njemačka). Glukoza u plazmi je kvantifikovana enzimskom metodom (ADVIA 1800 Clinical Chemistry System, Siemens Healthcare Diagnostics, Ballerup, Danska). BHB u serumu je određen mjerenjem apsorbancije na 340 nm zbog proizvodnje NADH pri alkalnom pH u prisustvu BHB dehidrogenaze. Serumska urea je analizirana spektrofotometrijom. Koeficijenti varijacije unutar i među testovima (CV) su u svim slučajevima bili ispod tri odnosno četiri procenta, respektivno, za niske i visoke kontrolne uzorke. Koncentracije serumskog IGF-1 su kvantificirane radioimunim testom nakon ekstrakcije kiselim etanolom [104]. Intra-test CV je bio 12,4, 7,5 i 9,9% za niske, srednje i visoke kontrolne uzorke, respektivno.
4.5. Ekstrakcija RNK krvi
Uzorci krvi za ekstrakciju RNK sakupljeni su punkcijom jugularne vene od svih krava na 14 ± 2 DIM u Tempus krvne RNA epruvete (Thermo-Fisher Scientific, Loughborough, UK). Epruvete su snažno protresene 15–20 sekundi odmah po sakupljanju, zatim zamrznute i pohranjene na -8{26}} ◦C za ekstrakciju RNK. RNK cijele krvi je ekstrahirana korištenjem Tempus Spin RNA izolacijskih kompleta (Thermo-Fisher) slijedeći upute proizvođača kao što je prethodno opisano [20]. Agilent BioAnalyzer 2000 (Agilent Technologies UK Ltd., Cheadle, UK) s Agilent RNA 6000 Nano Kit (Agilent Technologies UK Ltd., Cheadle, UK) korišten je za procjenu količine i integriteta RNK. Dodatno, količina i čistoća su potvrđeni sa NanoDrop 1000 (Thermo Fischer). Podaci o kvaliteti su sažeti u Dodatnoj datoteci S3. Ovo je pokazalo da su svi uzorci RNK imali razuman integritet (RIN broj > 8,7, 9,3 ± 0,3) i čistoću (260/280 između 2,01 i 2,15, srednja vrijednost ± STD 2,10 ± 0,03), tako da nijedna životinja nije uklonjena iz analize. RNK je pohranjena na -80 ◦C za naknadno sekvenciranje RNK.
4.6. RNA-sekvenciranje, mapiranje i kvantifikacija
Ekstrahirana RNA leukocita je sekvencirana na Illumina NextSeq 500 platformi kao što je prethodno opisano [68]. Ukratko, koristeći epMotion radnu stanicu za rukovanje tekućinom (Eppendorf, Hamburg, Njemačka) 750 ng ukupne RNK je reverzno transkribirano u biblioteke sekvencioniranja cDNK pomoću Illumina TruSeq Stranded Total RNA Library Prep Ribo-Zero Gold kompleta (Illumina, San Diego, CA ). Objedinjene biblioteke cDNK sekvencionirane su na Illumina NextSeq 500 sekvenceru na jednostranim čitanjima dužine 75 nukleotida kako bi se postiglo prosječno 33,5 miliona čitanja po uzorku. Sirovi FASTQ fajlovi su deponovani u Evropski arhiv nukleotida (E-MTAB-9347 i E-MTAB-9431). Sve analize sekvenciranja su sprovedene korišćenjem CLC Genomic Workbench v21 (Qiagen, Manchester, UK). Svaki uzorak je sadržavao očitavanja iz četiri trake i oni su spojeni u jednu fastq datoteku. Kvalitet neobrađenih i skraćenih fastq fajlova je procenjen nakon Illumina Pipeline-a 1.8 i sva neuspela čitanja su uklonjena. Čitanja su zatim mapirana u referentni skup genoma Bos taurus (ARS-UCD1.2 koju je obezbedio RefSeq na https://www.ncbi.nlm.nih.gov/assembly, pristupljeno 1. januara 2021.) i kvantifikovana kao čitanja po genu, čitanja po milionu kilobaze (RPKM) i transkripta po milionu kilobaze (TPM). Oni su pohranjeni kao datoteke ekspresije gena (GE) u CLC Genomics Workbench da bi se koristile za sljedeću analizu diferencijalne ekspresije gena.
4.7. Analiza diferencijalne ekspresije gena između grupa u ishrani
Prije analize diferencijalne ekspresije za efekat ishrane, koristili smo analizu glavnih komponenti (PCA) sa RPKM vrijednostima da identifikujemo vanjske vrijednosti, i to je pokazalo da su dvije krave (Blood020009, MP i Blood020103, PP) bile izvan populacija i stoga su isključeni iz dalje analize (dodatni fajl S4A). Analiza glavnih komponenti je također pokazala da postoji samo ograničeno preklapanje u ukupnom obrascu ekspresije gena između krava PP i MP (dodatni fajl S2B). Ovo je podržalo originalni dizajn studije za analizu svake starosne grupe posebno. GE fajlovi izvedeni iz svih pojedinačnih uzoraka su stoga razdvojeni prema starosnoj grupi (PP, n=5–6 po grupi i MP, n=14–15 po grupi). DEG između grupa u ishrani kod PP ili MP krava identifikovani su pomoću CLC Genomics Workbench V21 jednosmernom procedurom nalik ANOVA. Stope lažnog otkrivanja (FDR) za više testova su prilagođene sa Benjamini-Hochbergom (BH) i značajnost je uzeta u obzir pri p < 0,05. Promjene puta (FCs) su izračunate kao omjer ekspresije gena grupe sa višim koncentratom prema grupi sa nižim koncentratom (npr. HC vs. LC, MC vs. LC ili HC vs. MC) ako je vrijednost grupe s višim koncentratom bio veći nego u grupi sa nižim koncentratom (pozitivna promjena nabora, regulacija naviše). Ako je vrijednost grupe s nižim koncentratom bila veća od vrijednosti grupe s višim koncentratom, korišten je omjer grupe nižeg koncentrata i grupe sa višim koncentratom (npr. LC naspram HC, MC naspram HC i LC naspram MC ) (negativna promjena nabora, regulacija prema dolje). Za dalju analizu odabrani su DEG regulisani naviše i naniže sa apsolutnom promjenom više od ili jednako 1,5 između grupa sa ishranom.
4.8. Analiza obogaćivanja genske ontologije (GO).
DEG izvedeni iz poređenja parova između grupa u ishrani uneseni su u Partek Genomics Suite V7.1 (Partek Incorporation, Chesterfield, MO, SAD) za analizu obogaćivanja GO za istraživanje bioloških funkcija i interakcija između DEG-ova i pridružene Kjoto Enciklopedije Putevi gena i genoma (KEGG) sa genomom Bos taurus ARS-UCD1.2. Korišten je Fisherov egzaktni test sa BH prilagođavanjem i statistička značajnost je uzeta u obzir pri p < 0.05.
4.9. Statistička analiza fenotipskih podataka
Podaci dobijeni od svih krava prvo su podijeljeni po starosnoj grupi (PP i MP krave), prema dizajnu studije. Vrijednosti DMI, BW, parametara mlijeka, EBAL, BCS, cirkulirajućih metabolita (glukoza, urea, BHB, NEFA, holesterol i IGF{{0}}), SCC (logaritamski transformirani) i broja ćelija materice a njihovi omjeri su sumirani kao srednja vrijednost ± standardna greška srednje vrijednosti (SE). Statistička analiza je korištena za poređenje razlika između grupa u ishrani koristeći jednosmjernu ANOVA-u ugrađenu u softverski paket SPSS V28 (Čikago, IL, SAD). Homogenost varijanse za svaku varijablu je testirana Levenovom statistikom prije ANOVA. Rezultati su pokazali da homogenost između grupa za ECM, EBAL, glukozu, ureu, BHB i IGF-1 kod PP krava nije postignuta, pa je za ove varijable primijenjena logaritamska transformacija. Tamo gdje je ANOVA pokazala značajnost, izvršena su višestruka poređenja sa Fišerovom LSD metodom kako bi se identifikovao izvor razlika. Kako homogenost varijanse za podatke SCC mlijeka i citologije materice nije mogla biti postignuta nakon logaritamske transformacije, ove varijable su testirane korištenjem Kruskal-Wallis-ove jednosmjerne ANOVA sa Dunnovim višestrukim poređenjima. Podaci o plodnosti su testirani Wilcoxon metodom. U svim slučajevima, značajnost je uzeta u obzir pri p < 0,05.
5. Zaključci
Ova studija podržava raniji rad u demonstriranju jasnih veza između metaboličkog statusa krava u ranoj laktaciji i njihove imunološke funkcije. Većina prethodnih istraživanja usmjerenih na poboljšanje zdravlja nakon porođaja kroz bolju ishranu fokusirala su se na prepartalni period i pokazala da prekomjerno hranjenje i visok BCS u ovom trenutku promovišu kasniju mobilizaciju lipida i povećan upalni odgovor tokom peripartalnog perioda [34]. Umjesto toga, procijenili smo da li je moguće promijeniti imunološku funkciju nakon teljenja promjenom ishrane za laktaciju. Otkrili smo da je odgovor na uključivanje dodatnog koncentrata, koji je dao ishranu formuliranu da zadovolji potrebe životinja za energijom i proteinima, proizveo različite efekte na transkriptom leukocita kod krava MP i PP. Kod krava MP, HC ishrana je bila očito korisna, jer su leukociti LC krave imali pojačanu regulaciju kaskade komplementa i koagulacije i urođene imunološke odbrambene mehanizme protiv patogena. Nasuprot tome, leukociti u PP kravama na HC ishrani pokazali su veće imunološke/inflamatorne odgovore i imali su veći odnos PMN:UEC, što ukazuje na povećanu migraciju leukocita u matericu. Ove krave su kasnije imale duži interval od teljenja do začeća, što ukazuje na lošiju plodnost. Dalji rad s većim brojem krava je opravdan kako bi se potvrdio nalaz dijetetskog efekta na plodnost i kako bi se potpunije razumjelo kako se metabolički odgovori postpartalne prehrane razlikuju kod mlađih životinja.
Reference
1. Mallard, BA; Dekkers, JC; Ireland, MJ; Leslie, KE; Sharif, S.; Vankampen, CL; Wagter, L.; Wilkie, BN Promjena imunološkog odgovora tokom peripartalnog perioda i njena grana na zdravlje mliječnih krava i teladi. J. Dairy Sci. 1998, 81, 585–595. [CrossRef] [PubMed]
2. Wathes, DC; Cheng, Z.; Chowdhury, W.; Fenwick, MA; Fitzpatrick, R.; Morris, DG; Patton, J.; Murphy, JJ Negativan energetski balans mijenja globalnu ekspresiju gena i imunološke odgovore u materici postporođajnih mliječnih krava. Physiol. Genom. 2009, 39, 1–13. [CrossRef]
3. Ingvartsen, KL; Moyes, K. Ishrana, imunološka funkcija i zdravlje mliječnih goveda. Animal 2013, 7 (Suppl. 1), 112–122. [CrossRef] [PubMed]
4. Kehrli, ME, Jr.; Nonnecke, BJ; Roth, JA Promjene u funkciji goveđih neutrofila tokom periporođajnog perioda. Am. J. Vet. Res. 1989, 50, 207–214. [PubMed]
5. Ster, C.; Loiselle, MC; Lacasse, P. Utjecaj koncentracije neesterificiranih masnih kiselina u serumu nakon teljenja na funkcionalnost goveđih imunoloških stanica. J. Dairy Sci. 2012, 95, 708–717. [CrossRef] [PubMed]
6. Lacetera, N.; Scalia, D.; Bernabucci, U.; Ronchi, B.; Pirazzi, D.; Nardone, A. Funkcija limfocita kod previše kondicioniranih krava oko porođaja. J. Dairy Sci. 2005, 88, 2010–2016. [CrossRef] [PubMed]
7. Nonnecke, BJ; Kimura, K.; Goff, JP; Kehrli, ME, Jr. J. Dairy Sci. 2003, 86, 2359–2368. [CrossRef]
8. Habel, J.; Sundrum, A. Neusklađenost alokacije glukoze između različitih životnih funkcija u prijelaznom periodu mliječnih krava. Životinje 2020, 10, 1028. [CrossRef]
9. Horst, EA; Kvidera, SK; Baumgard, LH Pozvana recenzija: Utjecaj imunološke aktivacije na zdravlje i učinak krava u tranziciji – Kritička procjena tradicionalnih dogmi. J. Dairy Sci. 2021, 104, 8380–8410. [CrossRef]
10. Wathes, DC; Becker, F.; Buggiotti, L.; Crowe, MA; Ferris, C.; Foldager, L.; Grelet, C.; Hostens, M.; Ingvartsen, KL; Marchitelli, C.; et al. Povezanost između cirkulirajućih koncentracija IGF-1, statusa bolesti i transkriptoma leukocita kod mliječnih krava u ranoj laktaciji. Preživari 2021, 1, 147–177. [CrossRef]
11. Dimeloe, S.; Burgener, AV; Grahlert, J.; Hess, C. Metabolizam T-ćelija koji upravlja aktivacijom, proliferacijom i diferencijacijom; modularni pogled. Imunologija 2017, 150, 35–44. [CrossRef] [PubMed]
12. Loftus, RM; Finlay, DK Imunometabolizam: Ćelijski metabolizam pretvara imunološki regulator. J. Biol. Chem. 2016, 291, 1–10. [CrossRef] [PubMed]
13. Bauman, DE; Currie, WB Podjela nutrijenata tokom trudnoće i laktacije: Pregled mehanizama koji uključuju homeostazu i homeorhezu. J. Dairy Sci. 1980, 63, 1514–1529. [CrossRef] [PubMed]
14. Drackley, JK ADSA Foundation Scholar Award. Biologija muznih krava u periodu tranzicije: konačna granica? J. Dairy Sci. 1999, 82, 2259–2273. [CrossRef] [PubMed]
15. Jabbour, HN; Sales, KJ; Catalano, RD; Norman, JE Inflamatorni putevi u ženskom reproduktivnom zdravlju i bolesti. Reprodukcija 2009, 138, 903–919. [CrossRef]
16. Pascottini, OB; LeBlanc, SJ Modulacija imunološke funkcije u peripartumu goveđe materice. Theriogenology 2020, 150, 193–200. [CrossRef]
17. Sheldon, IM; Lewis, GS; LeBlanc, S.; Gilbert, RO Definiranje postporođajne bolesti materice kod goveda. Theriogenology 2006, 65, 1516–1530. [CrossRef]
18. Kuhla, B. Pregled: Proinflamatorni citokini i inflamacija hipotalamusa: Implikacije za nedovoljan unos hrane kod tranzicionih mliječnih krava. Animal 2020, 14, s65–s77. [CrossRef]
19. Ingvartsen, KL; Moyes, KM Faktori koji doprinose imunosupresiji kod mliječnih krava u periparturnom periodu. Jpn. J. Vet. Res. 2015, 63 (Suppl. 1), S15–S24.
20. Wathes, DC; Cheng, Z.; Salavati, M.; Buggiotti, L.; Takeda, H.; Tang, L.; Becker, F.; Ingvartsen, KI; Ferris, C.; Hostens, M.; et al. Odnosi između metaboličkih profila i ekspresije gena u jetri i leukocitima mliječnih krava u ranoj laktaciji. J. Dairy Sci. 2021, 104, 3596–3616. [CrossRef]
21. Pinedo, P.; Melendez, P. Poremećaji jetre povezani s metaboličkim neravnotežama kod mliječnih krava. Vet. Clin. N. Am. Food Anim. Prakt. 2022, 38, 433–446. [CrossRef] [PubMed]
22. Fenwick, MA; Fitzpatrick, R.; Kenny, DA; Diskin, MG; Patton, J.; Murphy, JJ; Wathes, DC Međusobne veze između negativnog energetskog bilansa (NEB) i regulacije IGF u jetri mliječnih krava u laktaciji. Domest. Anim. Endocrinol. 2008, 34, 31–44. [CrossRef] [PubMed]
23. Kobayashi, Y.; Boyd, CK; Bracken, CJ; Lamberson, WR; Keisler, DH; Lucy, MC Smanjena ribonukleinska kiselina receptora hormona rasta (GHR) u jetri goveda u periparturi je uzrokovana specifičnom regulacijom GHR 1A koja je povezana sa smanjenim faktorom rasta I. Endocrinology 1999, 140, 3947–3954. [CrossRef]
24. Kvidera, SK; Horst, EA; Abuajamieh, M.; Mayorga, EJ; Fernandez, MV; Baumgard, LH Potrebe za glukozom za aktivirani imunološki sistem kod krava Holstein u laktaciji. J. Dairy Sci. 2017, 100, 2360–2374. [CrossRef] [PubMed]
25. Cheng, Z.; Wylie, A.; Ferris, C.; Ingvartsen, KL; Wathes, DC; Gplus, EC Utjecaj prehrane i nivoa neesterificiranih masnih kiselina na globalne transkriptomske profile u cirkulirajućim mononuklearnim stanicama periferne krvi kod mliječnih krava u ranoj laktaciji. J. Dairy Sci. 2021, 104, 10059–10075. [CrossRef]
26. Wathes, DC; Fenwick, M.; Cheng, Z.; Bourne, N.; Llewellyn, S.; Morris, DG; Kenny, D.; Murphy, J.; Fitzpatrick, R. Utjecaj negativnog energetskog bilansa na cikličnost i plodnost visokoproduktivnih mliječnih krava. Theriogenology 2007, 68 (Suppl. 1), S232–S241. [CrossRef]
27. Santos, JE; Bisinotto, RS; Ribeiro, ES Mehanizmi koji leže u osnovi smanjene plodnosti kod anovularnih mliječnih krava. Theriogenology 2016, 86, 254–262. [CrossRef]
28. Pascottini, OB; Leroy, J.; Opsomer, G. Neprilagođenost prelaznom periodu i posljedice na plodnost mliječnih krava. Reprod. Dom. Anim. 2022, 57 (Suppl. 4), 21–32. [CrossRef]
29. Leroy, JL; Valckx, SD; Jordaens, L.; De Bie, J.; Desmet, KL; Van Hoeck, V.; Britt, JH; Marei, WF; Bols, PE Ishrana i metaboličko zdravlje majke u odnosu na kvalitet oocita i embrija: Kritički pogledi na ono što smo naučili iz modela mliječnih krava. Reprod. Fertil. Dev. 2015, 27, 693–703. [CrossRef]
30. Coffey, MP; Hickey, J.; Brotherstone, S. Genetski aspekti rasta holštajn-frizijskih mliječnih krava od rođenja do zrelosti. J. Dairy Sci. 2006, 89, 322–329. [CrossRef]
31. Wathes, DC; Cheng, Z.; Bourne, N.; Taylor, VJ; Coffey, MP; Brotherstone, S. Razlike između prvorotkinja i višerodnih mliječnih krava u međuodnosu između metaboličkih osobina, prinosa mlijeka i rezultata tjelesnog stanja u periparturnom periodu. Domest. Anim. Endocrinol. 2007, 33, 203–225. [CrossRef] [PubMed]
32. Little, MW; Wylie, ARG; O'Connell, NE; Welsh, MD; Grelet, C.; Bell, MJ; Gordon, A.; Ferris, CP Imunološki efekti promjene nivoa inkluzije koncentrata u ishrani na bazi silaže trave za krave Holstein Frizije u ranoj laktaciji. Animal 2019, 13, 799–809. [CrossRef] [PubMed]
33. Buggiotti, L.; Cheng, Z.; Salavati, M.; Wathes, CD; Genotip plus životna sredina, C. Poređenje transkriptoma u cirkulirajućim leukocitima u ranoj laktaciji između prvorodnih i višeporodnih krava pruža dokaze za promjene vezane za dob. BMC Genom. 2021, 22, 693. [CrossRef] [PubMed]
34. Cardoso, FC; Kalscheur, KF; Drackley, JK Pregled simpozijuma: Strategije ishrane za poboljšanje zdravlja, proizvodnje i plodnosti tokom perioda tranzicije. J. Dairy Sci. 2020, 103, 5684–5693. [CrossRef] [PubMed]
35. Ingvartsen, KL Bolesti vezane za ishranu i upravljanje kod krava u tranziciji. Anim. Feed Sci. Technol. 2006, 126, 175–213. [CrossRef]
36. Ferris, CP; Gordon, FJ; Patterson, DC; Mayne, CS; McCoy, MA Kratkoročno poređenje performansi četiri sistema proizvodnje mlijeka na pašnjacima za mliječne krave u jesenjem teljenju. Grass Forage Sci. 2003, 58, 8. [CrossRef]
37. Taylor, VJ; Cheng, Z.; Pushpakumara, PG; Beever, DE; Wathes, DC Odnosi između koncentracija insulinu sličnog faktora rasta-I u plazmi kod mliječnih krava i njihove plodnosti i prinosa mlijeka. Vet. Rec. 2004, 155, 583–588. [CrossRef]
38. LeBlanc, SJ Interakcije metabolizma, upale i zdravlja reproduktivnog trakta u postpartalnom periodu kod mliječnih goveda. Reprod. Domc. Anim. 2012, 47 (Suppl. 5), 18–30. [CrossRef]
39. Vailati-Riboni, M.; Kanwal, M.; Bugari, O.; Meier, S.; Priest, NV; Burke, CR; Kay, JK; McDougall, S.; Mitchell, MD; Walker, CG; et al. Skor tjelesnog stanja i ravan ishrane prepartum utiču na regulatore transkriptoma masnog tkiva metabolizma i inflamacije kod krava na ispaši tokom prelaznog perioda. J. Dairy Sci. 2016, 99, 758–770. [CrossRef]
40. Trevisi, E.; Minuti, A. Procjena urođenog imunološkog odgovora u peripartirne krave. Res. Vet. Sci. 2018, 116, 47–54. [CrossRef]
41. Druker, SA; Šišić, R.; van Straten, M.; Goshen, T.; Kedmi, M.; Raz, T. Dijagnoza citološkog endometritisa kod prvorodnih u odnosu na višerodne mliječne krave. J. Dairy Sci. 2022, 105, 665–683. [CrossRef] [PubMed]
42. Hamzeh-Cognasse, H.; Laradi, S.; Osselaer, JC; Cognasse, F.; Garraud, O. Amotosalen-HCl-UVA redukcija patogena ne mijenja metabolizam rastvorljivog CD40 liganda, Ox40 liganda i interkeukina-27 nakon skladištenja, citokina koji se općenito povezuju s ozbiljnim neželjenim događajima. Vox Sang. 2015, 108, 205–207. [CrossRef] [PubMed]
43. de Greeff, A.; Zadoks, R.; Ruuls, L.; Toussaint, M.; Nguyen, TK; Downing, A.; Rebel, J.; Stockhofe-Zurwieden, N.; Smith, H. Rani odgovor domaćina u mliječnoj žlijezdi nakon eksperimentalnog izazivanja Streptococcus uberis kod junica. J. Dairy Sci. 2013, 96, 3723–3736. [CrossRef] [PubMed]
44. Cheng, Z.; Chauhan, L.; Barry, AT; Abudureyimu, A.; Oguejiofor, CF; Chen, X.; Wathes, DC Infekcija virusom akutne goveđe virusne dijareje inhibira ekspresiju gena stimuliranih interferonom tau u endometriju goveda. Biol. Reprod. 2017, 96, 1142–1153. [CrossRef]
45. Schoggins, JW Interferonom stimulirani geni: šta sve oni rade? Annu. Rev. Virol. 2019, 6, 567–584. [CrossRef] [PubMed]
46. Ohto, U. Mehanizmi aktivacije i regulacije NOD-sličnih receptora zasnovani na strukturnoj biologiji. Front. Immunol. 2022, 13, 953530. [CrossRef]
47. Cheng, Z.; Palma-Vera, S.; Buggiotti, L.; Salavati, M.; Becker, F.; Werling, D.; Wathes, DC; Gplus, EC Transkriptomska analiza cirkulirajućih leukocita dobijenih tokom oporavka od kliničkog mastitisa uzrokovanog Escherichia coli u mliječnih krava Holstein. Životinje 2022, 12, 2146. [CrossRef]
49. Loria, V.; Dato, I.; Graziani, F.; Biasucci, LM Mijeloperoksidaza: Novi biomarker upale kod ishemijske bolesti srca i akutnih koronarnih sindroma. Mediat. Inflamm. 2008, 2008, 135625. [CrossRef]
50. Olivera, A.; Beaven, MA; Metcalfe, DD Mastociti signaliziraju njihovu važnost u zdravlju i bolesti. J. Allergy Clin. Immunol. 2018, 142, 381–393. [CrossRef]
50. Dickinson, SE; Griffin, BA; Elmore, MF; Kriese-Anderson, L.; Elmore, JB; Dyce, PW; Rodning, SP; Pristranost, profili FH transkriptoma u perifernim bijelim krvnim zrncima u vrijeme vještačke oplodnje razlikuju goveđe junice s različitim potencijalom plodnosti. BMC Genom. 2018, 19, 129. [CrossRef]
51. Van Meulder, F.; Van Coppernolle, S.; Borloo, J.; Rinaldi, M.; Li, RW; Chiers, K.; Van den Broeck, W.; Vercruysse, J.; Claerebout, E.; Geldhof, P. Egzocitoza granula granulizina i granzima B kao potencijalni ključni mehanizam u imunosti izazvanom vakcinom kod goveda protiv nematode Ostertagia ostertagi. Zaraziti. Immun. 2013, 81, 1798–1809. [CrossRef] [PubMed]
52. Taylor, JL; Brown, BL Strukturna osnova za disregulaciju sintaze aminolevulinske kiseline u bolesti ljudi. J. Biol. Chem. 2022, 298, 101643. [CrossRef] [PubMed]
53. Trapani, JA; Sutton, VR Granzyme B: Pro-apoptotičke, antivirusne i antitumorske funkcije. Curr. Opin. Immunol. 2003, 15, 533–543. [CrossRef] [PubMed]
54. Campanile, G.; Baruselli, PS; Limone, A.; D'Occhio, MJ Lokalno djelovanje citokina i imunih ćelija u komunikaciji između konceptusa i materice tokom kritičnog perioda ranog razvoja, vezivanja i implantacije embrija - Implikacije na preživljavanje embriona kod goveda: Pregled. Theriogenology 2021, 167, 1–12. [CrossRef] [PubMed]
55. Bougarne, N.; Weyers, B.; Desmet, SJ; Deckers, J.; Ray, DW; Staels, B.; De Bosscher, K. Molekularno djelovanje PPARalpha u metabolizmu lipida i inflamaciji. Endocr. Rev. 2018, 39, 760–802. [CrossRef]
57. Sobolev, VV; Čepourina, E.; Korsunskaya, IM; Geppe, NA; Chebysheva, SN; Soboleva, AG; Mezencev, A. Uloga transkripcionog faktora PPAR-gama u patogenezi psorijaze, ćelija kože i imunih ćelija. Int. J. Mol. Sci. 2022, 23, 9708. [CrossRef]
57. Song, S.; Attia, RR; Connaughton, S.; Niesen, MI; Ness, GC; Elam, MB; Hori, RT; Cook, GA; Park, EA Alfa receptor aktiviran proliferatorom peroksizoma (PPARalpha) i PPAR gama koaktivator (PGC-1alpha) induciraju karnitin palmitoiltransferazu IA (CPT-1A) preko nezavisnih genskih elemenata. Mol. Cell. Endocrinol. 2010, 325, 54–63. [CrossRef]
59. Ziouzenkova, O.; Plutzky, J. Metabolizam retinoida i odgovori nuklearnih receptora: Novi uvidi u koordiniranu regulaciju PPAR-RXR kompleksa. FEBS Lett. 2008, 582, 32–38. [CrossRef]
59. Espenshade, PJ; Hughes, AL Regulacija sinteze sterola kod eukariota. Annu. Rev. Genet. 2007, 41, 401–427. [CrossRef]
60. Van Meer, G.; Voelker, DR; Feigenson, GW Membranski lipidi: gdje su i kako se ponašaju. Nat. Rev. Mol. Cell. Biol. 2008, 9, 112–124. [CrossRef]
61. Aguilar-Ballester, M.; Herrero-Cervera, A.; Vinue, A.; Martinez-Hervas, S.; Gonzalez-Navarro, H. Utjecaj metabolizma kolesterola na funkciju imunoloških stanica i aterosklerozu. Nutrients 2020, 12, 2021. [CrossRef] [PubMed]
63. Mamedova, LK; Yuan, K.; Laudick, AN; Fleming, SD; Mashek, DG; Bradford, BJ Signalizacija receptora 4 sličnog Tollu potrebna je za indukciju ekspresije glukoneogenog gena palmitatom u ćelijama humanog karcinoma jetre. J. Nutr. Biochem. 2013, 24, 1499–1507. [CrossRef] [PubMed]
63. Soto-Heredero, G.; Gomez de Las Heras, MM; Gabande-Rodriguez, E.; Oller, J.; Mittelbrunn, M. Glikoliza-Ključni igrač u inflamatornom odgovoru. FEBS J. 2020, 287, 3350–3369. [CrossRef] [PubMed]
65. Kominsky, DJ; Campbell, EL; Colgan, SP Metaboličke promjene u imunitetu i upalama. J. Immunol. 2010, 184, 4062–4068. [CrossRef]
65. Afacan, NJ; Yeung, AT; Pena, OM; Hancock, RE Terapijski potencijal odbrambenih peptida domaćina u infekcijama otpornim na antibiotike. Curr. Pharm. Des. 2012, 18, 807–819. [CrossRef]
66. Auvynet, C.; Rosenstein, Y. Multifunkcionalni odbrambeni peptidi domaćina: Antimikrobni peptidi, mali, ali veliki igrači u urođenom i adaptivnom imunitetu. FEBS J. 2009, 276, 6497–6508. [CrossRef]
68. Hilchie, AL; Wuerth, K.; Hancock, RE Imunološka modulacija višestrukim kationskim odbrambenim (antimikrobnim) peptidima domaćina. Nat. Chem. Biol. 2013, 9, 761–768. [CrossRef]
68. Cheng, Z.; Buggiotti, L.; Salavati, M.; Marchitelli, C.; Palma-Vera, S.; Wylie, A.; Takeda, H.; Tang, L.; Crowe, MA; Wathes, DC; et al. Globalni transkriptomski profili cirkulirajućih leukocita kod krava u ranoj laktaciji s kliničkim ili subkliničkim mastitisom. Mol. Biol. Rep. 2021, 48, 4611–4623. [CrossRef]
69. Foley, C.; Chapwanya, A.; Callanan, JJ; Whiston, R.; Miranda-CasoLuengo, R.; Lu, J.; Meijer, WG; Lynn, DJ; O'Farrelly, C.; Meade, KG Integrisana analiza lokalnih i sistemskih promena koje prethode nastanku postporođajnog citološkog endometritisa. BMC Genom. 2015, 16, 811. [CrossRef]
70. Machado, VS; Silva, TH Adaptivni imunitet u postporođajnoj maternici: Potencijalna upotreba vakcina za kontrolu metritisa. Theriogenology 2020, 150, 201–209. [CrossRef]
71. Ley, K.; Hoffman, HM; Kubes, P.; Cassatella, MA; Zychlinsky, A.; Hedrick, CC; Catz, SD Neutrofili: Novi uvidi i otvorena pitanja. Sci. Immunol. 2018, 3, eaat4579. [CrossRef] [PubMed]
72. Wahl, SM; Feldman, GM; McCarthy, JB Regulacija adhezije leukocita i signalizacija kod upala i bolesti. J. Leukoc. Biol. 1996, 59, 789–796. [CrossRef] [PubMed]
73. Schubert, K.; Polte, T.; Bonisch, U.; Schader, S.; Holtappels, R.; Hildebrandt, G.; Lehmann, J.; Simon, JC; Anderegg, U.; Saalbach, A. Thy-1 (CD90) reguliše ekstravazaciju leukocita tokom upale. EUR. J. Immunol. 2011, 41, 645–656. [CrossRef] [PubMed]
74. Dreymueller, D.; Pruessmeyer, J.; Schumacher, J.; Fellendorf, S.; Hess, FM; Seifert, A.; Babendreyer, A.; Bartsch, JW; Ludwig, A. Metaloproteinaza ADAM8 podstiče regrutaciju leukocita in vitro i kod akutne upale pluća. Am. J. Physiol. Lung Cell. Mol. Physiol. 2017, 313, L602–L614. [CrossRef]
76. Kostelnik, KB; Barker, A.; Schultz, C.; Mitchell, TP; Rajeeve, V.; White, IJ; Aurrand-Lions, M.; Nourshargh, S.; Cutillas, P.; Nightingale, TD Dinamički promet i promet JAM-C je od suštinskog značaja za migraciju endotelnih ćelija. PLoS Biol. 2019, 17, e3000554. [CrossRef] [PubMed]
76. Stillie, R.; Farooq, SM; Gordon, JR; Stadnyk, AW Funkcionalni značaj iza ekspresije dva tipa IL-8 receptora na PMN. J. Leukoc. Biol. 2009, 86, 529–543. [CrossRef]
77. Bouton, AH; Riggins, RB; Bruce-Staskal, PJ Funkcije adapterskog proteina Cas: Konvergencija signala i određivanje ćelijskih odgovora. Oncogene 2001, 20, 6448–6458. [CrossRef]
78. Chen, X.; Cheng, Z.; Zhang, S.; Werling, D.; Wathes, DC Kombinovanjem studija asocijacija na nivou genoma i analiza podataka o diferencijalnoj ekspresiji gena identifikuju se geni kandidati koji utiču na mastitis uzrokovan dvama različitim patogenima kod mliječnih krava. Otvorite J. Anim. Sci. 2015, 5, 358–393. [CrossRef]
79. Chang, GW; Hsiao, CC; Peng, YM; Vieira Braga, FA; Kragten, NA; Remmerswaal, EB; van de Garde, MD; Straussberg, R.; Konig, GM; Kostenis, E.; et al. Adhezijski G protein spojen receptor GPR56/ADGRG1 je inhibitorni receptor u ljudskim NK ćelijama. Cell. Rep. 2016, 15, 1757–1770. [CrossRef]
80. Bi, J.; Tian, Z. Disfunkcija NK stanica i imunoterapija kontrolnih punktova. Front. Immunol. 2019, 10, 1999. [CrossRef]
82. Minuti, A.; Gallo, A.; Lopreiato, V.; Bruschi, S.; Piccioli-Cappelli, F.; Uboldi, O.; Trevisi, E. Utjecaj veličine legla na prepartalni metabolički i aminokiselinski profil kod kunića. Animal 2020, 14, 2109–2115. [CrossRef] [PubMed]
82. Crookenden, MA; Moyes, KM; Kuhn-Sherlock, B.; Lehnert, K.; Walker, CG; Loor, JJ; Mitchell, MD; Murray, A.; Dukkipati, VSR; Vailati-Riboni, M.; et al. Transkriptomska analiza cirkulirajućih neutrofila u peripartalnih mliječnih krava na ispaši pod metaboličkim stresom. J. Dairy Sci. 2019, 102, 7408–7420. [CrossRef] [PubMed]
84. Sharma, JN; Al-Omran, A.; Parvathy, SS Uloga dušikovog oksida u upalnim bolestima. Inflammofarmakologija 2007, 15, 252–259. [CrossRef] [PubMed]
84. Martino, MR; Gutierrez-Aguilar, M.; Yiew, NKH; Lutkewitte, AJ; Singer, JM; McCommis, KS; Ferguson, D.; Liss, KHH; Yoshino, J.; Renkemeyer, MK; et al. Utišavanje alanin transaminaze 2 u dijabetičkoj jetri ublažava hiperglikemiju smanjenjem glukoneogeneze iz aminokiselina. Cell Rep. 2022, 39, 110733. [CrossRef] [PubMed]
85. Tall, AR; Yvan-Charvet, L. Holesterol, upale i urođeni imunitet. Nat. Rev. Immunol. 2015, 15, 104–116. [CrossRef]
86. Wathes, D.; Cheng, Z.; Mareiy, W.; Fouladi-Nasht, A. Polinezasićene masne kiseline i plodnost kod ženki sisara: ažuriranje. CABI Rev. 2013, 8, 1–14. [CrossRef]
87. Alipour, A.; van Oostrom, AJ; Izraeljan, A.; Verseyden, C.; Collins, JM; Frayn, KN; Plokker, TW; Elte, JW; Castro Cabezas, M. Aktivacija leukocita lipoproteinima bogatim trigliceridima. Arterioscler. Thromb. Vasc. Biol. 2008, 28, 792–797. [CrossRef]
88. Castoldi, A.; Monteiro, LB; van Teijlingen Bakker, N.; Sanin, DE; Rana, N.; Corrado, M.; Cameron, AM; Hassler, F.; Matsushita, M.; Caputa, G.; et al. Sinteza triacilglicerola pojačava inflamatornu funkciju makrofaga. Nat. Commun. 2020, 11, 4107. [CrossRef]
89. Bell, AW Regulacija metabolizma organskih nutrijenata tokom tranzicije iz kasne trudnoće u ranu laktaciju. J. Anim. Sci. 1995, 73, 2804–2819. [CrossRef]
90. Moore, DAPSU; Varga, G. BUN i MUN: Ispitivanje azota uree u mliječnim govedima. Compendium 1996, 18, 712–720.
91. Wathes, DC; Bourne, N.; Cheng, Z.; Mann, GE; Taylor, VJ; Coffey, MP Višestruke korelacijske analize metaboličkih i endokrinih profila sa plodnošću krava prvorotki i višerodnih krava. J. Dairy Sci. 2007, 90, 1310–1325. [CrossRef] [PubMed]
92. Abe, R.; Donnelly, SC; Peng, T.; Bucala, R.; Metz, CN Fibrociti periferne krvi: put diferencijacije i migracija na mjesta rane. J. Immunol. 2001, 166, 7556–7562. [CrossRef] [PubMed]
93. Schreier, S.; Triampo, W. Populacija rijetkih ćelija koja cirkulira u krvi. Šta je to i za šta je dobro? Ćelije 2020, 9, 790. [CrossRef] [PubMed]
94. Lynn, AK; Yannas, IV; Bonfield, W. Antigenost i imunogenost kolagena. J. Biomed. Mater. Res. 2004, 71, 343–354. [CrossRef]
95. Roche, JR; Burke, CR; Crookenden, MA; Heiser, A.; Loor, JL; Meier, S.; Mitchell, MD; Phyn, CVC; Turner, SA Plodnost i tranzicijska mliječna krava. Reprod. Fertil. Dev. 2017, 30, 85–100. [CrossRef]
97. Galvao, KN; Flaminio, MJ; Brittin, SB; Sper, R.; Fraga, M.; Caixeta, L.; Ricci, A.; Guard, CL; Butler, WR; Gilbert, RO Povezanost između bolesti maternice i indikatora neutrofilnog i sistemskog energetskog statusa kod krava Holstein u laktaciji. J. Dairy Sci. 2010, 93, 2926–2937. [CrossRef]
97. Dahl, MO; Maunsell, FP; De Vries, A.; Galvao, KN; Risco, CA; Hernandez, JA Dokazi da mastitis može uzrokovati gubitak gravidnosti kod mliječnih krava: Sistematski pregled opservacijskih studija. J. Dairy Sci. 2017, 100, 8322–8329. [CrossRef]
98. Hansen, PJ; Soto, P.; Natzke, RP Mastitis i plodnost kod goveda-moguća uključenost upale ili imunološke aktivacije u embrionalni mortalitet. Am. J. Reprod. Immunol. 2004, 51, 294–301. [CrossRef]
99. Malinowski, E.; Gajewski, Z. Mastitis i poremećaji plodnosti kod krava. Pol. J. Vet. Sci. 2010, 13, 555–560.
100. Edmonson, AJ; Lean, IJ; Weaver, LD; Farver, T.; Webster, Džordžija Tabela za bodovanje tjelesnog stanja za krave holštajn. J. Dairy Sci. 1989, 72, 11. [CrossRef]
101. Larsen, T.; Rontved, CM; Ingvartsen, KL; Vels, L.; Bjerring, M. Aktivnost enzima i proteini akutne faze u mlijeku korišteni kao indikatori akutnog kliničkog mastitisa izazvanog E. coli LPS-om. Animal 2010, 4, 1672–1679. [CrossRef] [PubMed]
102. Krogh, MA; Hostens, M.; Salavati, M.; Grelet, C.; Sorensen, MT; Wathes, DC; Ferris, CP; Marchitelli, C.; Signorelli, F.; Napolitano, F.; et al. Varijacije između i unutar stada u biomarkerima krvi i mlijeka kod krava Holstein u ranoj laktaciji. Animal 2020, 14, 1067–1075. [CrossRef] [PubMed]
103. Buggiotti, L.; Cheng, Z.; Wathes, DC; Gplus, EC Mining nemapiranih očitavanja u goveđim RNA-Seq podacima otkriva prevalenciju virusa goveđeg herpesa-6 kod evropskih mliječnih krava i povezane promjene u njihovom fenotipu i transkriptomu leukocita. Virusi 2020, 12, 1451. [CrossRef] [PubMed]
104. Beltman, ME; Forde, N.; Furney, P.; Carter, F.; Roche, JF; Lonergan, P.; Crowe, MA Karakterizacija ekspresije gena endometrijuma i metaboličkih parametara kod goveđih junica koje daju održive ili neodržive embrije 7. dana nakon osjemenjavanja. Reprod. Fertil. Dev. 2010, 22, 987–999. [CrossRef] [PubMed]
