Abnormalnosti B ćelija i T ćelija kod pacijenata sa selektivnim nedostatkom IgA
Aug 09, 2023
Abstract
Pozadina
Selektivni nedostatak IgA (SIgAD) je najčešća urođena greška imuniteta sa gotovo nepoznatom etiologijom. Ova studija je imala za cilj da ispita kliničke dijagnostičke i prognostičke vrednosti podskupina i funkcije limfocita kod simptomatskih pacijenata sa SIgAD.
Metode
U ovu studiju uključeno je ukupno 30 dostupnih pacijenata sa SIgAD-om iz iranskog registra i 30 zdravih kontrolnih osoba koje odgovaraju spolu. Analizirali smo periferne podskupine B i T ćelija i test proliferacije T ćelija pomoću protočne citometrije kod pacijenata sa SIgAD sa blagim i teškim kliničkim fenotipovima.
Rezultati
Naši rezultati su ukazali na značajno povećanje naivnih i prelaznih B ćelija i snažno smanjenje B-ćelija sličnih marginalnim zonama i promenjenih memorijskih B-ćelija kod pacijenata sa SIgAD-om. Otkrili smo da su naivne i centralne memorijske CD4+ podskupove T ćelija, kao i Th1, Th2 i regulatorne T ćelije, značajno smanjene. S druge strane, došlo je do značajnog smanjenja podskupova CD8+ T ćelija centralne i efektorske memorije, dok su proporcije oba (CD4+ i CD8+) terminalno diferencirane efektorske memorijske T ćelije (TEMRA) bile su značajno povišene kod naših pacijenata. Iako su neke podgrupe T ćelija kod teškog SIgAD-a bile slične, smanjenje B ćelija u marginalnim zonama i promenjene memorije i povećanje CD21 niskih B ćelija kod pacijenata sa teškim SIgAD-om bilo je blago istaknuto. Štaviše, aktivnost proliferacije CD4+ T ćelija bila je snažno poremećena kod pacijenata sa SIgAD sa teškim fenotipom.
Zaključak
Pacijenti sa SIgAD-om imaju različite ćelijske i humoralne nedostatke. Stoga bi procjena T ćelija i B ćelija mogla pomoći u boljem razumijevanju heterogene patogeneze i procjeni prognoze bolesti.
Ključne riječi
Urođene greške imuniteta, primarna imunodeficijencija, selektivni nedostatak IgA, podskupine B ćelija, podskupovi T ćelija, protočna citometrija, proliferacijaesej

cistanche tubulosa-poboljšava imuni sistem

ekstrakt cistanche
Uvod
Selektivni nedostatak IgA (SIgAD) je najčešći primarni poremećaj imunodeficijencije (PID) ili urođene greške imuniteta (IEI), identificiran prema koncentraciji IgA u serumu ispod 7 mg/dL i normalnim koncentracijama IgG i IgM kod pacijenata starijih od četiri godine. . Većina pacijenata sa SIgAD-om je asimptomatska, iako neki od njih imaju različite kliničke manifestacije, uključujući infekcije gastrointestinalnog i respiratornog trakta, alergijske bolesti i autoimune poremećaje. Prijavljena je progresija bolesti do uobičajene varijabilne imunodeficijencije (CVID) u odabranoj grupi pacijenata sa SIgAD sa nedostatkom IgG podklasa ili autoimunim poremećajima [1]. Još uvijek nisu prijavljeni specifični uzroci za patogenezu SIgAD. Međutim, u neriješenim slučajevima otkriveni su defekti u procesu rekombinacije prekidača klase IgA (CSR), proizvodnje i izlučivanja IgA, kao i dugotrajnog preživljavanja IgA, promijenjenih memorijskih B ćelija i plazma ćelija pacijenata sa SIgAD [2 ]. Defekti u ovim imunološkim procesima povezani su sa abnormalnostima u limfocitima pacijenata sa SIgAD. Stoga bi procjena limfocita, posebno podskupina B ćelija i T ćelija, mogla biti vrijedna i korisna. Nekoliko studija je pokazalo abnormalnosti B ćelija i T ćelija u nekim grupama pacijenata sa SIgAD [3, 4]. Što se tiče podskupova B ćelija, zabilježeno je smanjenje broja promijenjenih memorijskih B ćelija, IgA plazma ćelija i prelaznih IL-10+ regulatornih B ćelija pacijenata sa SIgAD [5–8]. S druge strane, prijavljen je defekt u nekim podskupovima T ćelija slučajeva SIgAD koji je povezan sa nedovoljnim B ćelijama koje proizvode IgA [5, 8, 9]. Protočna citometrijska imunofenotipizacija može igrati važnu ulogu u dijagnozi, prognozi, klasifikaciji i liječenju pacijenata sa SIgAD-om. Stoga smo po prvi put imali za cilj da istražimo glavne subpopulacije B i T limfocita zajedno sa evaluacijom funkcije T ćelija, da razjasnimo korelaciju između imunoloških karakteristika i kliničkih manifestacija kod simptomatskih pacijenata sa SIgAD.
Materijal i metode
Pacijenti
Ukupno 30 dostupnih simptomatskih pacijenata sa SIgAD-om (iz iranskog IEI registra [10, 11]) i 30 zdravih kontrola (HC) podudarnog po spolu uključeno je u ovu studiju. Nakon kliničkih i laboratorijskih procjena potvrđeno je da HC nemaju imunodeficijencije ili bilo kakve osnovne bolesti. Pacijenti su upućeni u Dječiji medicinski centar (Pedijatrijski centar izvrsnosti pri Teheranskom univerzitetu medicinskih nauka, Teheran, Iran). Svim pacijentima je dijagnostikovan SIgAD prema Evropskom društvu za imunodeficijencije [12]. Studiju je odobrio Etički komitet Medicinskog univerziteta u Teheranu i dobijen je pismeni informirani pristanak svih pojedinaca (IR.TUMS.VCR.REC.1396.2018). Demografske, kliničke manifestacije i imunološki podaci pacijenata dokumentovani su u obliku upitnika.
Klasifikacija pacijenata
Da bi se uporedili demografski, klinički i imunološki podaci, pacijenti su kategorizirani u dvije grupe teške i blage (na osnovu kliničkih manifestacija), kao i srodne i nesrodničke grupe (na osnovu roditeljskog krvnog srodstva). Minimalni kriteriji uključivanja za pacijenta koji bi se smatrao simptomatičnim bili su deset znakova upozorenja Jeffrey Modell Foundation. Bolesnici su podijeljeni u dvije grupe blage i teške, jer su pacijenti sa teškim infekcijama (npr. krvotok, centralni nervni sistem i duboke infekcije poput osteomijelitisa i artritisa), autoimunom ili malignom kategorizacijom kategorizirani u tešku grupu, i drugim komplikacijama. smatrani su blagom grupom. Budući da su pneumonija i druge respiratorne infekcije česte kod pacijenata sa SIgAD-om i željeli smo je provjeriti kao parametar između teških i blažih grupa, pa je nismo kategorizirali u tešku grupu.

Prednosti suplemenata cistanche-kako ojačati imuni sistem
Kliknite ovdje za pregled proizvoda Cistanche Enhance Immunity
【Tražite više】 Email:cindy.xue@wecistanche.com / Whats App: 0086 18599088692 / Wechat: 18599088692
Analiza podskupova limfocita
Mononuklearne ćelije periferne krvi (PBMC) su izdvojene iz uzoraka krvi od 8 ml prikupljenih u epruvetama sa natrijum heparinom korišćenjem Ficoll-Hypaque centrifugiranja sa gradijentom gustine na 600 g tokom 25 minuta na 22 stepena. Za ekstracelularno bojenje, PBMC su podijeljeni u 5-frakcije panela i obojeni 20 minuta na 2-8 stepeni na tamnom mjestu sa svakim koktelom koji je sadržavao monoklonska antitijela u optimalnim koncentracijama. Ploča B1 je korištena za određivanje naivne (CD19+CD27−IgM+IgD+), IgM memorije (CD19+CD27+ IgM++IgD−), prebacivanja memorija (CD19+CD27+IgM−IgD−) i B ćelije slične marginalnim zonama (CD19+CD27+IgM++IgD+). Panel B2 je korišten za identifikaciju CD21low B ćelija (CD19+CD21−/lowCD38−/lowIgM+++), plazmablast (CD19+CD21−/lowCD38++/{ {34}}IgM−) i prelazne B ćelije (CD19+CD21+CD38++IgM+). T1 panel je korišten za klasifikaciju naivne (CD4+ ili CD8+ i CD45RA+CCR7+), efektorske memorije (CD4+ ili CD8+ i CD45RA−CCR7−), centralna memorija (CD4+ ili CD8+i CD45RA−CCR7+) i TEMRA (terminalno diferencirana efektorska memorija) T ćelije (CD4+ ili CD8+ i CD45RA+CCR7−). Te T2 panel je korišten za klasifikaciju regulatornih T ćelija (TregsCD4+CD25+FOXP3+CD127−/low). Za intracelularno bojenje, nakon bojenja površinskih molekula, oni su fiksirani i permeabilizirani kroz FOXP3/Permeabilizacijski pufer (eBioscience, US) prema uputama proizvođača za sljedeće: Anti-Human FOXP3 (PE), Anti-Human IL{{67} } (PE), Anti-Human IL-4 (APC) i Anti-Human IFN- (FITC). Sva antitijela i kontrole izotipova kupljena su od eBioscience, američke korporacije. Za procjenu T pomoćnih ćelija (uključujući T1, T2 i T17), 1×106 (ćelija/mL) PBMC-a je kultivirano u mediju za ćelijsku kulturu Roswell Park Memorijalnog instituta (RPMI 1640), nakon čega je uslijedila stimulacija s forbol miristat acetatom (PMA). , 50 ng/mL, Sigma-Aldrich, SAD) / jonomicin (1 ug/mL, Sigma-Aldrich), i u prisustvu brefeldina (5 ug/mL, eBioscience). Zatim su ćelije inkubirane na 37 stepeni u inkubatoru sa 5% CO2 i 95% vlažnosti tokom 5 h. Stimulirane ćelije su isprane fiziološkim rastvorom puferovanim fosfatom (PBS) i izvršeno je površinsko bojenje anti-humanim CD4 (PerCp)-Cy5.5. Intracelularna antitijela za bojenje citokina (anti-IFN-FITC, anti-IL-17 PE i anti-IL-4 APC za procjenu T podskupova i anti-FoxP3 PE za procjenu Treg) su dodana i inkubirana na sobnoj temperaturi 30 min. Ćelije su isprane puferom za permeabilizaciju i resuspendirane u hladnom puferu za bojenje, a broj je određen korištenjem BD FACSCalibur protočnog citometra (BD Biosciences) (Dodatna datoteka 1: Tabela S1). Strategija gatinga je slična našoj prethodnoj studiji [13, 14].
Test proliferacije T-ćelija
Da bi se procijenila proliferacija T ćelija, PBMC su uzgajani sa fluorescentnim 5,6-karboksifluorescein sukcinimidil esterom (CFSE, Biolegend, US). Osnovni rastvor CFSE je pripremljen otapanjem CFSE u dimetil sulfoksidu (DMSO) u koncentraciji od 5 mM/L, na osnovu uputstava proizvođača. Ova zaliha je zamrznuta u malim alikvotima kako bi se spriječili pretjerani ciklusi smrzavanja i odmrzavanja. CFSE je dodan u transverzalnu epruvetu Falcon koja sadrži 500 μL suspenzije PBMC (5×106 ćelija/mL) u mediju za ćelijsku kulturu RPMI 1640 koji sadrži 10% FBS (fetalni goveđi serum, Biosera, Francuska) sa konačnom koncentracijom od 5 μM i 2 mM L-glutamin, 100 U/mL penicilina i 100 ug/mL streptomicina (Lymphosep; Biosera, Francuska). Cev se brzo okretala i vorteksirala kako bi se osigurala homogena disperzija. Nakon obeležavanja, ćelijska suspenzija je inkubirana 5 minuta na 37 stepeni. Zatim je 9 mL RPMI1640 koji sadrži 10% FBS dodano u ćelijsku suspenziju i centrifugirano je na 500 g 5 min. Ćelije su isprane tri puta i dodat je 1 mL RPMI1640 sa 10% FBS. Što se tiče specifične stimulacije i proliferacije T ćelija, anti-CD3 antitelo (1 µg/ml) je dodato u 500 μL sterilnog PBS-a, a ploča je inkubirana na 37˚C tokom 2 h. Obložena ploča je dva puta isprana sterilnim PBS-om i direktno su dodane označene ćelije, i na kraju je dodano anti-CD28 antitelo (2 µg/ml) kao stimulans za T ćelije. Ploča je inkubirana na 37 ºC u inkubatoru sa 5% CO2 i 95% vlage 96 h [15–17]. Nestimulisani bunar se smatrao kontrolom neproliferativnih ćelija. Nakon 96 h, ćelije su sakupljene i isprane. Nakon bojenja sa Anti Human CD4 (PerCPCy5.5), ćelije su na kraju analizirane pomoću BD FACSCalibur™ protočnog citometra i CellQuest Pro softvera (BD, Biosciences, San Jose, Kalifornija, SAD). Analiza proliferacije obavljena je poređenjem tri kriterijuma, uključujući postotak podijeljenih ćelija (% podijeljenih), prosječan broj ćelijskih dioba kojima se ćelija podvrgava (Indeks diobe) i prosječan broj ćelijskih dioba koje se javljaju u cijeloj primarnoj ćelijskoj populaciji (Indeks proliferacije) softvera FlowJo 7.6.
Statistička analiza
SPSS softver (Windows verzija 16.0; SPSS Inc., Chicago, IL, US) je korišten za statističku analizu. Koristili smo Kolmogorov-Smirnov test da procijenimo da li su podaci normalno raspoređeni. Nalazi su predstavljeni kao medijane (interkvartilni raspon [IQR], predstavljen kao raspon sa 25.–75. percentilima) vrijednosti. Za poređenje je korišten hi-kvadrat test ili Fisherov egzaktni test. Za poređenje više od dvije grupe, ako je distribucija podataka bila normalna, korištena je ANOVA, a ako je distribucija podataka bila nenormalna, korišten je Kruskal Wallisov test. Razlike su se smatrale statistički značajnim za P-vrijednosti koje su bile<0.05.

cistanche koristi za muškarce - jača imuni sistem
Rezultati
Demografski, imunološki i klinički nalazi
Među svim registrovanim iranskim pacijentima sa SIgAD-om, 30 dostupnih pacijenata (23 muškarca i sedam žena) je regrutovano u ovoj studiji. Srednja (IQR) starost pacijenata bila je 11 (7,3-16) godina u vrijeme studije. Roditeljsko srodstvo bilo je prisutno kod 16 (53,3%) pacijenata. Pneumonija (42,3%) bila je najčešća klinička manifestacija kod ispitivanih pacijenata, a malignitet u ovoj kohorti nije dijagnosticiran. Demografske, kliničke i imunološke karakteristike pacijenata sumirane su u tabeli 1. Nakon kategorizacije pacijenata na osnovu teških i blagih fenotipova, upoređeni su demografski, klinički i imunološki podaci (Tabela 1, Slika 1). Kod pacijenata sa teškim fenotipovima bilo je više respiratornih komplikacija nego u blažoj grupi. Ostali parametri nisu pokazali značajnu razliku. Ista poređenja su obavljena kod pacijenata sa i bez krvnog srodstva, a nijedna od njih nije imala značajnu razliku. Nasuprot tome, pacijenti sa blagim fenotipovima su pokazali nešto veću stopu alergija i gastrointestinalnih manifestacija sa povećanim nivoom IgE u serumu, što ukazuje na povećano prebacivanje na proizvodnju IgE.
Tabela 1. Poređenje demografskih, kliničkih i imunoloških podataka pacijenata sa SIgAD-om s teškim i blagim fenotipovima


Slika 1. Poređenje kliničkih manifestacija između teškog i blagog SIgAD-a
Podskupovi B-ćelija
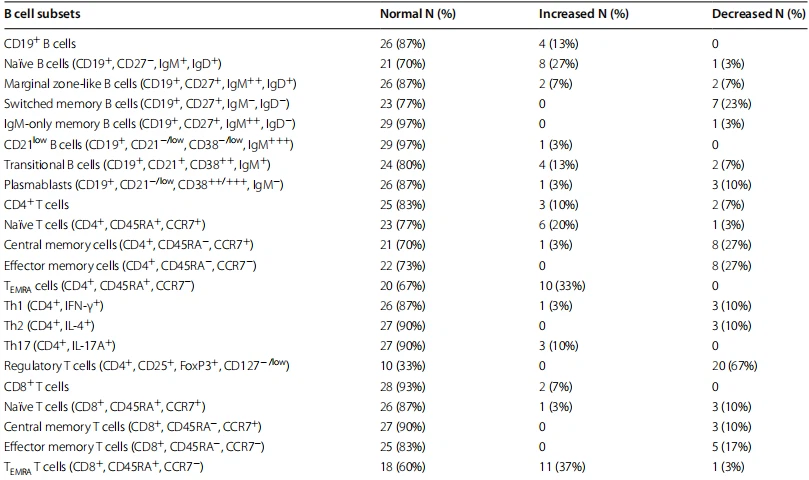
Pacijenti sa SIgAD-om pokazali su značajno povećanu učestalost CD{{0}} B-ćelija [11,2% (9,4–13.07%) naspram 7,2% (6–8,6%), p < 0.001], sa povećanim naivnim B-ćelijama [71% (63,7-80%) naspram 66,5% (56,2-71,1%), p=0}.036] i prelaznim B-ćelijama [ 8% (3,6–13,5%) naspram 4,8% (2,6–9,5%), p=0.032] u poređenju sa HC. Nasuprot tome, procenat B-ćelija sličnih marginalnim zonama [2,3% (2–3,5%) naspram 3,4% (2,3–4,8%), p=0.022) i B-ćelija sa komutacijom memorije [3,5% (1,9 –5,5%) naspram 6% (3,5–8,4%), p=0.006] su bili značajno niži od HC. Međutim, smanjena memorija samo IgM i plazmablasti i povećane CD21low B-ćelije kod pacijenata od onih u HC nisu bile značajne (slika 2). Zanimljivo je da su neka poređenja bila značajna između kliničkih grupa pacijenata. Procenat CD19+ B ćelija u blagim i teškim fenotipovima bio je značajno veći od HC [11,6% (8,7–13) naspram 7,2% (6–8,6), p < 0,0001, 10,8% (9,6–13,2) ) naspram 7,2% (6–8,6), p < 0,0001], respektivno. Pacijenti sa teškim SIgAD-om pokazali su značajno povećanje procenta CD21 niskih B-ćelija [1,5% (1–2,2) naspram 2,7% (1,6–5,6), p=0.025] i značajno smanjenje procenta podskupova B ćelija marginalne zone i komutiranih memorijskih ćelija [3,4% (2,3–4,8) naspram 2,2% [2, 3], p=0.040, 6% (3,5–8,4) naspram 2,7% ( 1.7–4.7), p=0.003], respektivno. Procenat prelaznih B ćelija kod pacijenata sa blagim SIgAD bio je veći od HC [10,7% (3,9–13,8) naspram 4,8% (2,6–9,5), p=0.047] (Sl. 3). Procenat pamćenja samo IgM bio je značajno veći kod pacijenata sa srodstvom nego kod onih bez krvnog srodstva. Takođe smo kategorisali učestalost podskupova B ćelija pacijenata sa SIgAD u tri kategorije: normalna, smanjena i povećana na osnovu normalnog opsega HC (tabela 2). Na osnovu ove analize, najveći pad u podskupovima B ćelija odnosi se na B-ćelije sa promenjenom memorijom (23%), dok se najveći porast odnosi na naivne B ćelije (27%) kod pacijenata sa SIgAD-om. Osim povećanih CD21low B-ćelija kod pacijenata sa teškim SIgAD u poređenju sa pacijentima sa blagim SIgAD.

Slika 2 Kvantitativna analiza procenta podskupine B ćelija i T ćelija kod pacijenata sa SIgAD i zdravih kontrola. Medijan je predstavljen horizontalnom linijom. Podaci su analizirani korištenjem Mann-Whitney U testa. *str<0.05, statistical significance between patients and HCs. HC Healthy control
Podskupovi T-ćelija
Odvajanje podskupa CD4+ T ćelija otkrilo je značajno smanjenje ukupnih CD4+ T ćelija [36,5% (30,8–41,2%) naspram 40,1% (37,3–47,2%), p{{14 }}.038)], centralne memorijske ćelije [11% (7,3–13,1%) naspram 24,5% (16–29%), p<0.0001), T1 [7.7% (5.2–9.9%) vs. 12% (7.8–16%), p=0.002], T2 [0.3% (0.2–0.4%) vs. 0.6% (0.4–1.3%), p<0.0001] and Tregs [0.3% (0.03–0.7%) vs. 1.4% (1.1– 1.6%), p<0.0001] in patients compared with HCs. Oppositely, the percentage of TEMRA [9.5% (5.7–16.4%) vs. 2% (1.3–6.2%), p<0.0001] was meaningfully higher than HCs. Moreover, decreased effector memory and T17, and increased naïve helper T cells in patients in comparison with HCs were not significant (Fig. 2). Regarding the percentage of CD8+ T cell subsets, central memory [0.6% (0.3–0.8%) vs. 3% (2–6%), p<0.0001] and effector memory [12.3% (7.6–22.1%) vs. 23.9% (19.5– 27.2%), p<0.0001] were markedly diminished in patients compared with HCs. On the other hand, the percentage of cytotoxic TEMRA [44.1% (28.4–55.7%) vs. 24.4% (20– 31%), p<0.0001] was significantly higher than HCs. However, increased total CD8+ T cells and decreased naïve CD8+ T cells were not significant in patients compared to those in HCs (Fig. 2). Regarding the comparison of the percentage of CD8+ T cells subsets between severe SIgAD patients with HCs, naïve T cells, effector, and central memory cells demonstrated a significant reduction. Also, there was a significant decrease in the percentage of total CD4+ T-cells, central memory, T1, T2, and regulatory T cells, whereas TEMRA in both CD4+ and CD8+ T cells demonstrated an increase. On the other hand, the percentage of effector and central memory cells within CD8+ T cells, as well as central memory, TEMRA, T1, and regulatory T cells within CD4+ T cell subsets demonstrated a significant decrease in mild forms of SIgAD compared to HCs. In contrast, we found an increase in TEMRA CD8+ T cells and T2 CD4+ T cells in mild patients compared to controls (Fig. 3). Comparisons of the percentages of all T cell subsets between SIgAD patients with and without consanguinity have not indicated any significant difference. We also categorized the frequency of T cell subsets of SIgAD patients into three categories: normal, decreased, and increased based on a normal range of HCs (Table 2). Based on this analysis, the most decrease in T cell subsets is related to Tregs (67%), while the most increase is related to CD8+ TEMRA (37%) in SIgAD patients. Flow cytometry results of B cell and T cell subsets in 30 SIgAD patients have shown separately in Additional file 1: Tables S2 and S3. To evaluate the impact of the T cell subset on the switching process of B cells and the production of different Ig subtypes we performed a correlation analysis. Surprisingly only IgG but not IgM and IgE were significantly associated with specific T cell subsets (negative association with naïve CD4 and naïve CD8 T cells and positive association with CD4+ TEM and T17 cells, Additional file 1: Table S4) indicating the independent association of IgM to IgE from co-stimulation of T cell subsets in our patient cohorts. Moreover, correlation analysis of absolute counts and percentage of subsets should significant direct correlation in all measured parameters (Additional file 1: Table S5).

Slika 3 Kvantitativna analiza procenta podskupine B ćelija i T ćelija kod pacijenata sa teškim i blagim SIgAD-om. Medijan je predstavljen horizontalnom linijom. Podaci su analizirani korištenjem Mann-Whitney U testa. *str<0.05, statistical signifcance between severe and mild patien
Tabela 2 Distribucija normalnih, povećanih i smanjenih proporcija podskupina T ćelija i B ćelija kod svih pacijenata sa SIgAD. N=30
Proliferacija T ćelija
Podaci dobijeni od kultura označenih sa CFSE analizirani su kako bi se kvantifikovala proliferacija CD4+ T ćelija. Nije bilo značajne razlike u indeksu podjele (DI), indeksu proliferacije (PI) i postotnoj podijeljenosti (PD) između pacijenata sa SIgAD i HC (slika 4). Zanimljivo, kada smo uporedili ove indekse između pacijenata sa SIgAD sa teškim i blagim fenotipovima, otkrili smo da je medijan DI i PD kod pacijenata sa teškim SIgAD u poređenju sa blagim slučajevima značajno poništen [0.1 (0 .08–0.4) vs. 0.5 (0.3–0.8), p=0.019 i 12.2 (8.4– 26,4) naspram 42,5 (26,8–52,6), p=0.009, respektivno]. Međutim, nije bilo značajne razlike u PI između teških i blagih grupa (slika 4). S druge strane, poređenja DI, PI i PD između SIgAD pacijenata sa i bez krvnog srodstva nisu bila značajna.
Slika 4 Poređenje indeksa proliferacije T limfocita kod pacijenata sa teškim i blagim SIgAD-om. Medijan je predstavljen horizontalnom linijom. *str<0.05, statistical significance between severe and mild patients

Diskusija
SIgAD je najrasprostranjeniji IEI sa različitim kliničkim manifestacijama. Ovi pacijenti imaju različit spektar kliničkih manifestacija. U skladu s tim, od pomoći su imunološka ispitivanja kod pacijenata s različitim spektrom kliničkih manifestacija. Najčešća klinička manifestacija kod IEI, posebno kod SIgAD-a, su rekurentne respiratorne infekcije [18–20]. Kao najčešću komplikaciju kod naših registrovanih simptomatskih pacijenata utvrdili smo upalu pluća. Rekurentne respiratorne infekcije obično se manifestiraju u obliku infekcija gornjih dišnih puteva i mogu ostati nedijagnosticirane nekoliko godina; međutim, neki pacijenti sa SIgAD-om manifestiraju teže fenotipove kao što su bronhiektazije ili obliterirani bronhiolitis, što zahtijeva imunološko ispitivanje kod ovih pacijenata [21]. S obzirom na to da su rekurentne respiratorne infekcije prijavljene kao najvažniji uzrok morbiditeta i smrti kod djece s IEI, posebno primarnih nedostataka antitijela [22, 23], rana dijagnoza i liječenje respiratornih poremećaja povezanih sa SIgAD-om su vrlo važni [24, 25]. . Ukazano je da su abnormalnosti u podskupinama B ćelija uočene kod nekih pacijenata sa SIgAD [3, 4]. Naši rezultati su pokazali značajno povećanje naivnih i prelaznih B ćelija i snažno smanjenje B-ćelija sličnih marginalnim zonama i preklopljenih memorijskih B-ćelija. Ovaj abnormalni obrazac B-ćelija ukazuje na defekte u terminalnim fazama diferencijacije B-ćelija, slično kao kod pacijenata sa CVID-om [26]. S obzirom da CVID i SIgAD dijele gotovo sličnu genetsku pozadinu i da se mogu akumulirati kao više slučajeva unutar porodice, ova sličnost je predvidljiva. Općenito, više od polovine pacijenata sa IEI registrovanim u iranskom registru ima srodstvo s roditeljima, ali je ova stopa još uvijek manje uobičajena kod pacijenata sa SIgAD-om. Kod SIgAD iranskih pacijenata u poređenju sa zapadnim pacijentima, krvno srodstvo je češće. Iako monogenetski uzroci mogu postojati, oni još uvijek nisu identificirani uprkos sekvenciranju sljedeće generacije kod nekoliko pacijenata [27]. Otkrili smo smanjenje broja B-ćelija sličnih marginalnim zonama i promijenjenih memorijskih B-ćelija, posebno kod pacijenata sa teškim SIgAD-om, kao što je ranije objavljeno [28]. Nedavno smo izvijestili o sličnom smanjenju B-ćelija sličnih marginalnim zonama i promijenjenih memorijskih B-ćelija kod pacijenata sa CVID-om [14].

Prednosti suplementa cistanche-povećavaju imunitet
S druge strane, iako smo primijetili značajno smanjenje promijenjene memorije kod pacijenata sa ataksijom teleangiektazijom (AT), ali je uočen nagli porast B ćelija sličnih marginalnim zonama [29]. Pacijenti sa SIgAD-om, posebno grupa pacijenata sa teškim kliničkim manifestacijama (ponavljajuća i intenzivna infekcija i autoimunost), imaju niže promijenjene memorijske B-ćelije [28, 30, 31]. Pretpostavlja se da je smanjenje subpopulacije B-ćelija s promijenjenom memorijom uzrokovano defektima u nivou procesa rekombinacije promjene klase antitijela (CSR), uzrokovanih enzimskim nedostatkom, ili abnormalnostima u mrežama citokina i njihovih receptora [28]. Neki pacijenti sa SIgAD-om sa teškim fenotipom napreduju u CVID, što odražava ovu podgrupu SIgAD-a, može dijeliti sa CVID-om zajedničku imunološku patogenezu, posebno u razvoju CSR koraka. U skladu s tim, B-ćelije s promijenjenom memorijom smatraju se dijagnostičkim biomarkerom kod pacijenata [28]. Međutim, učestalost promijenjenih memorijskih B-ćelija je normalna među djecom u našoj studijskoj populaciji, a smanjenje je uočeno više kod odraslih pacijenata; što sugerira da starenje vjerovatno dovodi do progresije SIgAD u CVID, posebno kod pacijenata sa teškim kliničkim manifestacijama (podaci nisu prikazani). S druge strane, B ćelije marginalne zone su specijalizirana populacija B stanica koje proizvode IgM za zaštitu od infekcija, posebno inkapsuliranih bakterija [32]. Iako su prethodne studije pokazale da se broj B ćelija sličnih marginalnim zonama kod pacijenata sa SIgAD-om nije razlikovao od normalnih kontrola [33], ipak smo dobili značajno smanjenje B ćelija sličnih marginalnim zonama u našim slučajevima, slično prethodni izvještaj kod pacijenata sa KVID-om [34]. Smanjenje marginalnih podskupina B ćelija kod drugih pacijenata sa defektima u proizvodnji antitela može biti povezano sa povećanim rizikom od infekcije kao što je upala pluća i smanjenje nivoa IgM u serumu, slično kao kod pacijenata sa CVID [35]. Pronašli smo povećane CD21low B ćelije u poređenju sa kontrolom, uglavnom kod pacijenata sa teškim SIgAD. Prethodne studije su prijavile povećanje broja CD21low B ćelija kod pacijenata sa SIgAD [3] i CVID [36], kao i kod drugih autoimunih bolesti [37]. Nedavno je također zabilježeno povećanje CD21low kod AT pacijenata [29]. Povećanje broja CD21low ćelija direktno je povezano ne samo sa autoimunitetom već i sa infekcijom [36]. S druge strane, kronična izloženost virusnoj infekciji može dovesti do konverzije antigen-reaktivnih B ćelija u CD21low B ćelije bez reakcije [38]. Da bi se razjasnio uzrok proširenih CD21low B ćelija; potrebno je izvršiti dalja istraživanja za ovu subpopulaciju B ćelija. S obzirom na visoku subpopulaciju CD21low B ćelija u CVID pacijenata i progresiju nekih pacijenata sa SIgAD u CVID, teška grupa pacijenata sa SIgAD sa povećanim CD21low B ćelijama će vjerojatnije razviti CVID. Stoga im je potrebno redovnije praćenje kako bi se procijenio tok bolesti. Tranzicione B ćelije su u srednjoj fazi razvoja između nezrelih ćelija koštane srži i zrelih B ćelija u slezeni [39]. U ovoj studiji uočili smo značajno povećanje prelaznih B ćelija kod naših pacijenata sa SIgAD, posebno kod pacijenata sa teškim SIgAD, iako je broj prelaznih B ćelija kod dece sa SIgAD bio normalan (podaci nisu prikazani). Nedavno smo uočili značajno smanjenje AT prelaznih B ćelija [29]. Za razliku od prethodnih studija koje su pokazale smanjenje tranzicijskih B ćelija [8, 28, 40], odrasli pacijenti su ukazivali na blago povećanje tranzicijskih B ćelija. Štaviše, Lemarquis et al. pokazalo smanjenje funkcionalne aktivnosti prelaznih B ćelija na osnovu proizvodnje IL-10 i CpG stimulacije [40]. S obzirom na defekt u terminalnim stadijumima B-ćelija u SIgAD-u, čini se da je povećanje prelaznih B ćelija i naivnih B ćelija naših pacijenata posledica kompenzacionog mehanizma koji povećava rani razvoj B ćelija. S obzirom na različite rezultate naše studije i drugih, čini se da je ova razlika posljedica različitih procesa selekcije, jer su svi naši pacijenti bili simptomatski, dok su drugi proučavali heterogeno asimptomatske i simptomatske SIgAD pacijente. Što se tiče podskupova T ćelija, uočili smo smanjenje ukupnog broja CD4+ T ćelija, T1, T2 i Treg ćelija, i povećanje TEMRA u CD4+ i CD8+ ćelijama. U skladu sa našim rezultatima, prethodne studije su pokazale povećanje i smanjenje populacije CD8+ i CD4+ T limfocita, respektivno [4]. Također smo otkrili da su centralna memorija u CD4+ i CD8+ T ćelijama i efektorska memorija u CD8+ T limfocitima smanjena kod pacijenata sa SIgAD u poređenju sa HC. Uočili smo značajno povećanje podskupine TEMRA ćelija u populaciji CD4+ i CD8+ limfocita, posebno kod pacijenata sa teškim SIgAD-om. TEMRA je treća podskupina memorije T ćelija u perifernim inflamatornim tkivima koja eksprimiraju CD45RA, ali nemaju ekspresiju CCR7 ili CD27. Kod ljudi, na akumulaciju TEMRA ćelija utiču hronične infekcije, kao što je CMV [41, 42]. Povećanje ovih prekinutih podskupina T stanica može biti posljedica kroničnog ćelijskog odgovora na infekcije kod ovih pacijenata; međutim, potrebno je izvršiti daljnje studije u vezi sa ovim fenomenom. U skladu sa našim rezultatima, Nechvatalova et al. demonstrirao proširene CD4+ i CD8+ TEMRA ćelije kod pacijenata sa SIgAD-om koji su povezani sa CMV infekcijom [43]. Nismo ispitivali CMV infekciju kod pacijenata sa SIgAD, ali povećanje broja podskupa TEMRA ćelija kod naših pacijenata moglo bi biti povezano s hroničnim infekcijama. Nedavno smo procijenili specifične odgovore antitijela na PPSV-23 kod pacijenata sa SIgAD i AT i otkrili da je 18,6% pacijenata sa SIgAD i 81,3% pacijenata sa AT imalo neadekvatan odgovor. Broj plazmablasta, B ćelija marginalne zone, prelaznih B ćelija, naivnih CD8+ T ćelija i procenat CD8+ T ćelija, IgM memorijskih B ćelija i promenjenih memorijskih B ćelija kod pacijenata sa SIgAD je bio značajno niže u grupi koja nije odgovorila nego u grupi koja je odgovorila. Iako je nedostatak specifičnih antitijela češći kod AT pacijenata nego kod pacijenata sa SIgAD [44]. Regulatorne T ćelije igraju važnu ulogu u proizvodnji IgA antitela transformišući sekreciju faktora rasta beta (TGF-) [45-47]. Otkrili smo značajno smanjene Tregs kod naših pacijenata u skladu s prethodnim objavljenim studijama [48], iako je jedna studija prijavila povećane Tregs kod pacijenata sa SIgAD [43]. Takođe je prijavljena korelacija između smanjenih Treg ćelija i težine SIgAD bolesti, posebno kod osoba sa autoimunitetom, i nedostatka IgA CSR kod pacijenata sa teškim kliničkim manifestacijama [30, 48]. Niska učestalost Treg stanica i drugih podskupina T stanica, uključujući T1 i T2 kod naših pacijenata, može biti posljedica niskih emigranta timusa uzrokovanih defektnom timopoezom i ili povećanom apoptozom ovih stanica [49]. Funkcionalni test T-ćelija mitogenom ili antigenom stimulacijom je važna karakteristika u dijagnozi različitih imunoloških poremećaja i imunodeficijencija [50]. Tradicionalno, postoji jedan protokol za procjenu funkcije T stanica zasnovan na unosu [3H] timidina nakon PHA stimulacije korištenjem radioaktivnih komponenti za koje su potrebni specifični laboratorijski uslovi, a također nije specifičan za T stanice jer može stimulirati nekoliko drugih imunoloških stanica kao što su dobro. S druge strane, najvažnija slabost je to što se ne mogu dobiti informacije o specifičnim podskupovima ćelija. CFSE test proliferacije je praktičan izbor za evaluaciju odgovora T ćelija na antigen ili mitogen kod pacijenata sa IEI, posebno SIgAD za ciljanje daljih analiza potencijalnih defekata T ćelija kod ovih pacijenata [51]. Do sada je bilo nekoliko izvještaja o defektima odgovora T-ćelija kod pacijenata sa SIgAD. Kao što se očekivalo, naša studija ne otkriva nikakvu značajnu razliku u odgovoru T ćelija između pacijenata i kontrolne grupe. Međutim, kada smo kategorizirali pacijente u dvije grupe na osnovu teških i blagih fenotipova, teški pacijenti su ukazivali na smanjenu proliferaciju T ćelija u poređenju sa blagim pacijentima. Ovaj rezultat bi mogao biti važan nalaz za kategorizaciju pacijenata sa SIgAD zbog poznavanja prognoze pacijenta. Nedavno smo izvijestili da je proliferacija T ćelija bila značajno poremećena u poređenju sa zdravim kontrolama kod pacijenata sa CVID i AT pacijenata [29, 52]. Štaviše, ovo ukazuje da pacijente sa SIgAD sa defektnom proliferacijom T-ćelija treba dalje pratiti radi preciznog medicinskog lečenja. Preporučujemo dalje studije za procjenu djelovanja funkcije T ćelija za pacijente sa SIgAD na osnovu teških i blagih fenotipova u drugim studijama. Ograničenja eksperimenta uključivala su mali broj simptomatskih pacijenata, nedostupnost mnogih od njih i e, pa čak i poboljšanje kod nekih pacijenata.
Zaključci
Naši rezultati su ukazali na značajne zlonamjernosti u obrascima B ćelija sličnih pacijentima sa CVID-om. S obzirom da CVID i teški oblici SIgAD dijele gotovo slične kliničke i imunološke fenotipove i najvjerovatnije genetsku pozadinu, ovaj pojam je predvidljiv. Na osnovu analiza fenotipa, uočili smo još neke abnormalnosti kod pacijenata sa SIgAD-om s teškim fenotipovima kao što je visoka subpopulacija CD21 niskih B ćelija i defekt proliferacije T ćelija. Shodno tome, teški bolesnici manifestiraju veći broj respiratornih infekcija u odnosu na blagi SIgAD, s brojnim brojem onih koji boluju od sinusitisa, otitisa, upale pluća i b, bronhiektazije, što sugerira dalje praćenje i preciznije liječenje ovih pacijenata. Očevi ove studije sugeriraju da bi istraživanje podskupina B i T stanica moglo biti od pomoći za bolje razumijevanje patogeneze i prognoze bolesti.
Reference
1. Aghamohammadi A, Mohammadi J, Parvaneh N, Rezaei N, Moin M, Espanol T, et al. Progresija selektivnog nedostatka IgA do uobičajene varijabilne imunodeficijencije. Int Arch Allergy Immunol. 2008;147(2):87–92.
2. Bagheri Y, Sanaei R, Yazdani R, Shekarabi M, Falak R, Mohammadi J, et al. Heterogena patogeneza selektivnog nedostatka imunoglobulina. Int Arch Allergy Immunol. 2019;179(3):232–46.
3. Nechvatalova J, Pikulova Z, Stikarovska D, Pesak S, Vlkova M, Litzman J. Subpopulacije B-limfocita kod pacijenata sa selektivnim nedostatkom IgA. J Clin Immunol. 2012;32(3):441–8.
4. Litzman J, Vlková M, Pikulová Z, Štikarovská D, Lokaj J. T i B limfocitne subpopulacije i markeri aktivacije/diferencijacije kod pacijenata sa selektivnim nedostatkom IgA. Clin Exp Immunol. 2007;147(2):249–54.
5. Lemarquis AL, Einarsdottir HK, Kristjansdottir RN, Jonsdottir I, Ludviksson BR. Tranzicione B ćelije i TLR9 odgovori su defektni u selektivnom nedostatku IgA. Front Immunol. 2018;9:909.
6. Celiksoy M, Yildiran A. Poređenje podskupina B ćelija kod primarnih imunih deficijencija napreduje sa zdravom decom sa nedostatkom antitijela. Allergol Immunopathol. 2016;44(4):331–40.
7. Marasco E, Farroni C, Cascioli S, Marcellini V, Scarsella M, Giorda E, et al. Aktivacija B-ćelija sa CD40L ili CpG-om meri funkciju podskupina B-ćelija i identifikuje specifične defekte kod pacijenata sa imunodeficijencijom. Eur J Immunol. 2017;47(1):131–43.
8. Lemarquis AL, Theodors F, Einarsdottir HK, Ludviksson BR. Mapiranje signalnih puteva povezanih sa sIgAD otkriva poremećenu IL-21-aktivaciju STAT3 B-ćelija. Front Immunol. 2019;10:403.
9. Borte S, Pan-Hammarstrom Q, Liu C, Sack U, Borte M, Wagner U, et al. Interleukin-21 obnavlja proizvodnju imunoglobulina ex vivo kod pacijenata sa uobičajenom varijabilnom imunodeficijencijom i selektivnim nedostatkom IgA. Krv. 2009;114(19):4089–98.
10. Abolhassani H, Kiaee F, Tavakol M, Chavoshzadeh Z, Mahdaviani SA, Momen T, et al. Četvrto ažuriranje iranskog nacionalnog registra primarnih imunodeficijencija: integracija molekularne dijagnoze. J Clin Immunol. 2018;38(7):816–32.
11. Aghamohammadi A, Rezaei N, Yazdani R, Delavari S, Kutukculer N, Topyildiz E, et al. Konsenzusni registar Bliskog istoka i Sjeverne Afrike o urođenim greškama imuniteta. J Clin Immunol. 2021;41(6):1339–51.
12. Seidel MG, Kindle G, Gathmann B, Quinti I, Buckland M, van Montfrans J, et al. Radne definicije registra Evropskog društva za imunodeficijencije (ESID) za kliničku dijagnozu urođenih grešaka imuniteta. J Allergy Clin Immunol Pract. 2019;7(6):1763–70.
13. Shad TM, Yousef B, Amirifar P, Delavari S, Rae W, Kokhaei P, et al. Varijabilne abnormalnosti u podskupinama T i B ćelija kod ataksije telangiektazije. J Clin Immunol. 2020:1–13.
14. TofghiZavareh F, Mirshafey A, Yazdani R, Keshtkar AA, Abolhassani H, Bagheri Y, et al. Podskupine limfocita u korelaciji sa kliničkim profilom kod pacijenata sa CVID-om bez monogenih defekata. Expert Rev Clin Immunol. 2021;17(9):1041–51.
15. Moeini Shad T, Yousef B, Amirifar P, Delavari S, Rae W, Kokhaei P, et al. Varijabilne abnormalnosti u podskupinama T i B ćelija kod ataksije telangiektazije. J Clin Immunol. 2021;41(1):76–88.
16. Azizi G, Mirshafey A, Abolhassani H, Yazdani R, Ghanavatinejad A, Noorbakhsh F, et al. Neravnoteža cirkulirajućih T pomoćnih podskupova i regulatornih T ćelija kod pacijenata sa nedostatkom LRBA: korelacija sa težinom bolesti. J Cell Physiol. 2018;233(11):8767–77.
17. Azizi G, Mirshafey A, Abolhassani H, Yazdani R, Jafarnezhad-Ansariha F, Shaghaghi M, et al. Cirkulirajuće pomoćne T-ćelije i regulatorne T-ćelije kod pacijenata sa uobičajenom varijabilnom imunodeficijencijom bez poznate monogene bolesti. J Investig Allergol Clin Immunol. 2018;28(3):172–81.
18. Reisi M, Azizi G, Kiaee F, Masiha F, Shirzadi R, Momen T, et al. Procjena plućnih komplikacija u bolesnika s primarnim imunodeficijencijskim poremećajima. Eur Ann Allergy Clin Immunol. 2017;49(3):122.
19. Cerutti A, Chen K, Chorny A. Imunoglobulinski odgovori na sučelju sluznice. Annu Rev Immunol. 2011;29:273–93.
20. Bagheri Y, Babaha F, Falak R, Yazdani R, Azizi G, Sadri M, et al. IL-10 indukuje sekreciju TGF-a, pojačanu regulaciju TGF-receptora II i lučenje IgA u B ćelijama. Eur Cytokine Netw. 2019;30(3):107–13.
21. Ozkan H, Atlihan F, Genel F, Targan S, Gunvar T. Deficit IgA i/ili IgG podklase kod djece s rekurentnim respiratornim infekcijama i njegov odnos s kroničnim oštećenjem pluća. J Investig Allergol Clin Immunol. 2005;15(1):69–74.
22. Tavakol M, Jamee M, Azizi G, Sadri H, Bagheri Y, Zaki-Dizaji M, et al. Dijagnostički pristup pacijentima sa sumnjom na primarnu imunodeficijenciju. Endocr Metab meta za lijekove protiv imunološkog poremećaja. 2020;20(2):157–71.
23. Resnick ES, Moshier EL, Godbold JH, Cunningham-Rundles C. Morbiditet i mortalitet kod uobičajenog varijabilnog imunodeficijencije tokom 4 decenije. Krv. 2012;119(7):1650–7.
24. Yazdani R, Abolhassani H, Asgardoon M, Shaghaghi M, Modaresi M, Azizi G, et al. Infektivne i neinfektivne plućne komplikacije u bolesnika s primarnim poremećajima imunodeficijencije. J Investig Allergol Clin Immunol. 2017;27(4):213–24.
25. Ahmadi M, Nouri M, Babaloo Z, Farzadi L, Ghasemzadeh A, Hamdi K, et al. Liječenje intravenskim imunoglobulinom (IVIG) modulira Th17 periferne krvi i regulatorne T ćelije kod pacijenata sa ponovljenim pobačajem: nerandomizirano, otvoreno kliničko ispitivanje. Immunol Lett. 2017;192:12–9.
26. Yazdani R, Seify R, Ganjalikhani-Hakemi M, Abolhassani H, Eskandari N, Golsaz-Shirazi F, et al. Poređenje različitih klasifikacija za pacijente sa uobičajenom varijabilnom imunodeficijencijom (CVID) korištenjem mjerenja podskupina B-ćelija. Allergol Immunopathol (Madr). 2017;45(2):183–92.
27. Aghamohammadi A, Abolhassani H, Rezaei N. Bolesti primarne imunodeficijencije u Iranu: prošlost, sadašnjost i budućnost. Arch Iran Med. 2021. https://doi. org/10.34172/aim.2021.18.
28. Aghamohammadi A, Abolhassani H, Biglari M, Abolmaali S, Moazzami K, Tabatabaeiyan M, et al. Analiza B-ćelija s komutiranom memorijom kod pacijenata sa nedostatkom IgA. Int Arch Allergy Immunol. 2011;156(4):462–8.
29. Yousef B, Amirifar P, Delavari S, Rae W, Kokhaei P, Abolhassani H, et al. Varijabilne abnormalnosti u podskupinama T i B ćelija kod ataksije telangiektazije. J Clin Immunol. 2020. https://doi.org/10.1007/s10875-020-00881-9.
30. Abolhassani H, Gharib B, Shahinpour S, Masoom SN, Havaei A, Mirminachi B, et al. Autoimunost kod pacijenata sa selektivnim nedostatkom IgA. J Investig Allergol Clin Immunol. 2015;25(2):112–9.
31. Arkwright PD, Abinun M, Cant AJ. Autoimunost kod primarnih bolesti imunodeficijencije ljudi. Krv. 2002;99(8):2694–702.
32. Cerutti A, Cols M, Puga I. Marginalna zona B ćelije: vrline limfocita koji proizvode urođena antitijela. Nat Rev Immunol. 2013;13(2):118–32.
33. Bukowska-Straková K, Kowalczyk D, Baran J, Siedlar M, Kobylarz K, Zembala M. Kompartment B-ćelija u perifernoj krvi djece s različitim tipovima primarne humoralne imunodeficijencije. Pediatr Res. 2009;66(1):28–34.
34. Karaman SBES, Gülez N, Genel F. Značaj podskupina B-ćelija kod pacijenata sa neklasifikovanom hipogamaglobulinemijom i povezanost sa zahtjevom za intravenskom zamjenom imunoglobulina. Iran J Immunol. 2018;15(1):1–13.
35. Patuzzo G, Mazzi F, Vella A, Ortolani R, Barbieri A, Tinazzi E, et al. Imunofenotipska analiza B limfocita kod pacijenata sa uobičajenom varijabilnom imunodeficijencijom: identifikacija CD23 kao korisnog markera u definiciji bolesti. ISRN Immunol. 2013. https://doi.org/10. 1155/2013/512527.
36. Patuzzo G, Barbieri A, Tinazzi E, Veneri D, Argentino G, Moretta F, et al. Autoimunost i infekcije kod uobičajene varijabilne imunodeficijencije (CVID). Autoimmun Rev. 2016;15(9):877–82.
37. Rakhmanov M, Keller B, Gutenberger S, Foerster C, Hoenig M, Driessen G, et al. Cirkulirajuće CD21low B ćelije kod uobičajene varijabilne imunodeficijencije nalikuju urođenim B ćelijama koje potiču tkivo. Proc Natl Acad Sci. 2009;106(32):13451–6.
38. Isnardi I, Ng YS, Menard L, Meyers G, Saadoun D, Srdanović I, et al. Receptor komplementa 2/CD21-humane naivne B ćelije sadrže uglavnom autoreaktivne klonove koji ne reaguju. Krv. 2010;115(24):5026–36.
39. Sims GP, Ettinger R, Shirota Y, Yarboro CH, Illei GG, Lipsky PE. Identifikacija i karakterizacija cirkulirajućih ljudskih tranzicijskih B ćelija. Krv. 2005;105(11):4390–8.
40. Lemarquis AL, Einarsdottir HK, Kristjansdottir RN, Jonsdottir I, Ludviksson BR. Tranzicione B ćelije i TLR9 odgovori su defektni u selektivnom nedostatku IgA. Front Immunol. 2018. https://doi.org/10.3389/fmmu.2018. 00909.
41. Willinger T, Freeman T, Hasegawa H, McMichael AJ, Callan MF. Molekularni potpisi razlikuju ljudsku centralnu memoriju od podskupina CD8 T ćelija efektorske memorije. J Immunol. 2005;175(9):5895–903.
42. Martin dr., Badovinac VP. Definiranje memorije CD8 T ćelije. Front Immunol. 2018;9:2692.
43. Nečhvatalova J, Pavlik T, Litzman J, Vlkova M. Terminalno diferencirane memorijske T ćelije su povećane kod pacijenata sa uobičajenom varijabilnom imunodeficijencijom i selektivnim nedostatkom IgA. Cent Eur J Immunol. 2017;42(3):244–51.
44. Khanmohammadi S, Shad TM, Delavari S, Shirmast P, Bagheri Y, Azizi G, et al. Procjena odgovora specifičnih antitijela kod pacijenata sa selektivnim nedostatkom IgA i telangiektazijom ataksije. Endocr Metab meta za lijekove protiv imunološkog poremećaja. 2022;22(6):640–9.
45. Cazac BB, Roes J. TGF- receptor kontroliše odgovor B ćelija i indukciju IgA in vivo. Imunitet. 2000;13(4):443–51.
46. Van Vlasselaer P, Punnonen J, De Vries J. Transformirajući faktor rasta-beta usmjerava prebacivanje IgA u ljudskim B ćelijama. J Immunol. 1992;148(7):2062–7.
47. Cerutti A, Rescigno M. Biologija odgovora intestinalnog imunoglobulina A. Imunitet. 2008;28(6):740–50.
48. Soheili H, Abolhassani H, Arandi N, Khazaei HA, Shahinpour S, Hirbod Mobarakeh A, et al. Procjena prirodnih regulatornih T ćelija kod subjekata sa selektivnim nedostatkom IgA: od starije ideje do novih mogućnosti. Int Arch Allergy Immunol. 2013;160(2):208–14.
49. Yazdani R, Fatholahi M, Ganjalikhani-Hakemi M, Abolhassani H, Azizi G, Hamid KM, et al. Uloga apoptoze kod uobičajene varijabilne imunodeficijencije i selektivnog nedostatka imunoglobulina A. Mol Immunol. 2016;71:1–9.
50. McCusker C, Warrington R. Primary immunodeficiency. All Asth Clin Immun. 2011;7(Suppl 1):S11.
51. Marits P, Wikström AC, Popadic D, Winqvist O, Thunberg S. Procjena funkcije T i B limfocita u kliničkoj praksi korištenjem testa proliferacije zasnovanog na protočnoj citometriji. Clin Immunol. 2014;153(2):332–42.
52. TofghiZavareh F, Mirshafey A, Yazdani R, Keshtkar AA, Abolhassani H, Mahdaviani SA, et al. Imunofenotipska i funkcionalna analiza podskupina limfocita kod pacijenata sa uobičajenom varijabilnom imunodeficijencijom bez monogenih defekata. Scand J Immunol. 2022;96(1):e13164.
